Sachverhalt:
A. Gegenstand
Gegenstand des vorliegenden Urteils bildet die von der Wettbewerbskommission
(WEKO) am 19. Dezember 2016 erlassene Verfügung im Verfahren Nr. 32-0249, Kommerzialisierung
von elektronischen Medikamenteninformationen (nachfolgend: angefochtene Verfügung). Danach verfügte
die damalige Galenica AG (nachfolgend: Galenica) mittels ihrer Tochtergesellschaft HCI Solutions AG (nachfolgend:
HCI) auf dem Markt der veredelten, maschinenlesbaren Daten betreffend Medikamenteninformationen sowie
auf dem Markt für den Zugang zu elektronischen Datensätzen betreffend Medikamenteninformationen
in der Schweiz über eine marktbeherrschende Stellung. In dieser Stellung hat sie unzulässige
Wettbewerbsbeschränkungen nach Art. 7 des Bundesgesetzes vom 6. Oktober 1995 über
Kartelle und andere Wettbewerbsbeschränkungen (Kartellgesetz, KG, SR
des Bundesgesetzes vom 6. Oktober 1995 über
Kartelle und andere Wettbewerbsbeschränkungen (Kartellgesetz, KG, SR 251) verwirklicht; indem
sie einerseits (i) den Absatz der Konkurrenten durch eine Alleinbezugspflicht der Softwarehäuser
sowie durch eine Untersagung der anderweitigen Verwendung der Software-Strukturen eingeschränkt
und andererseits (ii) durch die vertragliche Koppelung von Dienstleistungen den Zulassungsinhaberinnen
den Kauf zusätzlicher Leistungen aufgedrängt hat. Die beiden Unternehmen wurden mit einem Betrag
in der Höhe von Fr. 4'546'123.- sanktioniert.
251) verwirklicht; indem
sie einerseits (i) den Absatz der Konkurrenten durch eine Alleinbezugspflicht der Softwarehäuser
sowie durch eine Untersagung der anderweitigen Verwendung der Software-Strukturen eingeschränkt
und andererseits (ii) durch die vertragliche Koppelung von Dienstleistungen den Zulassungsinhaberinnen
den Kauf zusätzlicher Leistungen aufgedrängt hat. Die beiden Unternehmen wurden mit einem Betrag
in der Höhe von Fr. 4'546'123.- sanktioniert.
Die folgenden
Ausführungen zu den Beschwerdeführerinnen, den Medikamenteninformationen,
den Datenbanken sowie
zur Vertragsgestaltung und den Geschehensabläufen sollen eine grundlegende
Übersicht über den Verfahrensgegenstand bieten. Spezifische Abhandlungen von Einzelheiten erfolgen
zu den jeweiligen Detailaspekten im Rahmen der Erwägungen.
B. Beschwerdeführerinnen
B.a Vifor
Pharma AG
B.a.a Galenica
war bis Anfang 2017 Muttergesellschaft einer international tätigen schweizerischen Pharmazie- und
Logistikunternehmensgruppe. Die Gesellschaften der Galenica-Gruppe waren in die zwei Hauptbereiche "Vifor
Pharma" und "Galenica Santé" unterteilt. Die der Geschäftseinheit "Vifor
Pharma" zugeteilten Gesellschaften entwickelten, produzierten und vertrieben weltweit pharmazeutische
Produkte. Der Unternehmensbereich "Galenica Santé" unterteilte sich in die Geschäftsbereiche
"Products & Brands", "Retail" und "Services". Die ersten beiden Bereiche
vermarkteten Produkte für die Gesundheit, Schönheit und das Wohlbefinden und betrieben Apotheken.
Der Geschäftsbereich "Services" umfasste das Anbieten von Wholesale und Prewholesale Logistikdienstleistungen
sowie die Entwicklung und den Betrieb von Datenbanken und Softwarelösungen.
B.a.b Mittlerweile
wurden die Geschäftseinheiten "Vifor Pharma" und "Galenica Santé" zu zwei
eigenständigen, börsenkotierten Gesellschaften entwickelt. Am 13. Februar 2017 wurde die Galenica
Santé AG (nachfolgend: Galenica Santé) mittels Sacheinlage und -übernahme gegründet.
Seit dem 7. April 2017 agiert Galenica Santé als eigenständiges Unternehmen und ist an
der Schweizer Börse kotiert. An der Generalversammlung der Galenica vom 11. Mai 2017 wurde
entschieden, die Galenica in Vifor Pharma AG (nachfolgend: Vifor) umzufirmieren. Die Galenica Santé
firmiert seit dem 12. Mai 2017 wiederum unter Galenica AG.
B.b HCI
Solutions AG
B.b.a HCI
war bis Anfang 2016 die Managementfirma von Documed AG (nachfolgend: Documed) und e-mediat AG (nachfolgend:
e-mediat). Sie befasste sich mit der Entwicklung, Vermarktung und dem Betrieb netzwerkorientierter Software
für Partner im Gesundheitswesen, der Vermarktung von Informationen für das Gesundheitswesen
im In- und Ausland sowie mit dazugehörigen Dienstleistungen.
B.b.b Mit
Fusionsvertrag vom 8. Februar 2016 wurden die Gesellschaften Documed und e-mediat (s. unten E. B.c)
per 1. Januar 2016 in HCI fusioniert, sodass HCI deren Geschäftstätigkeit übernahm.
B.b.c HCI
war bis Anfang 2017 zu 100% eine Tochtergesellschaft der damaligen Galenica. Sie war der Geschäftseinheit
"Galenica Santé" und dort wiederum dem Geschäftsbereich "Services" angegliedert.
Im Rahmen der erwähnten Umstrukturierungen der ehemaligien Galenica-Gruppe (s. oben E. B.a)
wurde die Beteiligung von HCI mit Sacheinlagevertrag vom 13. Februar 2017 auf die Galenica Santé,
unterdessen firmierend unter Galenica AG, übertragen.
B.c Documed
AG und e-mediat AG
B.c.a Documed
befasste sich mit dem Betrieb eines medizinisch-pharmazeutischen Verlages, welcher Informationen über
in der Schweiz zugelassene Arzneimittel sammelte, aufbereitete und der Kundschaft in Form eines Kompendiums
zur Verfügung stellte. Dieses Kompendium war zunächst als Print-Version, später auch in
elektronischer Form erhältlich. Seit 2013 wird es nur noch in elektronischer Form herausgegeben
(s. unten E. D.a).
B.c.b E-mediat
befasste sich mit der Entwicklung, dem Unterhalt und der Verteilung von Stammdaten zu pharmazeutischen
Produkten. Früher wurden diese Datensammlungen im Format "Galdat" weitergegeben. Später
entwickelte und unterhielt e-mediat die sogenannten INDEX-Produkte (s. unten E. D.b.).
C. Medikamenteninformationen
Im Gesundheitswesen bedarf es für die Beratung, Verschreibung und Abgabe von Arzneimitteln an
die Patientinnen und Patienten, das Bestellwesen sowie die Abrechnung mit den Krankenkassen und weiteren
Versicherungen zahlreiche Informationen betreffend Arzneimittel und Akteure. Daneben sind auch Informationen
von weiteren Produkten wesentlich, so namentlich Mittel und Gegenstände, die der Behandlung oder
Untersuchung im Sinne einer Überwachung der Behandlung der Krankheit und ihrer Folgen dienen, weitere
Medizinprodukte im Sinne von Art. 4 Abs. 1 Bst. b des Bundesgesetzes über Arzneimittel und
Medizinprodukte vom 15. Dezember 2000 (Heilmittelgesetz, HMG, SR
des Bundesgesetzes über Arzneimittel und
Medizinprodukte vom 15. Dezember 2000 (Heilmittelgesetz, HMG, SR 812.21) und Non-Pharma Produkte
wie Verbandsmaterial, Medizinal-, Praxis- und Laborbedarf, Heilnahrung, Kurmittel, Nahrungsergänzungsmittel,
Trink- und Sondernahrung, Körperpflege, etc.
812.21) und Non-Pharma Produkte
wie Verbandsmaterial, Medizinal-, Praxis- und Laborbedarf, Heilnahrung, Kurmittel, Nahrungsergänzungsmittel,
Trink- und Sondernahrung, Körperpflege, etc.
C.a Arzneimittelinformationen
C.a.a Unter
Medikamenteninformationen fallen insbesondere Arzneimittelinformationen. Diese können unterteilt
werden in Fachinformationen und Patienteninformationen. Bei den Fachinformationen handelt es sich um
die Informationen über ein Arzneimittel, welche an Fachpersonen gerichtet sind. Die Patienteninformationen
sind demgegenüber die Informationen über ein Arzneimittel, die an die Patientinnen und Patienten
gerichtet und in der Packungsbeilage eines Arzneimittels enthalten sind. Die Fach- und Patienteninformationen
enthalten Informationen über Wirkstoffe, Dosierung, Anwendung, Nebenwirkungen etc. (vgl. Anhang
4 und 5 der Verordnung des Schweizerischen Heilmittelinstituts über die Anforderungen an die Zulassung
von Arzneimitteln vom 9. November 2001 [Arzneimittel-Zulassungsverordnung, AMZV, SR 812.212.22]).
812.212.22]).
C.a.b Bevor
Arzneimittel durch Fachpersonen an Patientinnen und Patienten verschrieben und abgegeben werden können,
müssen sie durch Swissmedic, die Schweizerische Zulassungs- und Aufsichtsbehörde für Arzneimittel
und Medizinprodukte, zugelassen werden. Im Zulassungsverfahren haben die Zulassungsinhaberinnen Swissmedic
die Fach- und Patienteninformationen in deutscher oder französischer Sprache einzureichen. Diese
werden von Swissmedic geprüft und anschliessend freigegeben.
C.a.c Nach
Art. 13 und 14
und 14 AMZV i.V.m. Art. 16a
AMZV i.V.m. Art. 16a der Verordnung über Arzneimittel vom 17. Oktober 2001 (Arzneimittelverordnung,
VAM, SR
der Verordnung über Arzneimittel vom 17. Oktober 2001 (Arzneimittelverordnung,
VAM, SR 812.212.21) müssen die Fach- und Patienteninformationen den für die zur Verschreibung,
Abgabe oder Anwendung von Humanarzneimitteln berechtigten Personen "auf geeignete Weise zur Verfügung
gestellt werden". Aus den Anhängen 4 und 5
812.212.21) müssen die Fach- und Patienteninformationen den für die zur Verschreibung,
Abgabe oder Anwendung von Humanarzneimitteln berechtigten Personen "auf geeignete Weise zur Verfügung
gestellt werden". Aus den Anhängen 4 und 5 AMZV folgt, dass es sich dabei um eine Veröffentlichung
handeln muss.
AMZV folgt, dass es sich dabei um eine Veröffentlichung
handeln muss.
C.a.d Gemäss
den Anordnungen von Swissmedic hatte die Veröffentlichung bis Juni 2011 in einer Sammlung von Fach-
bzw. Patienteninformationen zu erfolgen, die auf Vollständigkeit angelegt war. Die Fachinformationen
waren sowohl in einer elektronischen wie auch in einer gedruckten Sammlung zu veröffentlichen. Für
Patienteninformation war eine Veröffentlichung in einer elektronischen Sammlung ausreichend (Swissmedic-Journal
1/2004, S. 23 f., 2/2004, S. 148 und 3/2008, S. 164). Dies war ausschliesslich bei Documed möglich.
Mit Bundesgerichtsurteil BGE 134 III 166 wurde der urheberrechtliche Schutz des Kompendiums verneint.
Die sprachliche Gestaltung der Texte erreiche die erforderliche Individualität nicht. Infolge dieses
Urteils war deshalb ab 2008 die elektronische Publikation auch durch die ywesee GmbH (nachfolgend: ywesee)
möglich. Ein gedrucktes Gesamtwerk bot bis 2012 aber nur Documed an; und zwar das sogenannte Kompendium.
C.a.e Aus
diesen Anordnungen von Swissmedic resultierte ein faktischer Zwang der Zulassungsinhaberinnen zum Abschluss
eines kostenpflichtigen Publikationsvertrages mit Documed oder ywesee. Das Bundesverwaltungsgericht entschied
mit BVGE 2011/60, dass diese Verpflichtung als Eingriff in die Wirtschaftsfreiheit (Art. 27 der Bundesverfassung
der Schweizerischen Eidgenossenschaft vom 18. April 1999 [BV, SR
der Bundesverfassung
der Schweizerischen Eidgenossenschaft vom 18. April 1999 [BV, SR 101]) einer formell-gesetzlichen Grundlage
bedürfe, die nicht vorhanden sei. Zudem erwog das Bundesverwaltungsgericht, eine Publikation durch
Swissmedic selbst sei zulässig bzw. naheliegend (BVGE 2011/60 E. 4.5 und 6.3).
101]) einer formell-gesetzlichen Grundlage
bedürfe, die nicht vorhanden sei. Zudem erwog das Bundesverwaltungsgericht, eine Publikation durch
Swissmedic selbst sei zulässig bzw. naheliegend (BVGE 2011/60 E. 4.5 und 6.3).
C.a.f Mit
Mitteilung vom 27. Juni 2011 verzichtete Swissmedic deshalb darauf, die Zulassungsinhaberinnen zur Publikation
in einem Gesamtwerk zu verpflichten, empfahl aber die Publikation im Kompendium von Documed oder bei
ywesee vorübergehend beizubehalten. Im Herbst 2011 entscheid Swissmedic, eine eigene umfassende
elektronische Datenbank der Arzneimittelinformationen zu betreiben, und schrieb den entsprechenden Auftrag
mittels WTO-Ausschreibung öffentlich aus. HCI erhielt den Zuschlag für den Aufbau und den Betrieb
dieser neuen Publikationsplattform, das gegenwertig bestehende Arzneimittelinformationssystem (AIPS).
C.a.g AIPS
ist eine kostenfreie Plattform, auf der alle behördlich genehmigten Fach- und Patienteninformationen
von Arzneimitteln publiziert werden. Die auf AIPS gesammelten Arzneimittelinformationen können sowohl
vom Fachpublikum als auch der Öffentlichkeit eingesehen werden. Alle Daten können im XML-Format
von Datenveredlern kostenlos heruntergeladen werden. Die Daten sind nach Angaben von Swissmedic beschränkt
auf die Informationen gemäss den gesetzlichen Anforderungen der AMZV (Art. 13 und 14
und 14 AMZV, Anhang
4 und 5). Mit der Veröffentlichung der Arzneimittelinformationen auf AIPS erfüllen die Zulassungsinhaberinnen
ihre gesetzliche Pflicht zur Publikation. Die Veröffentlichung auf AIPS ist für die Zulassungsinhaberinnen
kostenlos. AIPS wird indirekt über die Zulassungsgebühren finanziert.
AMZV, Anhang
4 und 5). Mit der Veröffentlichung der Arzneimittelinformationen auf AIPS erfüllen die Zulassungsinhaberinnen
ihre gesetzliche Pflicht zur Publikation. Die Veröffentlichung auf AIPS ist für die Zulassungsinhaberinnen
kostenlos. AIPS wird indirekt über die Zulassungsgebühren finanziert.
C.a.h Die
Veröffentlichung der Arzneimittelinformationen erfolgt somit seit 1. Januar 2013 auf AIPS. Seit
dem 1. Januar 2019 ist anstelle von Swissmedic die Stiftung Refdata mit der Publikation der Fach- und
Publikumsinformation bezüglich Human- und Tierarzneimitteln betraut (Art. 67 Abs. 3 nHMG). Refdata
hat für den Betrieb der Publikationsplattform AIPS weiterhin HCI beauftragt.
nHMG). Refdata
hat für den Betrieb der Publikationsplattform AIPS weiterhin HCI beauftragt.
C.a.i Die
Publikation der Arzneimittelinformation ist zur Gewährleistung der Sicherheit der Anwendung von
Arzneimitteln wichtig. Die Medizinal- und Fachpersonen benötigen einen schnellen Zugang zu Informationen
über die von ihnen verschriebenen oder abgegebenen Arzneimittel oder über Arzneimittel, die
von ihren Patienten bereits eingenommen werden. Ein vollständiges Verzeichnis, das alle in der Schweiz
zugelassenen Arzneimittelinformationen beinhaltet, ist deshalb von grossem Nutzen (vgl. BVGE 2011/60
E. 5.2; Medienmitteilung Swissmedic vom 26. Juli 2011, https://www.swissmedic.ch/swissmedic/de/home/news/mitteilungen/archiv/praxisaenderung-betreffend-die-publikation-von-arzneimittelinfor.html
[abgerufen am 07.01.2022]).
C.b Weitere
relevante Informationen und Listen
C.b.a Neben
den Arzneimittelinformationen gibt es zahlreiche weitere Informationen und Listen, die für die Abwicklung
der Prozesse des Vertriebs, Verschreibung, Verkaufs und Abrechnung der Arzneimittel nötig sind.
Dabei handelt es sich namentlich um die Spezialitätenliste, die vom Bundesamt für Gesundheit
(BAG) herausgegeben wird und sämtliche Arzneimittel enthält, die von der obligatorischen Krankenversicherung
bei ärztlicher Verschreibung vergütet werden. Für jedes Arzneimittel auf der Liste werden
verschiedene Identifikatoren erfasst, wie beispielsweise das Datum der Aufnahme auf die Liste, der mit
dem Hersteller vereinbarte Fabrikabgabepreis, der Publikumspreis, die Limitationen und die Kategorisierung
gemäss Inhalts- und Stoffliste von Swissmedic und BAG. Die Informatikdienstleistungen und der administrative
Support im Bereich Datenverarbeitung erfolgt durch HCI (früher e-mediat).
C.b.b Weiter
gibt es die Mittel- und Gegenstände Liste (MiGeL), die ebenfalls vom BAG herausgegeben wird. Sie
enthält Mittel- und Gegenstände, die der Behandlung oder Untersuchung im Sinne einer Überwachung
der Behandlung einer Krankheit und ihrer Folgen dienen, die von den Versicherten selbst oder allenfalls
unter Beizug von nichtberuflich an der Untersuchung oder Behandlung mitwirkenden Personen angebracht
und/oder verwendet werden können und von der obligatorischen Krankenversicherung übernommen
werden (Art. 20 der Verordnung des EDI über Leistungen in der obligatorischen Krankenpflegeversicherung
vom 29. September 1995 [Krankenpflege-Leistungsverordnung, KLV, SR 832.112.31]).
832.112.31]).
C.b.c Zudem
gibt es die Datenbank refdatabase (vorherige Bezeichnung swissindex), die durch die Stiftung Refdata
bereitgestellt wird und Stammdaten über die Akteure des Gesundheitswesens (Adressen, Abrechnungsnummern
etc.) sowie über Pharma Artikel (von Swissmedic zugelassene Arzneimittel und immunbiologische Erzeugnisse)
enthält. Die Referenzierung der einzelnen Datensätze erfolgt gemäss dem internationalen
GS1-Standard: GLN (Global Location Number) für Partner und GTIN (Global Trade Item Number, s. unten)
für Artikel. Die täglich aktualisierte Datenbank ist lizenzkostenfrei verfügbar. Der Betrieb
der Datenbank refdatabase erfolgt durch HCI (früher durch e-mediat).
C.b.d Eine
wichtige Rolle spielen sodann auch diverse Codes und Identifikationsnummern, insbesondere der Pharmacode
und der GTIN-Code. Der Pharmacode ist ein Referenzcode, der von HCI (früher e-mediat) Pharma- und
Non-Pharma-Produkten kostenpflichtig zugeteilt wird. Es handelt sich um einen siebenstelligen numerischen
Identifikationsschlüssel, mit welchem sich Produkte im Schweizer Gesundheitsmarkt eindeutig referenzieren
lassen. Er fungiert als Referenzcode in den Datensammlungen von HCI und dient den mit diesen Daten arbeitenden
Softwareunternehmen zur Definition ihrer Schnittstellen. Vor der Einführung bzw. bis zur Durchsetzung
des GTIN-Codes war der Pharmacode als Referenznummern auf allen Marktstufen essentiell für den Vertrieb,
die Verschreibung, den Verkauf und die Abrechnung aller Arzneimittel. Er wurde bis Ende 2014 in der Spezialitätenliste
des BAG aufgeführt, wobei er bis Ende März 2013 als Referenznummer diente. Auch in der Datenbank
refdatabase wurde er bis mindestens Ende 2016 verwendet. Beim GTIN-Code, dessen frühere Bezeichnung
EAN-Code ist (European Article Number), handelt es ich um einen internationalen standardisierten Identifikationsschlüssel,
mit welchen sich ein Artikel eindeutig kennzeichnen lässt. Er wird durch die Stiftung Refdata kostenpflichtig
vergeben. Seit 1. April 2013 wird er beispielsweise in der Spezialitätenliste des BAG als Referenzierungsnummer
verwendet.
C.c Nachfragerinnen
und Nachfrager der Medikamenteninformationen
C.c.a Genutzt
und nachgefragt werden (elektronische) Medikamenteninformationen insbesondere von den Leistungserbringerinnen
und -erbringern, Vertriebsunternehmen und Kostenträgern. Zu den Leistungserbringerinnen und -erbringer
zählen (i) Ärztinnen und Ärzte, (ii) Spitäler, (iii) Apotheken, (iv) Drogerien und
(v) Heime. Sie benötigen Medikamenteninformationen für die Abgabe und Verschreibung von Arzneimittel,
für Beratungs- und Informationsaufgaben, für die Führung von elektronischen Patientendossier,
zur Bewirtschaftung des Lagers, etc.
C.c.b Abgesehen
von den Spitälern beziehen Leistungserbringerinnen und -erbringer die Arzneimittel und allenfalls
weitere Produkte grundsätzlich von Grossisten. Die Grossisten übernehmen die Feinverteilung
und haben individuelle Sortimente, Preise, Codes etc., welche im Zusammenhang mit dem Bestellwesen von
Bedeutung sind. Prewholesaler sind Logistikunternehmen für pharmazeutische Produkte und übernehmen
Dienstleistungen der Lagerung und der Vertriebslogistik für Arzneimittelhersteller, die diese Aufgaben
ausgelagert haben. Der Transport von Pharmaprodukten wird oftmals an spezialisierte Transportunternehmen
ausgelagert. Daneben können Prewholesaler den Herstellern verschiedene weitere Dienstleistungen
anbieten, wie beispielsweise die Abwicklung des Bestellwesens, Rechnungsstellung, Inkasso oder die Übernahme
des Delkredererisikos.
C.c.c Zu
den Kostenträgern gehören Krankenversicherungen, Unfallversicherungen und die Invalidenversicherung.
Bei denjenigen Arzneimitteln, die von den Krankenversicherungen im Rahmen der Grund- oder Zusatzversicherung
übernommen werden, hat der Abrechnungsprozess mit den Krankenversicherungen zu erfolgen (vgl. Art.
42 des Bundesgesetzes über die Krankenversicherung vom 18. März 1994 [KVG, SR
des Bundesgesetzes über die Krankenversicherung vom 18. März 1994 [KVG, SR 832.10]).
Für Kosten für die Heilbehandlung nach einem Unfall (vgl. Art. 10
832.10]).
Für Kosten für die Heilbehandlung nach einem Unfall (vgl. Art. 10 des Bundesgesetzes
über die Unfallversicherung vom 20. März 1981 [UVG, SR
des Bundesgesetzes
über die Unfallversicherung vom 20. März 1981 [UVG, SR 832.20]), benötigen die
Unfallversicherungen entsprechende Informationen für die Abrechnung der Arzneimittel und die Invalidenversicherung
benötigt diese für die Abrechnung solcher Kosten in Folge Invalidität (Art. 4
832.20]), benötigen die
Unfallversicherungen entsprechende Informationen für die Abrechnung der Arzneimittel und die Invalidenversicherung
benötigt diese für die Abrechnung solcher Kosten in Folge Invalidität (Art. 4 des
Bundesgesetzes über die Invalidenversicherung vom 19. Juni 1959 [IVG, SR
des
Bundesgesetzes über die Invalidenversicherung vom 19. Juni 1959 [IVG, SR 831.2]).
831.2]).
C.c.d Alle
genannten Tätigkeiten erfolgen weitgehend EDV-unterstützt und laufen vornehmlich und zunehmend
elektronisch ab.
C.d Fluss
der elektronischen Medikamenteninformationen
C.d.a 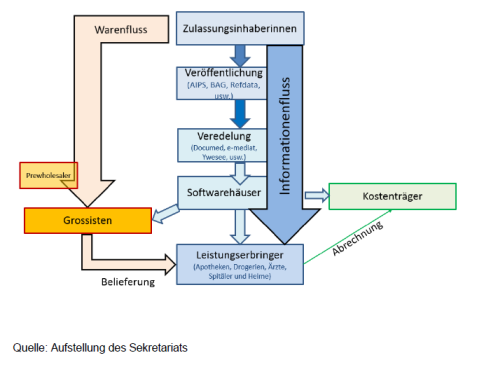
Die
Vorinstanz illustrierte den Datenfluss der Medikamenteninformationen wie folgt:
C.d.b Die
Arzneimittelinformationen werden seit 2013 aufgrund der regulatorischen Pflicht auf AIPS veröffentlich
(Veröffentlichung; s. oben E. C.a).
Andere Medikamenteninformationen, die für den Vertrieb, die Abgabe und die Abrechnung von Medikamenten
notwendig sind, werden ebenfalls veröffentlicht (z.B. Spezialitätenliste, Refdata-Datenbank,
MiGeL; s. oben E. C.b).
C.d.c Die
auf AIPS publizierten Arzneimittelinformationen und die weiteren Medikamenteninformationen werden veredelt,
um diese veredelten Daten anschliessend für die Nutzung durch Abnehmer von strukturierten Daten-sätzen
zu kommerzialisieren. Die Veredelung kann in folgende Arbeitsschritte
unterteilt werden:
- (i)
Aggregation: Die Daten werden aus verschiedenen Primärquellen (AIPS, Spezialitätenliste, etc.)
aggregiert und in einer Datenbank vereint. Daten, die selbst generiert werden, können ergänzt
werden (z.B. Produktabbildungen).
- (ii)
Strukturierung: Die Medikamenteninformationen werden in eine bestimmte Struktur gebracht, damit auf Basis
der Daten weitere Funktionen wie beispielsweise die Interaktionsprüfung programmiert werden können.
Welche Struktur ein Datensatz hat, ist für jede Datenbank unterschiedlich. Die Anzahl der Datenfelder,
die strukturiert werden, hängt von der Anzahl und Aufteilung der Daten ab.
- (iii)
Codierung: Die bei der Strukturierung verwendeten Datenfelder werden in einen maschinenlesbaren Code
"übersetzt". Anhand dieser Codierung sind auch Interaktionsprüfungen zwischen verschiedenen
Produkten möglich.
C.d.d Die
veredelten Medikamenteninformationen werden in Informatiksysteme von Softwarehäusern eingefügt
(Integration in Softwaresysteme). Die Softwarehäuser programmieren
und unterhalten Informatikprogramme, die auf die Bedürfnisse der verschiedenen Akteure im Gesundheitswesen
ausgerichtet sind. Die einzelnen Softwarehäuser bieten verschiedene Tools an, so beispielsweise
Praxisadministrationssysteme für Ärztinnen und Ärzte, die etwa Debitorenbewirtschaftung
oder elektronische Patientendossiers enthalten können, Pflegemanager für Heime oder Rezeptverkauf
und Lagerbewirtschaftung für Apotheken.
C.d.e Die
Bereitstellung der Daten kann auf verschiedene Wege erfolgen:
- Der
Datenveredler verkauft die Daten den Softwarehäusern. Die Softwarehäuser verkaufen anschliessend
die Software und bilden einen Gesamtpreis für Software und Daten.
- Der
Datenveredler bietet selbst eine Software an und vertreibt die Daten zusammen mit der Software.
- Die
Daten werden den Endabnehmern zur Software separat angeboten, indem die Daten entweder vom Datenveredler
direkt oder über die Softwarehäuser als Vermittler verkauft werden.
C.d.f Diese
veredelten maschinenlesbaren Medikamenteninformationen dienen den unter E. C.c
erwähnten Nachfragerinnen und Nachfragern zur Erfüllung ihrer Aufgaben bei der Führung
von Patientendossiers, der Beratung von Patientinnen und Patienten, der Verschreibung und dem Verkauf
der Arzneimittel, der Lagerbewirtschaftung und dem Bestellwesen sowie der Abrechnung mit den Kostenträgern
(Nutzung durch Endabnehmer).
D. Datenbanken
D.a Compendium
Das Compendium von HCI (früher Documed) stellt eine Informationsplattform zu rezeptpflichtigen
und rezeptfreien Arzneimitteln dar, welches zuerst in Buchform (Kompendium), später auf CD-ROM und
aktuell auf www.compendium.ch sowie als App für Android und iPhone verfügbar ist. Es enthält
die Fach- und Patienteninformationen der Arzneimittel sowie gemäss Angaben der Beschwerdeführerinnen
markt- und verschreibungsrelevante Daten und von HCI erstellte redaktionelle Arzneimittelkurzinformationen.
Für das Compendium werden die Daten - anders als bei AIPS, welches die Arzneimittelinformationen
als Fliesstext enthält - strukturiert und codiert, d.h. in programmierter Form verfügbar
gemacht.
D.b INDEX-Datenbank
D.b.a Die
INDEX-Datenbanken von HCI (früher e-mediat) waren im Untersuchungszeitraum in sieben benutzerspezifische
Datenangebote aufgeteilt, welche auf der gleichen Datenbank basierten und in ähnlichen Strukturen
ausgeliefert wurden. Umfang und Detaillierungsgrad waren jedoch unterschiedlich.
- careINDEX
richtet sich an Heime und enthielt rund 100'000 Artikel (insb. Arzneimittel, Medizinprodukte, Verbrauchsmaterialien,
Praxis- und Laborbedarf);
- drogINDEX
richtet sich an Drogerien und enthielt rund 180'000 Artikel (insb. OTC [Arzneimittel, die ohne ärztliche
Verschreibung erworben werden können], Alternativmedizin, Hygiene, Pflege und Schönheit);
- hospINDEX
richtet sich an Spitäler und enthielt rund 180'000 Artikel, die auf die Bedürfnisse der Spitäler
ausgerichtet sind;
- medINDEX
richtet sich an Ärztinnen und Ärzte und umfasste 100'000 Artikel (insb. Arzneimittel, Medizinprodukte,
Verbrauchsmaterial, Praxis- und Laborbedarf);
- pharmINDEX
richtet sich an Apotheken und umfasste rund 180'000 Artikel (insb. Arzneimittel, Phytotherapie, Nahrungsergänzung,
Hygiene, Pflege und Schönheit);
- insureINDEX
richtet sich an Kostenträger wie Kranken- und Unfallversicherer sowie Dienstleistungsunternehmen
aus diesem Bereich. Über insureINDEX sind insbesondere abrechnungsrelevante Informationen und Limitationen
verfügbar.
- logINDEX
richtet sich an Grossisten und umfasste rund 180'000 Artikel (insb. Arzneimittel, Phytotherapie, Nahrungsergänzung,
Hygiene, Pflege und Schönheit).
D.b.b Unterdessen
wird neben diesen sieben Datenangeboten zusätzlich webINDEX angeboten, welches Stammdaten für
Online-Shops enthält. Zudem hat in allen Datenangeboten die Anzahl der enthaltenen Artikel nochmals
deutlich zugenommen (https://www.hcisolutions.ch/de/medication-solutions/index-datenbanken.php [abgerufen
am 06.12.2021]).
D.b.c Die
INDEX-Datenbanken lösten 2012 das Vorgängerprodukt Galdat ab. Galdat wurde 1993 eingeführt
und war zunächst für Arztpraxen verfügbar, später wurde Galdat auch in Spitälern,
bei Krankenkassen oder in Heimen verwendet. Die Ablösung von Galdat erfolgte gemäss HCI hauptsächlich
aufgrund des technischen Wandels bzw. weil Galdat keine Individualisierungen nach den Bedürfnissen
der Zielgruppen zuliess.
D.b.d Gemäss
Angaben der Beschwerdeführerinnen hat HCI die INDEX-Datenbankstruktur neu entwickelt. Die INDEX-Produkte
würden aus zahlreichen verschiedenen Schemata bestehen und sich auf umfassende wissenschaftliche
und kommerzielle Informationen zu Artikeln und Produkten des Gesundheitswesens beziehen. Die XML-Schemata
seien untereinander durch Referenzen verknüpfbar. Die INDEX-Datenbanken würden auf www.compendium.ch
aufbauen. Die Aufbereitung der Arzneimittelinformationen für die INDEX-Datenbanken sei ein arbeitsintensiver
Prozess, der zur Gewährleistung der Patientensicherheit durch Fachpersonen ausgeführt werde.
Pro Produkt seien [...] Felder hinterlegt, womit sich der Informationsgehalt der INDEX-Datenbanken
seit 2007 [...] habe. Gemäss Schätzungen betrage der durchschnittliche Aufwand für
die Aufbereitung eines neuen Präparates in das maschinenlesbare Datenformat ca. [...] Stunden.
Durch die Abklärung mittels INDEX-Produkte würden eine Reduktion des ärztlichen Zeitaufwands
sowie tiefere Kosten im Gesundheitswesen herbeigeführt werden.
D.b.e Die
Beschwerdeführerinnen wiesen wiederholt auf die hohe Qualität ihrer Datenbanken sowie die Wichtigkeit
der Vollständigkeit dieser Datenbanken hin. So führten sie aus, dass die Qualität nicht
nur vom Umfang der Daten abhängig sei, sondern auch von der anwender- bzw. marktspezifischen Passgenauigkeit
in die Prozesse von Logistik, Abrechnung und Medikation sowie von der Art und Weise, wie die Daten aufbereitet
werden. HCI verfüge über eine eigene Fachredaktion mit [...] Fachpersonen (Ärzte,
Apotheker, IT-Spezialisten, Pharmaassistentinnen, etc.), welche die Fach- und Patienteninformationen
überprüfen und mit weiteren Informationen anreichern würden. Die in den Datenbanken von
HCI enthaltenen Informationen seien in den auf AIPS publizierten Fachinformationen überhaupt nicht,
nicht vollständig und/oder nur in variabler Prosaform enthalten, so beispielsweise Angaben zu Hilfsstoffen,
Maximaldosierungen, Angaben zur Anwendung bei Nieren- oder Leberinsuffienz, Angaben zur Anwendung bei
Schwangerschaft/Stillzeit, Kinderdosierungen sowie Angaben zu Kontraindikationen und Allergien. Weiter
würden die INDEX-Datenbanken wirtschaftliche und vertriebsbezogene Informationen enthalten.
D.c Datenbanken
anderer Anbieter
D.c.a Die
dr-ouwerkerk ag - just-medical! (nachfolgend: ouwerkerk) bietet gemäss eigenen Angaben seit 2000
eine Informationsplattform bzw. verschiedene Informationen wie Fortbildungskalender, Stellenangebote,
Patientenfälle und Medikamenteninformationen für Ärzte, Apotheker und für Pharma-
oder Medizinische Professionals an. Ab 2012 bot ouwerkerk mit med-drugs zudem Stammdaten von Medikamenteninformationen
als Dat-File und XML-File an. Dieses Angebot wurde durch einzelne Zulassungsinhaberinnen mitfinanziert.
Die Medikamenteninformationen wurden von ywesee geliefert. Die Daten stammten aus öffentlich verfügbaren
Datenbanken (AIPS, Refdata, Swissmedic, BAG) und wurden anschliessend "entsprechend zusammengesetzt".
Gemäss den Angaben von ouwerkerk konnte trotz intensiven Akquise-Tätigkeiten bei Softwarehäusern,
Spitälern und Apothekenketten kein Kunde für das Produkt gefunden werden. A._______ von ouwerkerk
gab am 7. November 2016 an, sich deshalb 2014 entschieden zu haben, in diesem Bereich nicht mehr aktiv
sein.
D.c.b Ywesee
bot im Bereich elektronische Medikamenteninformationen in Zusammenarbeit mit der B. _______ und C. _______
MEDIupdate XML an. Weiter betrieb ywesee online Datenbanken, namentlich ch.oddb.org sowie die Plattform
AMIKO, welche als iOS-App für I-Pad und I-Phone, Android-App,
Windows-App und als Web-Applikation programmiert wurde. MEDIupdate XML lieferte Daten für [...]
Medikamente und zu [...] von der Krankenkasse bezahlten Non-Pharma Artikeln. Gemäss Angaben
von ywesee wurde MEDIupdate XML von mindestens [...] Ärztinnen
und Ärzten verwendet und enthielt nicht nur die Fachinformationen, sondern auch weitere Daten stammend
von Refdata, Swissmedic, BAG, etc. Die kostenlose Amiko-App sei von mindestens [...] Usern benutzt
worden. Ywesee wurde gemäss eigenen Angaben bei Amiko durch eine Pharmafirma finanziell unterstützt.
E. Vertragsgestaltung
und Geschehensablauf
E.a betreffend
Zulassungsinhaberinnen
E.a.a Bis
2012 schlossen die Zulassungsinhaberinnen mit Documed einen Vertrag für die Aufnahme und Publikation
der Fach- und Patienteninformationen in das Compendium ab (zur Publikationspflicht s. oben E. C.a).
Die Aufnahme in die Datenbank Galdat bzw. ab 2012 in die INDEX-Datenbank von e-mediat erfolgte für
die Zulassungsinhaberinnen bis dahin ohne vertragliche Regelung und ohne ein spezifisches Entgelt.
E.a.b Mit
einem Schreiben vom Januar 2012 wies Documed die Zulassungsinhaberinnen darauf hin, dass Swissmedic die
regulatorische Publikationspflicht 2011 aufgehoben habe, die Zulassungsinhaberinnen die Publikation der
Fach- und Patienteninformationen aber dennoch "auf geeignete
Weise" sicherzustellen hätten. Weiter kündigte
Documed an, ab 1. April 2012 nur noch diejenigen Produkte aktuell und umfassend in den elektronischen
Medien und INDEX-Produkten zu dokumentieren, für die ein Auftrag vorliege. Dies wurde in der
Folge jedoch nicht umgesetzt.
E.a.c Am
20. und 27. September 2012 informierten Documed und e-mediat an einer Informationsveranstaltung über
ihr neues kostenpflichtiges Angebot. Viele Zulassungsinhaberinnen erhielten daraufhin eine Offerte inkl.
Leistungskatalog und Preisliste für das Jahr 2013 und die folgenden Jahre. Es handelte sich um ein
Angebot von Documed und e-mediat, formal betrachtet blieb weiterhin Documed Vertragspartnerin.
E.a.d Gemäss
den neuen "Vereinbarung[en] zur Publikation von Informationen im Arzneimittel-Kompendium der Schweiz®
und in den INDEX-Produkten" war Vertragsgegenstand die Geschäftsbeziehung zwischen Documed
und den Zulassungsinhaberinnen für die Aufträge zur Publikation von Informationen im Arzneimittel-Kompendium
und weiteren Diensten. Die Leistungen beinhalteten gemäss der Vereinbarung "Publikations-,
Distributions- sowie Serviceleistungen", wobei für die detaillierte Beschreibung auf den Leistungskatalog
verwiesen wurde.
E.a.e Im
Leistungskatalog wurden zunächst die Basisdienstleistungen der Module D1 und E1 aufgeführt,
welche insbesondere redaktionelle und technische Qualitätssicherungs- und Aufbereitungsarbeiten
enthielten sowie das Auftragsmanagement via "compendiumPORTAL2". Danach wurden die einzelnen
Module genannt. Das Basismodul D1 beinhaltete die Publikation der Fach- und Patienteninformationen auf
www.compendium.ch und in der entsprechenden App für iPhone und iPad sowie im E-Book. Das Basismodul
E1 beinhaltete im Wesentlichen Dienstleistungen rund um die INDEX-Produkte sowie Clinical Decision Support
(CDS) bei Rx-Produkten (verschreibungspflichtige Arzneimittel). Weiter finden sich im Leistungskatalog
die optionalen Module D2, D3 und E2. Das Modul D3 beinhaltete insbesondere redaktionelle Textbearbeitungen
und Übersetzungen. In der Preisliste wurde sodann explizit erwähnt, dass "die Module D
und E unabhängig von einander buchbar [sind]".
E.a.f 
Der
Upload auf AIPS war gemäss Leistungskatalog nicht in den Modulen enthalten. In der "Vereinbarung
zur Publikation von Informationen im Arzneimittel-Kompendium der Schweiz® und in den INDEX-Produkten"
wurde jedoch unter Ziffer 2 (Leistungen) erwähnt, dass Documed bei entsprechender Beauftragung durch
den Kunden auch die Publikation der Kundentexte in AIPS gemäss den Swissmedic-Anforderungen vornehme.
Hierzu wurde ein entsprechendes Auftragsformular beigelegt (Beilage 4). Für diese Dienstleistung
wurde den Zulassungsinhaberinnen kein zusätzliches Entgelt verrechnet.
E.a.g Die
Leistungen des Moduls D1 wurden nach Anzahl Fachinformationen und die Leistungen des Moduls E1 nach Anzahl
Artikel bzw. Pharmacode verrechnet. Auf eine Differenzierung zwischen veränderten und unveränderten
bzw. umfangreichen und kurzen Inhalten wurde verzichtet. Eine Preisdifferenzierung erfolgte jedoch nach
Art des Arzneimittels (Rx-P [verschreibungspflichtige und patentgeschützte Arzneimittel], Rx [verschreibungspflichtige
Arzneimittel ohne Patentschutz/Generika] und OTC [nicht verschreibungspflichtige Arzneimittel]. Bei beiden
Modulen wurde für Mehrjahresverträge ein Rabatt gewährt, [...] bei einem Zweijahresvertrag
und [...] bei einem Vierjahresvertrag. Später wurde entschieden, den Zulassungsinhaberinnen
eine jährliche Kündigungsmöglichkeit zu gewähren und allen Zulassungsinhaberinnen
rückwirkend per 1. Januar 2013 diejenigen Konditionen (Rabatte) zu gewähren, welche für
Vierjahresverträge galten. Zusätzlich wurde beim Modul E1 ab einer Anzahl von [...] Artikeln
bzw. Pharmacodes ein Staffelrabatt gewährt und bei einem ex factory Umsatz von weniger als Fr. [...]
pro Artikel in einem Kalenderjahr galten reduzierte Tarife.
E.a.h Mit
Schreiben vom 11. Dezember 2012 wies Documed jene Zulassungsinhaberinnen, welche die Offerte (noch) nicht
unterzeichnet hatten, auf die Vorteile ihrer Produkte hin und erklärte sich bereit, die Arzneimittelinformationen
in den nächsten Monaten weiterhin vollständig bereitzustellen. Die Neuaufnahme von Arzneimittelinformationen
von Zulassungsinhaberinnen ohne Rahmenvertrag E1 war bis im September 2013 mittels Einzelvereinbarungen
möglich. E-mediat verpflichtete sich dabei, die Neuaufnahme bzw. Mutation kostenlos in die INDEX-Datenbanken
aufzunehmen bzw. zu ändern. Gleichzeitig wies Documed darauf hin, dass die Aufnahme bzw. Mutation
der Daten länger dauern könne als bei Firmen, welche mit e-mediat und/oder Documed einen Vertrag
abgeschlossen hätten, sowie dass bei einem späteren Vertragsabschluss die Leistung nachträglich
verrechnet werde.
E.a.i Ab
1. Mai 2013 verwendeten Documed und e-mediat in den INDEX-Datenbanken und im Compendium das sogenannte
[QAP?]-Label. Die Leistungserbringerinnen und -erbringer wurden im März und April 2013 darüber
informiert. Mit dem [QAP?]-Label kennzeichneten Documed und e-mediat Arzneimittel von Zulassungsinhaberinnen
ohne Vertrag, welche geänderte Fach- und/oder Patienteninformationen auf AIPS aufgeschaltet hatten,
bis die Anpassungen in der Datenbanken von Documed und e-mediat erfolgten. Dadurch sollte erkennbar sein,
welche Informationen von Documed und e-mediat qualitätsgesichert sind. Infolge der Intervention
von Swissmedic wurde die Kennzeichnung [QAP?] ab dem 15. August 2013 mit der Kennzeichnung [!] ersetzt.
Ab dem 1. Oktober 2013 wurde die Praxis mit den Einzelvereinbarungen eingestellt. Neuaufnahmen und Änderungen
bei Arzneimitteln von Nicht-Vertragspartnern wurden in die INDEX-Datenbanken übernommen, wenn ein
entsprechendes Bedürfnis seitens der Leistungserbringerinnen und Leistungserbringer bestand.
E.a.j Für
das Jahr 2016 veränderten sich das Angebot und die Tarife für die obenerwähnten Dienstleistungen
leicht, während der Vertragsgegenstand, nämlich die Aufnahme der Medikamenteninformationen
in die Datenbanken und der anschliessende Vertrieb der Daten, unverändert blieb. Neu wurde der Upload
und die Sicherstellung der fristgerechten Publikation auf AIPS explizit als Bestandteil des Moduls D
geführt. Das Modul D beinhaltete zudem insbesondere "Redaktionelle Qualitätssicherung,
Plausibilitätsprüfungen, inhaltlicher Sprachenvergleich der wichtigsten Kapitel". Das
Modul E betraf die "Strukturierung und Integration in INDEX-Datenbanken, pharmaVISTA und vitaVISTA".
Daneben bot HCI weitere Zusatzleistungen an, die teilweise im Modul E ohne Zusatzkosten inbegriffen waren
(vitaVISTA Konsumenten-Applikation; Identa) und teilweise separat verrechnet wurden. Eine Zusatzleistung,
die separat verrechnet wurde, war "Lektorat / Übersetzungen / compendium-Fachinformationen".
E.a.k Mit
Schreiben vom 4. April 2016 informierte die Beschwerdeführerin 2 das Sekretariat der WEKO (nachfolgend:
Sekretariat) über die Einführung eines neuen Preismodells ab 2017. Dieses gestalte sich für
die Zulassungsinhaberinnen stärker aufwandorientiert, so dass für sie im Zeitpunkt der Markteinführung
eines Produktes höhere Kosten anfallen würden, die Kosten für die Pflege und Verteilung
der Daten unveränderter Produkte hingegen reduziert würden. Ebenfalls würden im neuen
Preismodell Eigenleistungen der Zulassungsinhaberinnen mit Rabatten "belohnt" werden. Generell
umfasse die Dienstleistung unter anderem die Publikation der Daten auf B2B- und B2C-lnformationsplattformen
und die Verteilung via INDEX-Produkte sowie die Qualitätssicherung der Daten. Fach- und Patienteninformationen
würden ohne speziellen Auftrag inhaltlich nicht geprüft werden. Daneben bot HCI gemäss
dem neuen Preismodell 2017 ergänzende Dienstleistungen an. Darunter fielen insbesondere redaktionelle
Dienstleistungen wie "Lektorat und Übersetzungen von Fach- bzw. Patienteninformationen"
und die "Qualitätssicherung der Fachinformationen (Textdurchsicht, Sprachenvergleich und Plausibilitätskontrolle)".
Die bisherigen Module D und E finden sich im neuen Preismodell nicht mehr.
E.a.l Mit
Eingabe vom 16. November 2018 legten die Beschwerdeführerinnen zudem dar, seit dem 1. Januar 2017
neben der Qualitätssicherung auch den Upload auf AIPS als "separate" Dienstleistung anzubieten.
Der Upload auf AIPS koste Fr. 30.- pro Aufschaltung der Fach- bzw. Patienteninformation.
E.b betreffend
Softwarehäuser
E.b.a HCI
(früher e-mediat) schliesst mit den Softwarehäusern für den Vertrieb der INDEX-Datenprodukte
Lizenzverträge ab. Danach erteilt HCI (früher e-mediat) dem Softwarehaus im Rahmen einer einfachen
Lizenz eine Zugriffsberechtigung zur Integration der Stammdaten in ihre Software-Programme zur Nutzung
(durch die gemeinsamen Kunden) im Rahmen eines von HCI lizenzierten Dienstleistungspakets. In den meisten
Fällen schliesst HCI mit den Leistungserbringerinnen und -erbringern direkte Vereinbarungen ab,
worin sie sich verpflichtet die Daten via Softwarehäuser zu liefern. Beim Datenprodukt medINDEX
für Ärztinnen und Ärzte werden die Daten aber direkt von den Softwarehäusern vertrieben.
Deshalb besteht mit einzelnen Softwarehäuser zusätzlich
ein Lizenzvertrag über den Vertrieb von Dienstleistungspaketen an Endkunden.
E.b.b Gemäss
den Angaben von Documed und e-mediat erfolgte 2012 eine prozessintegrierte Verteilung der veredelten
Medikamentendaten an über 115 Systemanbieter. Aus dem Dokument "Dienstleistungen und Tarife
2016" der HCI lässt sich entnehmen, dass 164 Systemanbieter mit den Arzneimittelinformationen
via HCI arbeiteten.
E.b.c Das
Sekretariat hat im Laufe der Untersuchung an gewisse Softwarehäuser ein Auskunftsbegehren gesandt.
Zudem wurde HCI am 29. November 2016 aufgefordert, sämtliche Verträge mit Softwarehäusern
sowie die Bestimmungen, die Ende 2012 in Kraft waren, einzureichen. Auch wurden die Verträge, die
nach diesem Datum geändert oder neu abgeschlossen wurden, verlangt. HCI hat daraufhin dem Sekretariat
176 Verträge mit Softwarehäusern aus der Zeit von 2007 bis 2016 eingereicht.
E.b.d Ein
Vertrag zwischen e-mediat und einem Softwarehaus D._______, welcher als Vertragsprodukte die Applikationen
und Datenbanken medINDEX Basic und CIS-Daten Produkte umfasst und sowohl die Integration der Daten in
die Software von D._______ als auch den Vertrieb der Daten beinhaltet, enthält folgende Klausel
(sogenannte Vertragsklausel A):
"Soweit es [...] zur Herstellung oder Weiterentwicklung
von Vertragsprodukten als sinnvoll erachtet, den Produktanwendern zusätzlich den Zugriff auf für
sie nützliche Partner- und Produkte-Stamm-Daten (d.h. auf andere als auf HOSPINDEX- und CIS-Daten)
zu ermöglichen, ist sie verpflichtet, dieselben bei e-mediat zu beschaffen. Soweit e-mediat zu deren
Bereitstellung nicht bereit oder dazu nicht innert einer der Problemstellung angemessenen nützlichen
Frist in der Lage ist, ist [...] berechtigt, diese Komponenten anderweitig zu beziehen."
E.b.e Dieser
Vertrag wurde am 16. bzw. 26. Februar 2006 von den Vertragsparteien unterzeichnet. In der Zusatzvereinbarung
vom 6. bzw. 13. September 2012 wurde zudem vereinbart, dass die D._______ an Arztpraxen
keine weiteren Medikamentendaten vertreibe ausser medINDEX.
E.b.f Eine
weitgehende identische Klausel findet sich in einem weiteren Vertrag zwischen e-mediat und einem Softwarehaus,
der von letzterer dem Sekretariat am 23. Juli 2013 mit der Stellungnahme zum Auskunftsbegehren eingereicht
wurde. Dieser Vertrag wurde von den Parteien zwar unterzeichnet, jedoch nicht datiert. HCI hat am 29.
November 2016 einen neuen Vertrag mit diesem Softwarehaus eingereicht, datiert auf [...], mit Bezugnahme
auf den alten Vertrag, wobei angegeben wird, dass dieser vom [...] datiere. Der neue Vertrag enthält
die oben erwähnte Klausel nicht.
E.b.g 83
Verträge zwischen e-mediat und Softwarehäusern enthalten folgende Klausel (sogenannte
Vertragsklausel B), wobei 75 dieser Verträge aus den Jahren 2012 bis 2014 stammen:
"Ohne vorgängige schriftliche Zustimmung von e-mediat ist
das SWH [Softwarehaus] nicht berechtigt, Daten Dritter in die XML-Strukturen von e-mediat zu implementieren
und/oder Daten in seine SW-Programme einzuspeisen, die nicht von e-mediat stammen und die gleich oder
im Wesentlichen gleich wie Daten von e-mediat strukturiert sind."
E.b.h Gemäss
den Beschwerdeführerinnen soll die Ratio hinter den beiden oben zitierten Vertragsklauseln gewesen
sein, dass die Softwarehäuser pro Softwarekunde bzw. Leistungserbringer keine Vermischung oder Veränderung
der von HCI gelieferten Daten vornehmen dürfen. Hintergrund hierfür sei das Interesse von HCI
gewesen, ihren guten Ruf als Anbieterin von Datenbanken hoher Qualität gegenüber den Leistungserbringerinnen
und Leistungserbringer zu wahren, Haftungsrisiken zu minimieren und die Patientensicherheit zu schützen.
Weiter hätten die Vertragsklauseln auch zur Verhinderung von Leistungsstörungen in den Lizenzverträgen
zwischen HCI und den Leistungserbringerinnen und -erbringer gedient. Schliesslich hätten sie sichergestellt,
dass keine Verletzungen des Bundesgesetzes gegen den unlauteren Wettbewerb vom 19. Dezember 1986 (UWG,
SR 241) durch Anbieter von Drittdaten vorkommen könnten, indem die Datenbankstruktur von HCI
einfach übernommen werde.
241) durch Anbieter von Drittdaten vorkommen könnten, indem die Datenbankstruktur von HCI
einfach übernommen werde.
E.b.i Die
Beschwerdeführerinnen gaben weiter an, nie eine Anfrage um Erlaubnis für die Zusammenarbeit
mit einer Drittfirma verweigert zu haben. So habe HCI beispielsweise E._______ eine Zusammenarbeit mit
ywesee erlaubt und weiterhin mit E._______ zusammengearbeitet. Letztlich habe E._______ die Daten der
ywesee zwar nicht eingesetzt. Der Grund hierfür habe darin gelegen, dass die Daten der ywesee wegen
der schlechteren Qualität nicht verkäuflich gewesen seien. Zudem hätten [...] Softwarehäuser
neben dem Vertrag mit HCI auch einen Vertrag mit F._______, welche die Datenbank [...] anbiete. Diese
Datenbank enthalte Informationen zur sicheren Handhabung der Medikamentenabgabe, insbesondere Warn- und
Abgabehinweise, die teilweise in Konkurrenz und teilweise in Ergänzung zu den Daten der HCI stünden.
E.b.j Ab
2015 hat HCI in den Verträgen mit den Softwarehäusern folgende neue Formulierung verwendet,
die in 21 (von 23) Verträgen zu finden ist, die seit 2015 abgeschlossen wurden:
"Kundenindividuelle Daten oder Daten von Dritten dürfen
in der Softwarelösung zu den bestehenden INDEX-Daten hinzugefügt werden, sofern deren Datenquelle
klar ersichtlich ist. Die Datenquelle sowie jegliche Veränderung muss für den Kunden sichtbar
angezeigt werden."
E.b.k In
Ihrer Eingabe vom 16. November 2018 legen die Beschwerdeführerinnen schliesslich dar, HCI habe im
April 2017 die Softwarehäuser angeschrieben und darüber informiert, "dass sie nicht mehr
an den Zustimmungsvorbehalt gemäss der Klausel B gebunden seien".
F. Verfügung
der WEKO vom 7. Juli 2008 i.S. Publikation von Arzneimittelinformationen
F.a Mit
Verfügung vom 7. Juli 2008 i.S. Publikation von Arzneimittelinformationen
(RPW 2008/3 S. 385 ff.) stellte die Vorinstanz fest, dass Documed auf dem Markt für die Publikation
von Fachinformationen gedruckt und online in einem vollständigen Werk eine marktbeherrschende Stellung
hat und dass Documed durch Diskriminierung von Handelspartnern gemäss Art. 7 Abs. 1 i.V.m.
Art. 7 Abs. 2 Bst. b
i.V.m.
Art. 7 Abs. 2 Bst. b KG ihre Stellung missbraucht hat. Zu diesem Zeitpunkt bestanden noch die unter E.
C.a.d
f. beschriebenen regulatorischen Rahmenbedingungen, die zu einer faktischen Pflicht der Zulassungsinhaberinnen
zum Abschluss eines solchen Vertrages führten.
KG ihre Stellung missbraucht hat. Zu diesem Zeitpunkt bestanden noch die unter E.
C.a.d
f. beschriebenen regulatorischen Rahmenbedingungen, die zu einer faktischen Pflicht der Zulassungsinhaberinnen
zum Abschluss eines solchen Vertrages führten.
F.b Die
gerügte Preisdiskriminierung bestand gemäss WEKO einerseits darin, dass Documed es den grösseren
Pharmaunternehmen ermöglichte, die Preise zu vereinbaren und dadurch die kleineren Unternehmen diskriminierte.
Andererseits habe Documed keine preisliche Unterscheidung gemacht bei zu publizierenden Texten, die gegenüber
dem Vorjahr unverändert blieben. Damit seien Unternehmen, deren Texte unverändert zu übernehmen
waren, gegenüber Unternehmen, deren Texte noch durch Documed zu korrigieren waren, diskriminiert
worden. Mit den vereinbarten einvernehmlichen Regelungen wurden diese Diskriminierungen beseitigt.
F.c Die
anderen in diesem Verfahren untersuchten Vorwürfe liessen sich nicht bestätigen. Insbesondere
wurde festgestellt, dass keine unzulässige Koppelung i.S.v. Art. 7 Abs. 1 i.V.m. Abs. 2 Bst. f KG
zwischen Publikationsdienstleistungen und Korrekturarbeiten bestehe. Die WEKO erwog, dass die Korrekturkosten
im Vergleich zu den anderen Standardprozessen vernachlässigbar tief seien. Eine Differenzierung
zwischen Standard- und Korrekturkosten sowie deren gesonderte Inrechnungstellung sei nicht angezeigt,
da es wahrscheinlich sei, dass dies insgesamt zu höheren Kosten führen würde.
i.V.m. Abs. 2 Bst. f KG
zwischen Publikationsdienstleistungen und Korrekturarbeiten bestehe. Die WEKO erwog, dass die Korrekturkosten
im Vergleich zu den anderen Standardprozessen vernachlässigbar tief seien. Eine Differenzierung
zwischen Standard- und Korrekturkosten sowie deren gesonderte Inrechnungstellung sei nicht angezeigt,
da es wahrscheinlich sei, dass dies insgesamt zu höheren Kosten führen würde.
F.d Documed
wurde gestützt auf Art. 49a Abs. 1 KG mit einer Verwaltungssanktion in der Höhe von Fr. 50'000.-
sanktioniert.
KG mit einer Verwaltungssanktion in der Höhe von Fr. 50'000.-
sanktioniert.
G. Vorinstanzliches
Verfahren
G.a Vorabklärung
G.a.a Am
7. September 2010 eröffnete das Sekretariat eine Vorabklärung gemäss Art. 26 KG in Sachen
Medikamentenvertrieb. Im Rahmen dieser Vorabklärung wurde das Sekretariat auf mögliche Verstösse
gegen das Kartellgesetz im Bereich der Kommerzialisierung von elektronischen Medikamenteninformationen
aufmerksam gemacht.
KG in Sachen
Medikamentenvertrieb. Im Rahmen dieser Vorabklärung wurde das Sekretariat auf mögliche Verstösse
gegen das Kartellgesetz im Bereich der Kommerzialisierung von elektronischen Medikamenteninformationen
aufmerksam gemacht.
G.a.b Im
Laufe der Voruntersuchung sandte das Sekretariat der e-mediat ein Auskunftsbegehren betreffend Wettbewerbsverhältnisse
im Bereich der Verarbeitung und des Vertriebs von Medikamentendaten zu. Documed wurde aufgefordert, sich
zu einem allfälligen Verstoss gegen die einvernehmliche Regelung vom 7. Juli 2008 (s. oben E. F)
zu äussern. Zudem haben mehrere Unternehmen Informationen zum Verhalten von e-mediat, zu den allgemeinen
Strukturen und der Funktionsweise des Marktes sowie von AIPS geliefert. Auch Documed und e-mediat haben
sich im Rahmen der Vorabklärung mehrmals geäussert und Informationen geliefert, insbesondere
zur künftigen Vertragsgestaltung mit den Zulassungsinhaberinnen.
G.a.c Am
11. Oktober 2012 reichte ywesee beim Sekretariat eine Anzeige ein und beantragte die Eröffnung eines
formellen Verfahrens sowie den Erlass von vorsorglichen Massnahmen gegen Documed und e-mediat. Dem Gesuch
betreffend Erlass von vorsorglichen Massnahmen wurde aufgrund fehlender Dringlichkeit nicht stattgegeben.
G.b Untersuchung
G.b.a
Eröffnung
der Untersuchung
G.b.a.a Am
6. Dezember 2012 eröffnete das Sekretariat im Einverständnis mit einem Mitglied des Präsidiums
gegen Galenica, HCI, Documed und e-mediat eine Untersuchung gemäss Art.
27 KG in Sachen Kommerzialisierung von elektronischen Medikamenteninformationen.
KG in Sachen Kommerzialisierung von elektronischen Medikamenteninformationen.
G.b.a.b Das
Sekretariat hielt fest, es sei auf Anhaltspunkte für möglicherweise unzulässige Wettbewerbsbeschränkungen
im Bereich der Verarbeitung und des Vertriebs von elektronischen Medikamenteninformationen gestossen.
Mit der Untersuchung solle geprüft werden, ob es e-mediat und Documed aufgrund ihrer Marktstellung
möglich sei, die Pharmahersteller zur Neuaufnahme und Unterhaltung von Geschäftsbeziehungen
betreffend die Aufnahme deren elektronischen Medikamenteninformationen in die Datensammlungen der e-mediat
zu bewegen. Dies indem sie den Pharmaherstellern in Aussicht stellten, frei verfügbare Medikamenteninformationen
nicht direkt aus öffentlich zugänglichen Quellen, sondern nur bei Abschluss eines entsprechenden
Vertrages in die eigenen Datensammlungen zu übernehmen. Zudem würden einzelne Vertragsbestimmungen
auf ihre Kartellrechtskonformität überprüft werden; namentlich die Verpflichtung derjenigen
Zulassungsinhaberinnen, welche einen Vertrag betreffend Aufnahme elektronischer Medikamenteninformationen
in die Datensammlungen von e-mediat abschliessen, einen solchen für die Medikamenteninformationen
all ihrer Produkte abzuschliessen sowie die fehlende Wahlmöglichkeit der Zulassungsinhaberinnen,
in welchen Datensammlungen der e-mediat sie mit ihren Medikamenteninformationen vertreten sein möchten.
Schliesslich würden auch das Verhalten in Zusammenhang mit dem Ausschreibungsverfahren der Swissmedic
betreffend Betrieb und Verwaltung von AIPS sowie die vertikalen Beziehungen zwischen e-mediat und Documed
und den Softwarehäusern von Relevanz sein (vgl. Vorinstanz, act. 107 sowie amtliche Publikation
der Untersuchungseröffnung im Schweizerischen Handelsamtsblatt [SHAB] vom 28. Dezember 2012, Nr.
252, 27 f. sowie im Bundesblatt vom 28. Dezember 2012 [BBl 2012 9833 f.]).
G.b.b
Untersuchungshandlungen
G.b.b.a Am
20. Dezember 2012 fand ein Gespräch zwischen dem Sekretariat und der Beschwerdeführerin 2 und
am 20. Februar 2013 die Parteiverhöre von G._______ ([...] von Documed) und H._______ ([...]
von HCI) statt. In der Folge sandte das Sekretariat einen Fragebogen an Swissmedic zum Thema Entstehung,
Ausschreibung und Funktionsweise von AIPS sowie an alle Zulassungsinhaberinnern der Schweiz ein Auskunftsbegehren,
das Fragen zur Publikation von Arzneimittelinformationen und zur Kommerzialisierung von elektronischen
Medikamenteninformationen enthielt.
G.b.b.b Am
27. Mai 2013 führte das Sekretariat ein Gespräch mit Swissmedic zur Thematik AIPS und am 26.
Juni 2013 stellte es den Beschwerdeführerinnen ein Auskunftsbegehren zur Tarif- und Rabattgestaltung
der Module D1 und E1 sowie zur Anzahl und Umsatz der Verträge je Modul zu. Im weiteren Verlauf der
Untersuchung versandte das Sekretariat an ausgewählte Softwarehäuser einen Fragebogen, der
Fragen zur Beziehung zu e-mediat, zu den Preisen und Kosten der INDEX-Produkte sowie zu Alternativen
zu den INDEX-Produkten beinhaltete.
G.b.b.c Am
4. Juli 2013 fand ein Gespräch zwischen der Stiftung Refdata und dem Sekretariat statt. Darauffolgend
richtete das Sekretariat ein Auskunftsbegehren zum Ausschreibungsverfahren von AIPS an drei Unternehmen,
welche nebst HCI an der AIPS-Ausschreibung teilgenommen hatten. Sodann wurden zwei Gesellschaften, die
in Deutschland in den Vertrieb von Medikamenteninformationen involviert waren, ein Auskunftsbegehren
betreffend Markt- und Vertriebsstrukturen von elektronischen Medikamenteninformationen in Deutschland
zugestellt.
G.b.b.d Am
13. November 2013 fand ein weiteres Treffen zwischen dem Sekretariat und der Beschwerdeführerin
2 statt. Am 10. Februar 2014 reichten die Beschwerdeführerinnen einen Verfahrensantrag auf Befragung
der Leistungserbringerinnen und -erbringer mit einem Fragekatalog zu verschiedenen Themen ein. Der Antrag
wurde aufgeschoben und letztlich mit der hier angefochtenen Verfügung abgewiesen.
G.b.b.e Am
20. Februar 2014 wurde betreffend die Teilnahme von HCI an der AIPS-Ausschreibung I._______, ehemaliger
[...] von HCI, als Zeuge einvernommen. Sodann wurden HCI, Documed und e-mediat aufgefordert, sämtliche
Bilanzen und Erfolgsrechnungen von 2009 bis 2013 einzureichen.
G.b.b.f Am
2. Juli 2014 fand ein Gespräch zwischen dem Sekretariat und einem Softwarehaus statt. Später
holte das Sekretariat bei Swissmedic und beim Bundesamt für Gesundheit (BAG) Informationen über
die laufende Revision des Heilmittelgesetzes ein.
G.b.b.g Ab
Frühjahr 2014 führten das Sekretariat und HCI, Documed und e-mediat Gespräche über
die Möglichkeit einer einvernehmlichen Regelung. Am 27. Oktober 2014 wurden die Rahmenbedingungen
für die Verhandlungen über eine einvernehmliche Regelung unterschrieben und die Verhandlungen
aufgenommen. Mit Schreiben vom 10. Juli 2015 teilte das Sekretariat mit, dass keine Einigung erzielt
werden konnte und die Verhandlungen abgebrochen werden.
G.b.b.h Daraufhin
reichten HCI, Documed und e-mediat am 10. August 2015 ein Ausstandgesuch gegen die zuständigen Sekretariatsmitarbeitenden
ein und machten im Wesentlichen geltend, diese hätten im Rahmen der Verhandlungen über eine
einvernehmliche Regelung Aussagen gemacht, die den Anschein der Befangenheit erweckt hätten, womit
der Verfahrensausgang vorherbestimmt sei. Der Präsident der Vorinstanz wies das Ausstandsgesuch
ab. Die gegen diese Zwischenverfügung beim Bundesverwaltungsgericht erhobene Beschwerde wurde mit
Urteil vom 12. Februar 2016 abgewiesen (Urteil des BVGer B-6830/2015 vom 12. Februar 2016).
G.b.b.i Am
10. November 2015 forderte das Sekretariat HCI, Documed und e-mediat auf, die Bilanzen und Erfolgsrechnungen
des Jahres 2014 einzureichen. Die Beschwerdeführerin 2 beantragte am 28. Januar 2016 und 9.
Mai 2016 die Einstellung der Untersuchung. Zur Begründung verwies sie im Wesentlichen auf die Revision
des Heilmittelgesetzes.
G.b.b.j Während
des Verfahrens äusserten sich die Parteien mehrmals von sich aus und reichten Unterlagen ein, unter
anderem die Studie "Grundlagenanalyse Stammdaten" und weitere Informationen über die Entwicklungen
auf dem Markt.
G.b.b.k Das
Sekretariat gewährte den Beschwerdeführerinnen am 15. Mai 2013, 4. Juni 2013, 17. Februar 2014,
30. April 2014, 16. Juli 2014, 22. Januar 2015, 12. Mai 2016 sowie am 1. Dezember 2016 Akteneinsicht.
G.b.c
Beteiligung
Dritter am Verfahren
G.b.c.a Im
Laufe des Verfahrens beantragten mehrere juristische Personen die Beteiligung am Verfahren (als Partei).
Vips, Vereinigung Pharmafirmen in der Schweiz, und ywesee wurde die Stellung als beteiligte Dritte ohne
Parteistellung i.S.v. Art. 43 Abs. 1 Bst. b KG gewährt. Der Antrag von J._______ auf Parteistellung
wurde abgewiesen. Ebenfalls abgewiesen wurde der Antrag von Swissmedic auf Beteiligung am Verfahren.
Das Sekretariat stellte Swissmedic aber in Aussicht, dass sie sich spätestens im Zeitpunkt von Art.
30 Abs. 2
KG gewährt. Der Antrag von J._______ auf Parteistellung
wurde abgewiesen. Ebenfalls abgewiesen wurde der Antrag von Swissmedic auf Beteiligung am Verfahren.
Das Sekretariat stellte Swissmedic aber in Aussicht, dass sie sich spätestens im Zeitpunkt von Art.
30 Abs. 2 KG zu einem allfälligen sie betreffenden Teil der Ermittlungsergebnisse äussern könne.
KG zu einem allfälligen sie betreffenden Teil der Ermittlungsergebnisse äussern könne.
G.b.c.b Insbesondere
ywesee lieferte im Laufe der Untersuchung wiederholt Informationen zum Markt, zu AIPS und zu Verhaltensweisen
von HCI, Documed und e-mediat. Zudem stellte ywesee verschiedene Verfahrensanträge. Auch von weiteren
Dritten erhielt das Sekretariat freiwillige Informationen, unter anderem vom Verein für die unabhängige
Apotheke (IFAK) die Ankündigung einer Petition zur Aufrechterhaltung des pharmINDEX.
G.c Verfügungsantrag
G.c.a Am
12. Mai 2016 sandte das Sekretariat den Beschwerdeführerinnen den Verfügungsantrag zur Stellungnahme
zu. Gleichzeitig wurden sie aufgefordert die Bilanzen und Erfolgsrechnungen des Jahres 2015 einzureichen.
G.c.b Der
Verfügungsantrag des Sekretariats schlug vor, im Dispositiv festzustellen, dass die Galenica mittels
ihrer Tochtergesellschaft HCI seit dem 1. Januar 2013 auf dem Markt für veredelte, maschinenlesbare
Daten betreffend Medikamenteninformationen sowie auf dem Markt für den Zugang zu elektronischen
Datensätzen betreffend Medikamenteninformationen über eine markbeherrschende Stellung im Sinne
von Art. 4 Abs. 2 KG verfüge. Weiter schlug er vor, die Beschwerdeführerinnen zu verpflichten:
KG verfüge. Weiter schlug er vor, die Beschwerdeführerinnen zu verpflichten:
- die
öffentlich verfügbaren Medikamenteninformationen in ihre an die Leistungserbringer, Vertriebsunternehmen
und Kostenträger bzw. Softwarehäuser vertriebenen Datenbanken ohne Erhebung eines Entgeltes
bei den Zulassungsinhaberinnen aufzunehmen, solange sie auf der Marktseite der Leistungserbringerinnen
und -erbringer, Vertriebsunternehmen und Kostenträger die Preise nicht senke oder es nicht zu einer
Erhöhung der Gesamtkosten für die Plattform komme;
- gegenüber
den Leistungserbringerinnen und -erbringern, Vertriebsunternehmen und Kostenträgern sowie Softwarehäusern
die Medikamenteninformationen und die Daten von Non-Pharma Produkten entbündelt anzubieten, wobei
dieses entbündelte Angebot zu kostenbasierten Preisen zu erfolgen habe;
- den
Zulassungsinhaberinnen die Dienstleistung der Aufnahme der Medikamenteninformationen in die INDEX-Produkte
und andere Dienstleistungen entbündelt sowie die redaktionelle und technische Qualitätskontrolle
und den Upload der Arzneimittelinformationen auf AIPS zu kostenbasierten Preisen anzubieten.
G.c.c Sodann
schlug der Verfügungsantrag vor, den Beschwerdeführerinnen zu untersagen, in ihren Verträgen
mit den Softwarehäusern Vertragsklauseln zu verwenden und durchzusetzen, die eine Alleinbezugspflicht
der Softwarehäuser für zusätzliche Partner- und Produkt-Stamm-Daten bei HCI oder eine
Untersagung der anderweitigen Verwendung der Strukturen der auf der Datenbank der Beschwerdeführerinnen
beruhenden Software für Softwarehäuser vorsehen. Schliesslich schlug der Verfügungsantrag
im Dispositiv eine Sanktionierung der Beschwerdeführerinnen gestützt auf Art. 49a Abs.
1 i.V.m. Art. 7
i.V.m. Art. 7 KG mit einem Betrag von Fr. [...] unter solidarischer Haftung vor.
KG mit einem Betrag von Fr. [...] unter solidarischer Haftung vor.
G.c.d Am
13. Juli 2016 nahmen die Beschwerdeführerinnen fristgerecht zum Verfügungsantrag Stellung.
Sie beantragten, das Untersuchungsverfahren sei einzustellen und es sei festzustellen, dass HCI auf dem
Markt für die Publikation von Patienteninformationen online in einem vollständigen Werk und
auf dem Markt für die Publikation von Fachinformationen gedruckt und online in einem vollständigen
Werk über keine marktbeherrschende Stellung verfüge. Eventualiter sei die Sache zur Durchführung
weiterer Sachverhaltserhebungen, insbesondere zur Durchführung einer Befragung der Leistungserbringerinnen
und -erbringer, an das Sekretariat zurückzuweisen. Subeventualiter wurde der Antrag gestellt, von
der Auferlegung einer Sanktion abzusehen bzw. diese massiv zu reduzieren.
G.c.e Bereits
mit Eingabe vom 20. Juni 2016 hatten die Beschwerdeführerinnen beantragt, auf eine Zustellung des
Antrages an ywesee sei zu verzichten oder ywesee sei unter Androhung der Straffolgen gemäss Art.
292 des Schweizerischen Strafgesetzbuchs vom 21. Dezember 1937 (StGB, SR
des Schweizerischen Strafgesetzbuchs vom 21. Dezember 1937 (StGB, SR 311.0) zu verpflichten,
den Antrag bis zum rechtskräftigen Abschluss des Verfahrens geheim zu halten. Nach Ergänzung
dieses Antrages am 23. Juni 2016 um vips einigten sich das Sekretariat und die Beschwerdeführerinnen
darauf, die Stellungnahme an die beteiligten Dritten ywesee und vips nach Abgabe einer Verpflichtungserklärung,
den Antrag nicht publik zu machen, zuzustellen. Vips verzichtete am 4. Juli 2016 auf die Zustellung des
Antrages. Swissmedic nahm am 7. Juli 2016 zum Antrag Stellung und ywesee reichte ihre Stellungnahme am
13. Juli 2016 ein.
311.0) zu verpflichten,
den Antrag bis zum rechtskräftigen Abschluss des Verfahrens geheim zu halten. Nach Ergänzung
dieses Antrages am 23. Juni 2016 um vips einigten sich das Sekretariat und die Beschwerdeführerinnen
darauf, die Stellungnahme an die beteiligten Dritten ywesee und vips nach Abgabe einer Verpflichtungserklärung,
den Antrag nicht publik zu machen, zuzustellen. Vips verzichtete am 4. Juli 2016 auf die Zustellung des
Antrages. Swissmedic nahm am 7. Juli 2016 zum Antrag Stellung und ywesee reichte ihre Stellungnahme am
13. Juli 2016 ein.
G.c.f Am
6. September 2016 reichten die Beschwerdeführerinnen ein ökonomisches Gutachten nach.
G.c.g Die
Vorinstanz trat am 26. September 2016 auf den Antrag des Sekretariats ein und führte am 24. Oktober
2016 die Parteianhörung durch. Daran nahmen für die Beschwerdeführerinnen zwei Rechtsvertreter
sowie H._______ ([...] der HCI), K._______ ([...] der HCI) und L._______ ([...] von Galenica
Santé) teil. Die Vorinstanz hörte auch ouwerkerk (A._______), ywesee (M._______) und N._______,
[...] von Documed und e-mediat, als Zeugen an.
G.c.h Am
21. November 2016 verlangte die Vorinstanz von der Beschwerdeführerin 2 eine Kopie sämtlicher
Verträge und Bestimmungen zwischen e-mediat und den Softwarehäusern, die Ende 2012 in Kraft
waren. Ebenso wurden die Verträge, die nach diesem Datum geändert haben oder neu abgeschlossen
wurden, verlangt.
G.c.i Schliesslich
reichte HCI ein weiteres ökonomisches Gutachten ein.
G.d Verfügung
G.d.a Am
19. Dezember 2016 erliess die Vorinstanz die angefochtene Verfügung mit folgendem Dispositiv:
"1. Es wird festgestellt, dass die Galenica AG mittels ihrer
Tochtergesellschaft HCI Solutions AG seit dem 01. Januar 2013 auf dem Markt für veredelte, maschinenlesbare
Daten betreffend Medikamenteninformationen sowie auf dem Markt für den Zugang zu elektronischen
Datensätzen betreffend Medikamenteninformationen über eine marktbeherrschende Stellung im Sinne
von Art. 4 Abs. 2 KG verfügt.
KG verfügt.
2. Galenica AG und HCI Solutions AG wird untersagt, in ihren Verträgen
mit den Softwarehäusern Vertragsklauseln zu verwenden und durchzusetzen, die eine Alleinbezugspflicht
der Softwarehäuser für zusätzliche Partner und Produkt-Stamm-Daten bei HCI Solutions AG
oder eine Untersagung der anderweitigen Verwendung der Strukturen der auf der Datenbank der Galenica-Gruppe
beruhenden Software für die Softwarehäuser vorsehen.
3. Galenica AG und HCI Solutions AG werden verpflichtet, den Zulassungsinhaberinnen
die Dienstleistung der Aufnahme der Medikamenteninformationen in die Indices und andere Dienstleistungen
entbündelt anzubieten. Die Galenica AG und ihre Tochtergesellschaft HCI Solutions AG werden verpflichtet,
die redaktionelle und technische Qualitätskontrolle der Arzneimittelinformationen sowie den Upload
der Arzneimittelinformationen auf AIPS zu kostenbasierten Preisen anzubieten.
4. Galenica AG und HCI Solutions AG werden in Anwendung von Art.
49a Abs. 1 i.V. mit Art. 7
i.V. mit Art. 7 KG wegen unzulässiger Verhaltensweise mit einem Betrag von CHF 4'546'123
belastet. Der Betrag von insgesamt CHF 4'546'123 wird den Adressaten der Verfügung
unter solidarischer Haftung auferlegt.
KG wegen unzulässiger Verhaltensweise mit einem Betrag von CHF 4'546'123
belastet. Der Betrag von insgesamt CHF 4'546'123 wird den Adressaten der Verfügung
unter solidarischer Haftung auferlegt.
5. Die Beweisanträge von Galenica AG und HCI Solutions AG, inklusive
derjenigen, die durch die früheren Tochtergesellschaften Documed AG und e-mediat AG eingereicht
wurden, werden abgewiesen.
6. Die Verfahrenskosten in Höhe von CHF [...] werden Galenica
AG und HCI Solutions AG auferlegt.
7. Im Übrigen wird die Untersuchung eingestellt.
8. [Eröffnung der Verfügung]
9. [Zustellung der Verfügung]
[Rechtsmittelbelehrung]"
G.d.b Zur
Begründung erwog die Vorinstanz zusammengefasst, die Galenica-Gruppe habe mittels ihrer Tochtergesellschaften
HCI, Documed und e-mediat eine marktbeherrschende Stellung auf dem Markt für veredelte, maschinenlesbare
Daten betreffend Medikamenteninformationen sowie auf dem Markt für den Zugang zu elektronischen
Datensätzen betreffend Medikamenteninformationen.
G.d.c Documed
und e-mediat hätten zwar ab 1. Januar 2013 von den Zulassungsinhaberinnen für die Aufnahme
in ihre Datenbank eine Entschädigung für die zuvor unentgeltlich erbrachte Dienstleistung verlangt.
Es sei jedoch nicht genügend erstellt, dass damit der Tatbestand der Erzwingung unangemessener Preise
im Sinne von Art. 7 Abs. 2 Bst. c KG erfüllt sei. Insbesondere die Unangemessenheit der Bepreisung
für die Aufnahme der Medikamenteninformationen in die Datenbank könne nicht mit dem erforderlichen
Beweismass nachgewiesen werden.
KG erfüllt sei. Insbesondere die Unangemessenheit der Bepreisung
für die Aufnahme der Medikamenteninformationen in die Datenbank könne nicht mit dem erforderlichen
Beweismass nachgewiesen werden.
G.d.d Weiter
erwog die Vorinstanz, e-mediat habe in einem Vertrag und möglicherweise auch in einem weiteren Vertrag
mit einem Softwarehaus eine Klausel aufgenommen, die es den Softwarehäusern untersage, zusätzliche
Partner- und Produkte-Stamm-Daten auf dem Markt zu beschaffen. Sie müssten exklusiv e-mediat ein
Vorrecht gewähren. Nur falls e-mediat diese Daten nicht anbieten möchte oder könne, sei
es den Softwarehäusern gestattet, diese Daten bei anderen Datenveredlern zu beschaffen bzw. diese
Daten selbst aus Primärquellen zu beziehen und zu veredeln. Damit liege eine Alleinbezugspflicht
für neu nachgefragte Daten zugunsten e-mediat vor. In 83 weiteren Verträgen mit Softwarehäusern
sei zudem eine Klausel zu finden, die es den Softwarehäusern untersage, die vorhandenen Strukturen
für Produkte von anderen Datenveredlern bzw. für eigene Datenbanken zu verwenden, wenn die
Softwarehäuser selbst die Daten veredeln wollten. Beide Klauseln würden den Markt für
veredelte, maschinenlesbare Daten betreffend Medikamenteninformationen für aktuelle und potentielle
Konkurrenten verschliessen und somit wettbewerbswidrige Effekte zeitigen. Denn aufgrund der Klauseln
müssten potenzielle Konkurrenten einen vollständigen Datensatz anbieten. Auch sei um die Durchsetzung
des Vertrages zu sichern eine Konventionalstrafe vereinbart worden. Die systematische Anwendung dieser
Klauseln zeige, dass die Strategie gegen allfällige Konkurrenten gerichtet gewesen sei. Sachliche
Rechtfertigungsgründe für diese Klauseln seien nicht ersichtlich, weshalb durch diese der Absatz
der Konkurrenten in missbräuchlicher Art und Weise im Sinne von Art. 7 Abs.1 i.V.m. Abs. 2 Bst.
e KG eingeschränkt werde.
i.V.m. Abs. 2 Bst.
e KG eingeschränkt werde.
G.d.e Weiter
erwog die Vorinstanz, auch der Verdacht von unzulässigen Koppelungsgeschäften habe sich teilweise
erhärtet. Softwarehäuser und Leistungserbringerinnen und -erbringer, welche die INDEX-Produkte
bei e-mediat beziehen, müssten sowohl die Medikamenteninformationen als auch die Daten von
Non-Pharma Produkten beziehen. Bei diesem sogenannten Datenbundling könne das Vorliegen von Verdrängungseffekten
aber nicht bewiesen werden. Deshalb sei diesbezüglich der Tatbestand der an den Abschluss von Verträgen
gekoppelten Bedingung im Sinne von Art. 7 Abs.1 i.V.m. Abs. 2 Bst. f KG nicht erfüllt.
i.V.m. Abs. 2 Bst. f KG nicht erfüllt.
G.d.f Anders
zu beurteilen sei aber der Sachverhalt, wonach die Arzneimittelinformationen in die INDEX-Datenbanken
nur aufgenommen würden, wenn die Zulassungsinhaberinnen gleichzeitig die Dienstleistung der redaktionellen
Qualitätskontrolle, der technischen Aufarbeitung der Fachinformationen und der Optimierung von Tabellen
und Grafiken bei Documed/e-mediat beziehen würden. Zudem werde der Upload der Medikamenteninformationen
auf AIPS kostenlos dazu angeboten. Dabei handle es sich um eine reine Bündelung. Die Dienstleistung
der redaktionellen und technischen Qualitätskontrolle sei eine von der Dienstleistung der Aufnahme
in das Kompendium und in die INDEX-Daten getrennte Dienstleistung. Auch der Upload der Arzneimittelinformationen
auf AIPS sei ein zusätzlicher Arbeitsschritt, der unabhängig von der Aufnahme der Daten in
die INDEX-Produkte vollzogen werden könne. Dieses sogenannte Modulbundling zeitige Verdrängungs-
und Ausbeutungs- und somit wettbewerbsschädigende Effekte. Ausreichende Rechtfertigungsgründe
seien keine vorgebracht worden, denn weder das Argument der marginalen Zusatzkosten, noch dasjenige der
in der Untersuchung "Publikation von Arzneimittelinformationen"
noch zulässigen Koppelung im regulierten Bereich, noch die Vorbringen im Zusammenhang mit der Patientensicherheit
hätten verfangen. Damit sei der Tatbestand der an den Abschluss von Verträgen gekoppelten Bedingung
im Sinne von Art. 7 Abs. 1 i.V.m. Abs. 2 Bst. f KG erfüllt.
i.V.m. Abs. 2 Bst. f KG erfüllt.
G.d.g Weiter
stellte die Vorinstanz fest, dass die Preise der Module im Leistungskatalog von Documed/e-mediat für
die Zulassungsinhaberinnen identisch seien, unabhängig davon, ob die Arzneimittelinformationen Änderungen
erfahren hätten oder nicht. In diesem Zusammenhang seien aber eine Wettbewerbsbehinderung und konkrete
Diskriminierungsfälle bei Preisen oder sonstigen Geschäftsbedingungen (Art. 7 Abs. 2 Bst. b KG) nicht genügend bewiesen. Die bis anhin undifferenzierte Festlegung der Preise für die Aufnahme
der Arzneimittelinformationen in die INDEX-Datenbank habe sich nicht als kartellrechtlich problematisch
erhärten lassen.
KG) nicht genügend bewiesen. Die bis anhin undifferenzierte Festlegung der Preise für die Aufnahme
der Arzneimittelinformationen in die INDEX-Datenbank habe sich nicht als kartellrechtlich problematisch
erhärten lassen.
G.d.h Schliesslich
erwog die Vorinstanz, im Untersuchungsverfahren habe sich auch die Frage gestellt, ob sich HCI im Zusammenhang
mit der AIPS-Ausschreibung unzulässig verhalten habe, indem sie die Mitbewerber für die Ausschreibung
betreffend den Preis missbräuchlich im Sinne von Art. 7 Abs. 1 i.V.m. Abs. 2 Bst. d KG unterboten
habe. Das Angebot von HCI zur Implementierung und zum jährlichen Betrieb von AIPS habe deutlich
unter den Angeboten der anderen Offerenten gelegen. Auf eine umfangreiche Kostenanalyse werde jedoch
verzichtet, womit offengelassen werde, ob der Tatbestand von Art. 7 Abs. 1
i.V.m. Abs. 2 Bst. d KG unterboten
habe. Das Angebot von HCI zur Implementierung und zum jährlichen Betrieb von AIPS habe deutlich
unter den Angeboten der anderen Offerenten gelegen. Auf eine umfangreiche Kostenanalyse werde jedoch
verzichtet, womit offengelassen werde, ob der Tatbestand von Art. 7 Abs. 1 i.V.m. Abs. 2 Bst. d KG erfüllt
sei. Dies rechtfertige sich, da der Preismissbrauch gegenüber den Zulassungsinhaberinnen im Zentrum
stehe, andere missbräuchliche Verhaltensweisen nachgewiesen worden seien und der Aufwand einer Kostenanalyse
im Vergleich zum möglichen Ergebnis eines weiteren Verstosses gegen Art. 7
i.V.m. Abs. 2 Bst. d KG erfüllt
sei. Dies rechtfertige sich, da der Preismissbrauch gegenüber den Zulassungsinhaberinnen im Zentrum
stehe, andere missbräuchliche Verhaltensweisen nachgewiesen worden seien und der Aufwand einer Kostenanalyse
im Vergleich zum möglichen Ergebnis eines weiteren Verstosses gegen Art. 7 KG unverhältnismässig
wäre.
KG unverhältnismässig
wäre.
G.d.i Im
Ergebnis folgerte die Vorinstanz, dass die Beschwerdeführerinnen infolge unzulässiger Verhaltensweisen
im Sinne von Art. 7 KG gestützt auf Art. 49a Abs. 1
KG gestützt auf Art. 49a Abs. 1 KG zu sanktionieren seien. Es sei von einem
zumindest eventualvorsätzlichen Kartellrechtsverstoss auszugehen. Zur Bestimmung des Basisbetrages
könne auf die kumulierten Umsätze von Documed und e-mediat in den Jahren 2013 bis 2015 abgestellt
werden. Der Schwere und Art der Kartellrechtsverstösse angemessen zu erachten sei ein Basisbetrag
in der Höhe von 5%. Die Verhaltensweisen und die wettbewerbsschädigenden Effekte hätten
mit der Offertstellung an die Zulassungsinhaberinnen im September 2012 begonnen und bis zum Zeitpunkt
des Erlasses der Verfügung angehalten. Deshalb sei von einer Dauer von 44 Monaten (September 2012
bis Mitte Mai 2016) auszugehen und der Sanktionsbetrag somit um 33.3333 % zu erhöhen. Weiter sei
der Basisbetrag aufgrund erschwerender Umstände zu erhöhen. Es liege ein wiederholter Verstoss
gegen das Kartellgesetz vor. Betreffend Documed sei bereits 2008 eine unzulässige Verhaltensweise
im Sinne von Art. 7 Abs. 1
KG zu sanktionieren seien. Es sei von einem
zumindest eventualvorsätzlichen Kartellrechtsverstoss auszugehen. Zur Bestimmung des Basisbetrages
könne auf die kumulierten Umsätze von Documed und e-mediat in den Jahren 2013 bis 2015 abgestellt
werden. Der Schwere und Art der Kartellrechtsverstösse angemessen zu erachten sei ein Basisbetrag
in der Höhe von 5%. Die Verhaltensweisen und die wettbewerbsschädigenden Effekte hätten
mit der Offertstellung an die Zulassungsinhaberinnen im September 2012 begonnen und bis zum Zeitpunkt
des Erlasses der Verfügung angehalten. Deshalb sei von einer Dauer von 44 Monaten (September 2012
bis Mitte Mai 2016) auszugehen und der Sanktionsbetrag somit um 33.3333 % zu erhöhen. Weiter sei
der Basisbetrag aufgrund erschwerender Umstände zu erhöhen. Es liege ein wiederholter Verstoss
gegen das Kartellgesetz vor. Betreffend Documed sei bereits 2008 eine unzulässige Verhaltensweise
im Sinne von Art. 7 Abs. 1 i.V.m. Abs. 2 Bst. a KG rechtskräftig festgestellt worden. Die kurze
Dauer seit dem letzten Verstoss sowie die Gleichartigkeit des Verstosses seien erschwerend zu berücksichtigen,
was eine Erhöhung der Sanktion um 20 % rechtfertige. Mildernde Umstände lägen demgegenüber
nicht vor. Weder hätten die Beschwerdeführerinnen die Verhaltensweisen eingestellt, noch läge
eine überdurchschnittliche Kooperation vor. Entsprechend erachtete die Vorinstanz eine Sanktion
in der Höhe von Fr. 4'545'123.- als angemessen, welche den Beschwerdeführerinnen
unter solidarischer Haftung aufzuerlegen sei.
i.V.m. Abs. 2 Bst. a KG rechtskräftig festgestellt worden. Die kurze
Dauer seit dem letzten Verstoss sowie die Gleichartigkeit des Verstosses seien erschwerend zu berücksichtigen,
was eine Erhöhung der Sanktion um 20 % rechtfertige. Mildernde Umstände lägen demgegenüber
nicht vor. Weder hätten die Beschwerdeführerinnen die Verhaltensweisen eingestellt, noch läge
eine überdurchschnittliche Kooperation vor. Entsprechend erachtete die Vorinstanz eine Sanktion
in der Höhe von Fr. 4'545'123.- als angemessen, welche den Beschwerdeführerinnen
unter solidarischer Haftung aufzuerlegen sei.
G.d.j Zu
den Kosten erwog die Vorinstanz schliesslich, die Beschwerdeführerinnen seien gebührenpflichtig
im Sinne von Art. 27 ff. KG. In Anbetracht des vom Antrag des Sekretariates abweichenden Entscheides
sei ein pauschaler Abzug in der Höhe eines Drittels der Kosten für die Tatbestände, die
sich nicht erhärtet hätten, zu gewähren und zulasten der Staatskasse auszuscheiden. Somit
sei den Beschwerdeführerinnen unter solidarischer Haftung eine Gebühr von Fr. [...] aufzuerlegen.
ff. KG. In Anbetracht des vom Antrag des Sekretariates abweichenden Entscheides
sei ein pauschaler Abzug in der Höhe eines Drittels der Kosten für die Tatbestände, die
sich nicht erhärtet hätten, zu gewähren und zulasten der Staatskasse auszuscheiden. Somit
sei den Beschwerdeführerinnen unter solidarischer Haftung eine Gebühr von Fr. [...] aufzuerlegen.
H. Verfahren
vor Bundesverwaltungsgericht
H.a Beschwerde
H.a.a Gegen
die Verfügung der Vorinstanz vom 19. Dezember 2016 erhoben die Beschwerdeführerinnen am 4.
Mai 2017 Beschwerde an das Bundesverwaltungsgericht.
H.a.b Sie
stellen folgende Rechtsbegehren:
"1. Die Ziffern 1, 2, 3, 4 und 5 des Dispositivs der Verfügung
der Wettbewerbskommission vom 19. Dezember 2016 seien in Bezug auf HCI Solutions AG und in Bezug auf
Galenica AG aufzuheben.
2. Eventualiter: Die Ziffern 4 und 6 des Dispositivs der Verfügung
der Wettbewerbskommission vom 19. Dezember 2016 seien zu korrigieren, indem davon abzusehen sei, Galenica
AG und HCI Solutions AG eine Sanktion und/oder Verfahrenskosten aufzuerlegen oder indem die Galenica
AG und HCI Solutions AG betreffende Sanktion und/oder Verfahrenskosten zu reduzieren seien.
- unter Kosten- und Entschädigungsfolge zu Lasten des
Bundes -"
H.a.c Gleichzeitig
stellen sie folgende Verfahrensanträge:
"1. Die Akten der Untersuchung 32-0249 seien bei der Vorinstanz
einzuholen.
2. Es sei ein zweiter Schriftenwechsel i.S.v. Art. 37 VGG i.V.m. Art.
57 Abs. 2
VGG i.V.m. Art.
57 Abs. 2 VwVG anzuordnen.
VwVG anzuordnen.
3. Es sei eine öffentliche Parteiverhandlung i.S.v. Art. 40
Abs. 1 VGG und/oder eine Instruktionsverhandlung i.S.v. Art. 57 Abs. 2
VGG und/oder eine Instruktionsverhandlung i.S.v. Art. 57 Abs. 2 VwVG durchzuführen.
VwVG durchzuführen.
4. Diese Beschwerde sowie sämtliche Beilagen zu dieser Beschwerde
enthalten Geschäftsgeheimnisse der beteiligten Unternehmen. Entsprechend seien die darin enthaltenen
Informationen Dritten nicht offenzulegen.
5. Im Fall einer Entscheidpublikation sei der zu publizierende Text
vor dessen Veröffentlichung zur Prüfung auf allfällige Geschäftsgeheimnisse hin den
Beschwerdeführerinnen zuzustellen."
H.a.d Zudem
beantragen sie in der Beschwerde und in weiteren Eingaben die Parteibefragung von H._______, O._______
und K._______.
H.a.e Zur
Begründung machen die Beschwerdeführerinnen die unrichtige bzw. unvollständige Feststellung
des rechtserheblichen Sachverhalts, verschiedene Verletzungen von Bundesrecht sowie Unangemessenheit
geltend.
H.a.f Im
Zusammenhang mit der Feststellung der marktbeherrschenden Stellung kritisieren die Beschwerdeführerinnen
vorweg die von der Vorinstanz vorgenommene Marktabgrenzung betreffend die Marktgegenseiten der Leistungserbringerinnen
und -erbringer. So würden die Softwarehäuser nicht zur Marktgegenseite gehören, denn die
Lizenzverträge würden direkt mit den Leistungserbringerinnen und -erbringern - mit Ausnahme
des medINDEX - abgeschlossen werden. Bei der räumlichen Abgrenzung des Marktes müsse
zudem berücksichtigt werden, dass potenzieller Wettbewerb auch von ausländischen Anbietern
ausgehen könne.
H.a.g Im
Zusammenhang mit der Beurteilung der Marktstellung auf dem Markt für veredelte, maschinenlesbare
Daten betreffend Medikamenteninformationen rügen die Beschwerdeführerinnen, die Vorinstanz
habe zu Unrecht das Vorliegen von aktuellem und potenziellem Wettbewerb verneint. Denn HCI könne
sich nicht unabhängig verhalten. Mit ywesee sei eine aktuelle Konkurrentin vorhanden und auch andere
Konkurrenten könnten HCI konkurrieren, würden sie Investitionen tätigen und eine Fachredaktion
aufbauen. Ferner sei zu berücksichtigen, dass sich der Markt mit Inkrafttreten des neuen HMG stark
verändern werde. Schliesslich sei der Markt durch niedrige Sunk Costs, keine erheblichen Switching
Costs oder andere Lock-in-Effekte geprägt. Vielmehr würden Inventionen und Innovationen eine
wichtige Rolle spielen, was sich in einem "the winner takes it all"-Ergebnis niederschlage.
H.a.h Betreffend
die Marktgegenseite der Zulassungsinhaberinnen rügen die Beschwerdeführerinnen, dass der sachlich
relevante Markt nicht nur wie von der Vorinstanz festgestellt den Markt für den "Zugang"
zu elektronischen Datensätzen betreffend Medikamenteninformationen umfasse, sondern auch "die
Aufbereitung und Kontrolle der Daten sowie die Aufnahme und der Erhalt/den Unterhalt in den elektronischen
Datensätzen und gleichzeitig die Nutzung einer aufgebauten Infrastruktur". Bei der räumlichen
Abgrenzung des Marktes sei die zukünftige Öffnung des Marktes einzubeziehen. Bei
der Beurteilung der Marktstellung müsse mit einbezogen werden, dass auf der Marktgegenseite der
HCI mitunter global tätige Pharmakonzerne ständen, welche die finanzielle Kraft hätten,
um jederzeit in den Markt einzutreten. [...]. Mit ywesee sei eine aktuelle Konkurrentin vorhanden.
Im Ergebnis habe die Vorinstanz unrichtig erwogen, dass HCI über einen Marktanteil von 100% verfüge
und potentieller Wettbewerb nicht möglich sei.
H.a.i Weiter
beanstanden die Beschwerdeführerinnen die separate Feststellung der marktbeherrschenden Stellung
im Dispositiv. Einerseits sei eine solche im Dispositiv einer Sanktionsverfügung gemäss Art.
49a KG nach der neueren bundesgerichtlichen Rechtsprechung weder erforderlich noch zulässig. Andererseits
würden die Beschwerdeführerinnen aufgrund der erfolgten Umstrukturierungen nicht mehr demselben
Konzern angehören. Schon zum Zeitpunkt der Eröffnung der Verfügung sei die Beschwerdeführerin
2 keine Tochtergesellschaft der Beschwerdeführerin 1 mehr gewesen, weshalb die Feststellung in Ziffer
1 des Dispositivs aufzuheben sei.
KG nach der neueren bundesgerichtlichen Rechtsprechung weder erforderlich noch zulässig. Andererseits
würden die Beschwerdeführerinnen aufgrund der erfolgten Umstrukturierungen nicht mehr demselben
Konzern angehören. Schon zum Zeitpunkt der Eröffnung der Verfügung sei die Beschwerdeführerin
2 keine Tochtergesellschaft der Beschwerdeführerin 1 mehr gewesen, weshalb die Feststellung in Ziffer
1 des Dispositivs aufzuheben sei.
H.a.j Betreffend
den Vorwurf der Einschränkung des Absatzes durch die Klauseln A und B in den Verträgen mit
den Softwarehäusern machen die Beschwerdeführerinnen geltend, bei beiden Klauseln handle es
sich nicht um ein Verbot zur Zusammenarbeit mit Drittanbietern und somit nicht um eine Alleinbezugsverpflichtung,
sondern nur um einen Zustimmungsvorbehalt. Die Klausel A finde sich nur in einem und die Klausel B nur
in 83 von insgesamt 175 Verträgen, womit die überwiegende Mehrheit der Softwarehäuser
nicht an eine solche Klausel gebunden gewesen sei. Es habe sich auch nie ein Softwarehaus auf die Klausel
A oder B berufen. Vielmehr hätte HCI die entsprechende Erlaubnis erteilt, wenn sie angefragt worden
wäre. Die Vorinstanz vermöge mit keinem Beispiel zu beweisen, dass die monierten Klauseln eine
absatzeinschränkende Wirkung gehabt hätten. Der mangelnde Erfolg der Konkurrenten sei auf die
Qualitätsunterschiede bei den angebotenen Daten zurückzuführen.
H.a.k Des
Weiteren sei in Anlehnung an das europäische Wettbewerbsrecht für die Erfüllung des Tatbestandes
von Art. 7 Abs. 1 i.V.m. Abs. 2 Bst. e KG eine Schädigung des wirksamen Wettbewerbs erforderlich.
Eine solche werde von der Vorinstanz aber weder dargelegt noch nachgewiesen. HCI habe mit den Klauseln
keine Verdrängungsstrategie verfolgt, sondern lediglich sicherstellen wollen, dass die INDEX-Daten
nicht ohne ihre Kenntnis verändert oder mit Drittdaten vermischt würden oder dass sie nur unvollständig
an die Leistungserbringerinnen und -erbringer übermittelt würden. Zudem habe es in qualitativer
Hinsicht in der untersuchten Zeitperiode keine vergleichbare Datenbank in der Schweiz gegeben, weshalb
der Erfolg der HCI auf der Qualität ihrer Leistungen und nicht auf den von der Vorinstanz genannten
Vertragsklauseln basiere. Jedenfalls bestehe eine glaubwürdige Alternativerklärung, weshalb
ywesee und ouwerkerk nicht mit dem gewünschten Erfolg in den Markt hätten eintreten können.
i.V.m. Abs. 2 Bst. e KG eine Schädigung des wirksamen Wettbewerbs erforderlich.
Eine solche werde von der Vorinstanz aber weder dargelegt noch nachgewiesen. HCI habe mit den Klauseln
keine Verdrängungsstrategie verfolgt, sondern lediglich sicherstellen wollen, dass die INDEX-Daten
nicht ohne ihre Kenntnis verändert oder mit Drittdaten vermischt würden oder dass sie nur unvollständig
an die Leistungserbringerinnen und -erbringer übermittelt würden. Zudem habe es in qualitativer
Hinsicht in der untersuchten Zeitperiode keine vergleichbare Datenbank in der Schweiz gegeben, weshalb
der Erfolg der HCI auf der Qualität ihrer Leistungen und nicht auf den von der Vorinstanz genannten
Vertragsklauseln basiere. Jedenfalls bestehe eine glaubwürdige Alternativerklärung, weshalb
ywesee und ouwerkerk nicht mit dem gewünschten Erfolg in den Markt hätten eintreten können.
H.a.l Sodann
bringen die Beschwerdeführerinnen vor, mit den Klauseln hätten Leistungsstörungen in den
Lizenzverträgen zwischen HCI und den Leistungserbringerinnen und -erbringern, Haftungs- und Reputationsrisiken
sowie UWG-Verletzungen verhindert werden wollen. Entsprechend sei die Verhaltensweise durch legitimate
business reasons gerechtfertigt. Die Vorinstanz habe sich mit diesen Argumenten aber nicht auseinandergesetzt.
H.a.m Zum
Vorwurf der unzulässigen Koppelung von Leistungen halten die Beschwerdeführerinnen fest, eine
Koppelung sei nur dann unzulässig, wenn tatsächlich zwei getrennte Güter oder Leistungen
kombiniert angeboten würden. Die Prüfung, ob getrennte Güter vorlägen, habe gestützt
auf eine marktorientierte Abgrenzung zu erfolgen. Eine genaue marktorientierte Analyse der Frage, ob
die gekoppelten Dienstleistungen in unterschiedlichen Märkten nachgefragt würden, könne
nur unterbleiben, falls offensichtlich feststehe, dass es sich beim Haupt- und Zusatzprodukt um separate
Produkte handle. Vorliegend habe die Vorinstanz Inhalt und Bedeutung der angeblich gekoppelten Dienstleistungen
nicht untersucht, keine Marktabgrenzung vorgenommen und auf eine marktorientierte Analyse der Frage,
ob die gekoppelten Dienstleistungen in unterschiedlichen Märkten nachgefragt würden, verzichtet.
Eine Begründung für diesen Verzicht fehle.
H.a.n Die
Validierung der Daten durch die Fachredaktion sei eine notwendigerweise vorausgesetzte Eigenschaft der
INDEX- und Kompendiumsdaten. Andere Unternehmen, welche Qualitätssicherungsmassnahmen anbieten würden,
würden nicht jene Dienstleistungen erbringen, welche für die Qualitätssicherung der INDEX-Datenbanken
erforderlich seien. Es fehle auch an einem Beweis für die von der Vorinstanz behauptete Verdrängungswirkung.
H.a.o Das
Compendium und die INDEX-Datenbanken würden äusserst sensitive Daten enthalten, für deren
Korrektheit HCI gegenüber ihren Vertragspartnern Gewähr leiste, weshalb sich HCI selber von
der Korrektheit und Vollständigkeit der Daten überzeuge müsse. Zudem verursache der Upload
auf AIPS nur einen marginalen Aufwand von Sekunden bzw. Minuten. Entsprechend sei die Verhaltensweise
durch die legitimen Gründe Patientensicherheit und Effizienzgewinn gerechtfertigt.
H.a.p Hinsichtlich
der Sanktionierung rügen die Beschwerdeführerinnen, die Vorinstanz sei zu Unrecht zum Schluss
gekommen, dass sie zumindest eventualvorsätzlich gehandelt hätten. Aus dem früheren Kartellrechtsverfahren
gegen Documed könne betreffend den Vorwurf der Koppelung nicht auf die Vorhersehbarkeit eines Verstosses
gegen das Kartellgesetz geschlossen werden. Hinzukomme, dass im Schreiben des Sekretariates vom 6. Dezember
2012 der Vorwurf der unzulässigen Koppelung von Leistungen noch nicht bestanden und HCI die neuen
Verträge vorgängig dem Sekretariat eingereicht habe. Auch habe sie um Beratung ersucht, was
jedoch vom Sekretariat abgelehnt worden sei. Die Vorinstanz habe nicht begründet, inwiefern die
Beschwerdeführerinnen eine objektive Sorgfaltspflicht verletzt hätten oder ein Organisationsverschulden
vorläge. Entsprechend sei auch Fahrlässigkeit zu verneinen.
H.a.q Sodann
kritisieren die Beschwerdeführerinnen auch die Bemessung der Sanktion. Die Vorinstanz habe es unterlassen,
anhand der abgegrenzten sachlich relevanten Märkten und der vorgeworfenen Verhaltensweisen eine
getrennte Berechnung der relevanten Umsätze auf beiden Märkten vorzunehmen. Zudem hätte
die Vorinstanz bei der Bestimmung des Basisbetrages nur diejenigen Umsätze der Documed und e-mediat
berücksichtigen dürfen, die auch tatsächlich auf den relevanten Märkten erzielt worden
seien. Die Vorinstanz habe aber auch Umsätze auf nicht relevanten Märkten in ihre Berechnung
miteinbezogen, ebenso konzerninterne Umsätze. Diese seien jedoch in Abzug zu bringen.
H.a.r Weiter
seien auch die zur Art und Schwere des Verstosses gemachten Erwägungen der Vorinstanz nicht haltbar.
Die Verhaltensweise der HCI sei nicht Ausdruck einer Gesamtstrategie "mit der die Kontrolle über
die Gesamtwertschöpfungskette" hätte gesichert werden können. Unsachgemäss seien
die Erwägungen auch, weil die Vorinstanz darin implizit davon ausgehe, dass den nicht als unzulässig
qualifizierten Verhaltensweisen gleichwohl ein Unrechtsgehalt beiliege. Auch die Dauer des Verstosses
sei unrichtig auf 44 Monate anstelle von 40 Monaten festgelegt worden. Die Erhöhung des Basisbetrages
um 33,33% erscheine aber gerechtfertigt. Der Umstand, dass sich Documed bereits einmal eine rechtskräftig
festgestellte unzulässige Verhaltensweise im Sinne von Art. 7 KG habe zu Schulden komme lasse, könne
aufgrund der nicht nachgewiesenen Gleichartigkeit der Verhaltensweisen nicht erschwerend bzw. höchstens
im Umfang von 10% berücksichtigt werden. Auf der anderen Seite müsse aber bei der Sanktionsberechnung
die gute Kooperation der HCI mildernd berücksichtigt werden.
KG habe zu Schulden komme lasse, könne
aufgrund der nicht nachgewiesenen Gleichartigkeit der Verhaltensweisen nicht erschwerend bzw. höchstens
im Umfang von 10% berücksichtigt werden. Auf der anderen Seite müsse aber bei der Sanktionsberechnung
die gute Kooperation der HCI mildernd berücksichtigt werden.
H.a.s Schliesslich
rügen die Beschwerdeführerinnen die Kostenfestlegung der Vorinstanz. Die ihr aufzuerlegenden
vorinstanzlichen Kosten seien nicht nur um einen, sondern um zwei Drittel zu reduzieren, da vier der
insgesamt sechs untersuchten Verhaltensweisen als nicht missbräuchlich qualifiziert worden seien
und es sich bei den aufrecht erhaltenen Vorwürfen um "Nebenschauplätze" handle.
H.b Vernehmlassung
H.b.a Mit
Vernehmlassung vom 10. Juli 2017 beantragt die Vorinstanz die Abweisung der Beschwerde. Gleichzeitig
reichte sie die Verfahrensaktenakten (auf zwei Memory-Sticks) ein.
H.b.b Vorweg
hält die Vorinstanz zur Begründung in allgemeiner Weise fest, das regulatorische Konzept sehe
vor, dass alle Datenveredler von der Plattform AIPS, welche als Bindeglied zwischen Zulassungsinhaberinnen
und Datenveredler zu verstehen sei, den kompletten Stamm der Fach- und Patienteninformationen downloaden
könnten, um ihn sodann für ihre veredelten Produkte zu verwenden. HCI verkehre mit ihrem Geschäftsmodell
dieses Konzept in sein Gegenteil. Auch sei im gesetzlichen System der öffentlichen Aufgabe der Gewährleistung
der Patientensicherheit HCI oder ihre Datenbank nicht vorgesehen. Deshalb entbehre die Ausführung,
HCI nehme eine öffentliche Aufgabe wahr und habe die Patientensicherheit zu gewährleisten,
einer gesetzlichen Grundlage und sei nicht korrekt. Weiter sei der Zeithorizont der Verhaltensweisen
insbesondere im Kontext des Entscheides des Bundesverwaltungsgerichts betreffend die Publikationspflicht
zu berücksichtigen. Dieser und die Einführung von AIPS hätten aus Sicht der Beschwerdeführerinnen
die Gefahr des Verlusts des Monopols über die (elektronischen) Medikamenteninformationen mit sich
gebracht. Zur Sicherung der Marktposition hätten die Beschwerdeführerinnen 2012 verschiedene
Massnahmen ergriffen, wobei nur gewisse davon Leistungswettbewerb dargestellt hätten und andere
als missbräuchliche Verhaltensweisen i.S.v. Art. 7 KG zu qualifizieren seien. Massnahmen oder Änderungen
nach dem Jahr 2014 hätten deshalb kaum eine Auswirkung und würden das Gesamtbild der missbräuchlichen
Verhaltensweisen nicht erschüttern können.
KG zu qualifizieren seien. Massnahmen oder Änderungen
nach dem Jahr 2014 hätten deshalb kaum eine Auswirkung und würden das Gesamtbild der missbräuchlichen
Verhaltensweisen nicht erschüttern können.
H.b.c Betreffend
die Marktabgrenzung und die Feststellung der Marktbeherrschung verweist die Vorinstanz auf ihre Ausführungen
in der angefochtenen Verfügung. Es sei dargelegt worden, weshalb ein Wettbewerb "um" den
Markt abgelehnt werde. Aber selbst wenn man von einem Wettbewerb "um" den Markt ausgehe, läge
eine marktbeherrschende Position vor. Denn es sei weder ein aktueller Konkurrent ersichtlich, der in
der Lage sei, den Beschwerdeführerinnen den Markt streitig zu machen, noch seien irgendwelche konkreten
Anzeichen vorhanden, dass potentielle Konkurrenz entstehen könnte, die einen disziplinierenden Einfluss
auf die Verhaltensweise der Beschwerdeführerinnen haben könnte.
H.b.d Auch
betreffend die isolierte Feststellung der marktbeherrschenden Stellung der Beschwerdeführerinnen
verweist die Vorinstanz auf ihre Erwägungen in der Verfügung. Ergänzend hält sie
fest, es sei unzutreffend, dass HCI zum Zeitpunkt der Eröffnung der Verfügung keine Tochtergesellschaft
von Vifor (vormals Galenica) mehr gewesen sei. Zwar sei aus dem Sacheinlagevertrag ersichtlich, dass
HCI auf die am 13. Februar 2017 gegründete Galenica Santé, unterdessen wiederum firmierend
unter Galenica AG, übertragen worden sei. Aber aus kartellrechtlicher Sicht habe sich zu diesem
Zeitpunkt nichts geändert, da die Galenica Santé zum Zeitpunkt der Gründung eine 100%ige
Tochtergesellschaft der Beschwerdeführerin 1 gewesen sei. Denn gemäss [...] habe die Sacheinlegerin,
die Beschwerdeführerin 1, als Gegenleistung für die Sacheinlage 50'000'000 Namenakten,
mithin 100% der Aktien erhalten. Es handle sich beim Sacheinlagevertrag vom 13. Februar 2017 somit um
eine konzerninterne Restrukturierung, die keinen Einfluss auf die Kontrollmöglichkeiten der Beschwerdeführerin
1 über die Beschwerdeführerin 2 gehabt habe.
H.b.e Betreffend
den Vorwurf der Einschränkung des Absatzes sei in der Verfügung ausführlich dargelegt
worden, dass die Klauseln A und B die Marktstellung der Beschwerdeführerinnen zementiert und den
Markt für potentielle Konkurrenten verschlossen habe. Einerseits sei grundsätzlich nicht relevant,
in wie viel Prozent der Verträge die relevanten Klauseln aufgenommen worden seien, sofern diese
eine verschliessende Wirkung gehabt hätten. Andererseits spreche bei der Klausel A bereits deren
Wortlaut gegen ein reines Zustimmungserfordernis. Aus dem Umstand, dass die Beschwerdeführerinnen
selbst mit keiner Anfrage konfrontiert worden seien, könne nicht gefolgert werden, die Klauseln
hätten sich nicht ausgewirkt. Vielmehr könne bereits die vertragliche Festlegung verschliessende
Wirkung zeitigen, dies insbesondere vor dem Hintergrund, dass die Marktzutrittsschranken für allfällige
Drittdatenanbieter bereits ohne diese Klauseln sehr hoch seien.
H.b.f Auch
betreffend die von den Beschwerdeführerinnen vorgebrachten Rechtfertigungsgründe verweist die
Vorinstanz auf ihre Ausführungen in der Verfügung. Das Argument, die Klausel habe der Verhinderung
von Verletzungen gegen das UWG gedient, sei neu. Es sei jedoch nicht stichhaltig, da die zivil- und/oder
strafrechtlichen Mittel offensichtlich als mildere Mittel als die Wettbewerbsbehinderung zur Verfügung
stünden. Da das Argument erst im Rahmen der Beschwerde nachgeschoben werde, könne diese Rechtfertigung
auch kaum dem ursprünglichen Zweck der Klausel entsprechen.
H.b.g In
Bezug auf den Vorwurf der Koppelung hält die Vorinstanz an ihren Erwägungen in der Verfügung
vollumfänglich fest. Die redaktionelle und technische Qualitätskontrolle der Arzneimittelinformationen
im Hinblick auf die Publikation sowie der Upload dieser Informationen auf AIPS einerseits und die Veredelung
von Medikamenteninformationen (inklusive einer allfälligen, mit der Erstellung des spezifischen
Produktes zusammenhängenden [erneuten] Qualitätssicherung) andererseits seien nicht dem gleichen
Markt zuzuordnen. Die Ausbeutungs- und Behinderungswirkungen der Koppelung seien im vorliegenden Fall
zu bejahen, auch wenn dies gemäss der Rechtsprechung des Bundesverwaltungsgerichts gar nicht gesondert
nachzuweisen wäre. Ein ausreichender Rechtfertigungsgrund sei nicht vorgebracht worden. In der Verfügung
werde dargelegt, dass weder das Argument marginaler Zusatzkosten, noch dasjenige der noch im Jahre 2008
zulässigen Koppelung im regulierten Bereich, noch die Vorbringen im Zusammenhang mit der Patientensicherheit
verfangen würden. Die Qualitätskontrolle im Hinblick auf die Publikation habe nicht zwingend
mit derjenigen eines Datenveredlers im Hinblick auf sein eigenes Produkt zu erfolgen.
H.b.h Betreffend
die Sanktionierung sei in der Verfügung dargelegt worden, weshalb eine zumindest eventualvorsätzliche
Tatbegehung vorliege. Auch seien alle Elemente für einen fahrlässigen Kartellrechtsverstoss
aufgezeigt worden. Bei der Gestaltung des Geschäftsmodells und der Verträge handle es sich
um einen Strategieentscheid, der von der Führungsebene getroffen werde. Daher sei ein Organisationsverschulden
- was für das Vorliegen von Verschulden im Sinne von Vorwerfbarkeit ausreichend sei -
in jedem Fall gegeben.
Darüber hinaus gehe auch das Vorbringen der Beschwerdeführerinnen, es treffe sie kein Verschulden,
da sie dem Sekretariat die überarbeiteten Verträge eingereicht habe, fehl. Die Einreichung
der Verträge sei im Rahmen des kartellrechtlichen Verfahrens erfolgt und nicht im Rahmen eines Widerspruchsverfahren
i.S.v. Art. 49a Abs. 2 Bst. b KG oder einer Beratung i.S.v. Art. 23 Abs. 2
KG oder einer Beratung i.S.v. Art. 23 Abs. 2 KG. Was die von den Beschwerdeführerinnen
geltend gemachte Beratungsanfrage von 2013 betreffe, sei festzuhalten, dass während eines kartellrechtlichen
Untersuchungsverfahrens kein Raum für eine Beratung nach Art. 23 Abs. 2
KG. Was die von den Beschwerdeführerinnen
geltend gemachte Beratungsanfrage von 2013 betreffe, sei festzuhalten, dass während eines kartellrechtlichen
Untersuchungsverfahrens kein Raum für eine Beratung nach Art. 23 Abs. 2 KG bestehe.
KG bestehe.
H.b.i Zur
Berechnung der Sanktion führt die Vorinstanz aus, eine Aufschlüsselung nach Märkten sei
nicht nötig und darüber hinaus gekünstelt, da der Umsatz auf den beiden erwähnten
Märkten erzielt worden sei und das Ergebnis der Berechnung von den Beschwerdeführerinnen auch
nicht beanstandet werde. Zum Vorwurf der Beschwerdeführerinnen, es seien Umsätze von nicht
relevanten Märkten in die Sanktionsberechnung miteinbezogen worden, hielt die Vorinstanz fest, die
von den Beschwerdeführerinnen nunmehr präsentierten "bereinigten" Umsatzzahlen seien
intransparent und es seien jeweils ohne sachliche Begründung unterschiedliche Umsatzzahlen als "bereinigte"
Umsatzzahlen vorgelegt worden. Es werde nicht belegt, dass und in welcher Höhe Umsätze auf
anderen Märkten erzielt worden seien. Ferner seien konzerninterne Umsätze nicht abzuziehen,
da praxisgemäss keine Unterscheidung danach vorzunehmen sei, welcher Anteil des Umsatzes durch ein
wettbewerbswidriges Verhalten erzielt worden sei und ob allenfalls ein Anteil nicht in Verbindung mit
einem wettbewerbswidrigen Verhalten stehe.
H.b.j Der
Vorwurf, die Sanktionsbegründung erwecke den Anschein, dass den vier nicht bestätigten Vorwürfen
des Sekretariats gleichwohl ein Unrechtsgehalt beiliege, gehe fehl. Vielmehr sei der Basisbetrag genau
aus diesem Grund im Vergleich zum Antrag (10%) massiv herabgesetzt worden (5%). Auch der Umstand, dass
sich Documed bereits einmal eine rechtskräftig festgestellte unzulässige Verhaltensweise im
Sinne von Art. 7 KG habe zu Schulden komme lasse, sei bei der Sanktionsbemessung korrekt erschwerend
berücksichtigt worden. Denn anders als die Bestimmung in der EU enthalte Art. 5 Abs. 1 Bst. a
KG habe zu Schulden komme lasse, sei bei der Sanktionsbemessung korrekt erschwerend
berücksichtigt worden. Denn anders als die Bestimmung in der EU enthalte Art. 5 Abs. 1 Bst. a der Verordnung über die Sanktionen bei unzulässigen Wettbewerbsbeschränkungen vom 12.
März 2004 (KG-Sanktionsverordnung, SVKG, SR
der Verordnung über die Sanktionen bei unzulässigen Wettbewerbsbeschränkungen vom 12.
März 2004 (KG-Sanktionsverordnung, SVKG, SR 251.5) keine Eingrenzung auf gleichartige oder
ähnliche Verstösse. Die von den Beschwerdeführerinnen geltend gemachte gute Kooperation
sei zu verneinen, vielmehr habe sich das Verfahren zu keinem Zeitpunkt als besonders transparent dargestellt.
251.5) keine Eingrenzung auf gleichartige oder
ähnliche Verstösse. Die von den Beschwerdeführerinnen geltend gemachte gute Kooperation
sei zu verneinen, vielmehr habe sich das Verfahren zu keinem Zeitpunkt als besonders transparent dargestellt.
H.b.k Betreffend
die Auferlegung der vorinstanzlichen Kosten könne nicht eine schematische Reduktion im Verhältnis
der Anzahl ursprünglich untersuchter Vorwürfe zu den erhärteten vorgenommen werden. Vielmehr
sei dem Umstand Rechnung zu tragen, dass ein erheblicher Teil des Aufwandes zur Erstellung des Sachverhaltes
und für das Verständnis das Marktes anfalle.
H.c Replik
und Duplik
H.c.a In
ihrer Replik vom 13. September 2017 halten die Beschwerdeführerinnen an den mit der Beschwerde vom
4. Mai 2017 gestellten Rechtsbegehren fest.
H.c.b Zum
Vorbringen der Vorinstanz, ihr Geschäftsmodell verkehre das regulatorisch vorgesehene Konzept, halten
die Beschwerdeführerinnen fest, Unternehmen wie HCI seien nicht verpflichtet, ihre privatwirtschaftlichen
Dienstleistungen im Sinne eines regulatorischen Konzepts anzubieten. Zudem sei es bei der Schaffung von
AIPS nicht um die Umsetzung eines weitgreifenden regulatorischen Konzeptes gegangen, sondern nur um die
Möglichkeit, eine gesetzeskonforme Publikationsplattform zu schaffen. Wenn HCI mit der Aufbereitung
der AIPS-Daten beauftragt werde, bereite sie die AIPS-Versionen sowie die übrigen Daten (Compendium
und INDEX) parallel auf. In Bezug auf die Publikation von Fach- und Patienteninformationen auf AIPS bestehe
ein unzureichender Regulierungsrahmen.
H.c.c Bei
der Frage der Marktbeherrschung sei zu berücksichtigen, dass sich die untersuchten Märkte rasch
wandeln könnten, was die beschlossene Revision des Heilmittelgesetzes zeige. Zudem dürfe das
Argument der Vorinstanz, die Beschwerdeführerinnen würden die Kosten der Validierung der Daten
weiterhin den Zulassungsinhaberinnen aufbürden, was die marktbeherrschende Stellung aufzeige, aufgrund
der Unschuldsvermutung keine Berücksichtigung finden.
H.c.d Betreffend
den Tatbestand der Einschränkung des Absatzes könne nicht nur aus dem europäischen Wettbewerbsrecht
und dem kürzlich ergangenen Entscheid Intel Corporation/Kommission
des Europäischen Gerichtshofes (EuGH) geschlossen werden, dass ein wettbewerbsschädigender
Effekt erforderlich sei, sondern auch das Bundesgericht habe im Entscheid Publigroupe
festgehalten, die Missbräuchlichkeit einschliesslich der Wettbewerbsschädigung der strittigen,
in Art. 7 Abs. 2 KG aufgeführten Verhaltensweisen müsse jeweils im Einzelfall festgestellt
werden (BGE 139 I 72, Publigroupe, E. 10.1.2). Die Feststellung
der Vorinstanz, bereits die vertragliche Festlegung könne sich marktverschliessend auswirken und
die Klauseln hätten möglicherweise Wirkungen gehabt, genüge somit nicht. Hinsichtlich
der mit der Beschwerde geltend gemachten Rechtfertigungsgründe wiederholen die Beschwerdeführerinnen,
HCI habe tatsächlich befürchtet, die Verwendung von Daten Dritter könne zu intransparenten
Verhältnissen führen. Auch sei der Rechtfertigungsgrund der Verhinderung von UWG-Verletzungen
nicht nachgeschoben, vielmehr hätten sich die Beschwerdeführerinnen bereits 2012 mit Schutzmöglichkeiten
vor UWG-Verletzungen befasst.
KG aufgeführten Verhaltensweisen müsse jeweils im Einzelfall festgestellt
werden (BGE 139 I 72, Publigroupe, E. 10.1.2). Die Feststellung
der Vorinstanz, bereits die vertragliche Festlegung könne sich marktverschliessend auswirken und
die Klauseln hätten möglicherweise Wirkungen gehabt, genüge somit nicht. Hinsichtlich
der mit der Beschwerde geltend gemachten Rechtfertigungsgründe wiederholen die Beschwerdeführerinnen,
HCI habe tatsächlich befürchtet, die Verwendung von Daten Dritter könne zu intransparenten
Verhältnissen führen. Auch sei der Rechtfertigungsgrund der Verhinderung von UWG-Verletzungen
nicht nachgeschoben, vielmehr hätten sich die Beschwerdeführerinnen bereits 2012 mit Schutzmöglichkeiten
vor UWG-Verletzungen befasst.
H.c.e Betreffend
den Vorwurf der Koppelung halten die Beschwerdeführerinnen daran fest, dass es an einer Abgrenzung
der relevanten Märkte fehle. Aus dem Urteil des Bundesverwaltungsgerichts B-2618/2013 vom 24. November
2016, dem Urteil des Bundesgerichts i.S. Publigroupe (BGE 139
I 72), welches insbesondere auf Lucas David/Reto Jacobs,
Schweizerisches Wettbewerbsrecht, 5. Aufl. 2012 verweise, sowie aus der jüngeren Rechtsprechung
in der EU ergebe sich, dass die negativen Effekte - die Wettbewerbsbehinderung - festgestellt
werden müssten.
H.c.f Betreffend
die Sanktionierung halten die Beschwerdeführerinnen an der Rüge, es fehle die Begründung,
worin genau die Fahrlässigkeit oder das Organisationsverschulden bestehen solle, fest. Ebenso halten
die Beschwerdeführerinnen daran fest, dass bei der Bestimmung des Basisbetrages nur diejenigen Umsätze
zu berücksichtigen seien, die auch tatsächlich auf den relevanten Märkten erzielt wurden
sowie dass die konzerninternen Umsätze abzuziehen sind. Sie erläutern in der Folge zahlreiche
vorzunehmende Abzüge vom Nettoerlös von Documed und e-mediat.
H.c.g Weiter
bringen die Beschwerdeführerinnen vor, die vorinstanzliche Sanktionsbegründung werde der Rechtsprechung
des Bundesverwaltungsgerichts nicht gerecht, auch wenn die Vorinstanz bei der Berücksichtigung von
Art und Schwere des Verstosses den Basisbetrag von 10% auf 5% reduziert habe. Die Begründung der
Vorinstanz bezüglich der Art und Schwere des Verstosses in der Verfügung entspreche grösstenteils
unverändert jener des Sekretariats im Antrag.
H.c.h Mit
Duplik vom 19. Oktober 2017 beantragt die Vorinstanz unverändert die Abweisung der Beschwerde.
H.c.i Die
Vorinstanz weist auf die Änderung der regulatorischen Rahmenbedingungen per 1. Januar 2013 hin.
Nach wie vor sei aber nur der Bereich der Publikation der Arzneimittelinformationen reguliert. Diese
habe auf der staatlichen Plattform AIPS zu erfolgen. Die Veredelung hingegen sei dem freien Markt überlassen
und dem Wettbewerb zugänglich. In diesem Umfeld hätten die Beschwerdeführerinnen ihre
bisher auf dem Papier getrennten Angebote durch ein neues, die Aufnahme in die INDEX-Datenbank umfassendes,
gemeinsames Angebot an die Zulassungsinhaberinnen ersetzt. Ausgehend von ihrer marktbeherrschenden Stellung
auf dem Markt für veredelte, maschinenlesbare Daten betreffend Medikamenteninformationen und der
daraus resultierenden Marktbeherrschung auf dem Markt für den Zugang zu elektronischen Datensätzen
betreffend Medikamenteninformationen hätten sie die Aufbereitung der Daten für die Publikation
mit der Aufnahme in ihre Datenbank gekoppelt. Damit hätten die Zulassungsinhaberinnen nicht mehr
frei wählen können, wer ihre Arzneimittelinformationen für die Publikation aufbereite,
ohne einen wirtschaftlichen Nachteil zu erleiden. Was marktgerecht und aus Nachfragesicht effizient sei,
dürfe nicht das marktbeherrschende Unternehmen entscheiden. Ein für ein marktbeherrschendes
Unternehmen effizientes und vorteilhaftes Verhalten sei nicht automatisch auch für den Markt bzw.
den Wettbewerb effizient und vorteilhaft. Durch die Koppelung würden Konkurrenten auf der Stufe
Publikation behindert und Zulassungsinhaberinnen benachteiligt.
H.c.j Im
Zeitraum, indem infolge Einführung einer behördlichen Publikationsplattform eine Öffnung
des Marktes möglich gewesen wäre, hätten die Beschwerdeführerinnen nicht nur die
Koppelung vorgenommen, sondern auch wettbewerbsbeschränkende Klauseln in ihre Verträge mit
Softwarehäusern aufgenommen. Diese Klauseln würden den Wettbewerb einschränken und helfen,
die vormaligen Marktstrukturen zu erhalten. Die Versuche mindestens zweier Konkurrenten, im Markt Fuss
zu fassen, seien erfolglos gewesen. Wie sich der Markt ohne Koppelung und ohne diese Klauseln hypothetisch
entwickelt hätte, könne nicht bewiesen werden. Der junge Markt sei von vornherein im Keim erstickt
worden.
H.c.k Mit
Eingabe vom 27. November 2017 nahmen die Beschwerdeführerinnen unaufgefordert zur Duplik der Vorinstanz
Stellung.
H.d Weitere
Verfahrensschritte
H.d.a Am
16. November 2018 reichten die Beschwerdeführerinnen eine weitere Eingabe inklusiv Kostennote ein.
Die Beschwerdeführerinnen legen darin im Wesentlichen dar, ihr Verhalten aufgrund des Verfahrens
vor der Vorinstanz vorläufig angepasst zu haben, sodass die von der Vorinstanz als unzulässig
qualifizierten Verhaltensweisen nicht mehr praktiziert würden. Die Erfahrungen auf dem Markt seit
der Anpassung des Verhaltens würden zeigen, dass sich die von der Vorinstanz als missbräuchlich
qualifizierten Verhaltensweisen von HCI nicht negativ auf den Wettbewerb ausgewirkt hätten.
H.d.b HCI
habe im April 2017 die Softwarehäuser schriftlich darüber informiert, nicht mehr an den Zustimmungsvorbehalt
gemäss der Klausel B gebunden zu sein. Entsprechend sei die Klausel B in einem Grossteil der Verträge
bereits seit 2015 nicht mehr in Kraft und seit April 2017 flächendeckend aufgehoben. Trotz der Verhaltensänderung
hätten keine Veränderungen in den Wettbewerbsverhältnissen stattgefunden. Es sei in der
Zwischenzeit kein zusätzlicher Datenanbieter in den Markt getreten und bestehende Anbieter hätten
ihren Marktanteil nicht ausgeweitet. Daraus sei ersichtlich, dass die Klauseln keine Wettbewerbswirkungen
gehabt hätten. Auch was das als unzulässig qualifizierte Verhalten der Koppelung betreffe,
habe sich HCI veranlasst gesehen, die Qualitätskontrolle für die Fachinformationen optional
anzubieten. Diese Optionalität sei künstlich und sorge für Verwirrung. Nur ein geringer
Prozentsatz der Zulassungsinhaberinnen würden neu auf die Qualitätskontrolle verzichten. Bei
der Weiterverarbeitung der Daten im INDEX (Strukturierung, Clinical Decision Support) müsse HCI
aber dennoch eine Qualitätskontrolle durchführen, welche nahezu alle relevanten Kapitel erfasse,
die HCI auch im Rahmen der beauftragten Prüfung der Fachinformation zu kontrollieren habe. Markteintritte
von Unternehmen, welche die Qualitätskontrolle in Konkurrenz zum Angebot von HCI erbringen würden,
habe es keine gegeben. Da es weder Markteintritte noch sonstige Veränderungen auf dem Markt gegeben
habe, aus welchen auf die Beeinträchtigung des Wettbewerbs durch HCI vor der Verhaltensanpassung
geschlossen werden könne, sei erstellt, dass die Vorinstanz das Verhalten der HCI zu Unrecht als
missbräuchlich qualifiziert habe. Schliesslich würde HCI seit dem 1. Januar 2017 auch den Upload
auf AIPS im Auftrag der Zulassungsinhaberinnen als separate Dienstleistung zum Preis von Fr. 30.-
anbieten. Seit dieser Änderung würden mit einer einzigen Ausnahme (P._______) alle Zulassungsinhaberinnen
diese Dienstleistung von HCI in Anspruch nehmen. Daneben gäbe es kleinere Zulassungsinhaberinnen,
die vereinzelt den Upload selber vornähmen. Zu Markteintritten sei es aber auch hier nicht gekommen.
Zudem habe es auch vorher schon einige Zulassungsinhaberinnen gegeben, welche den Upload auf AIPS selbst
hätten vornehmen wollen. Entsprechend sei auch in Bezug auf den Upload auf AIPS das Tatbestandselement
der Wettbewerbsbehinderung nicht erfüllt.
H.d.c Die
Vorinstanz nahm zur Eingabe der Beschwerdeführerinnen vom 16. November 2018 mit Schreiben vom 5.
Februar 2019 Stellung. Sie stellt sich auf den Standpunkt, die Eingabe der Beschwerdeführerinnen
sei als verspätetes, für den Verfahrensausgang nicht erhebliches Vorbringen im Interesse der
Verfahrensökonomie und des Beschleunigungsgebotes aus den Akten zu weisen. Es handle sich nicht
um neu hinzugekommene und bekanntzumachende Sachverhaltselemente. Die vorgebrachten Wirkungen lägen
ausserhalb des Untersuchungszeitraumes und würden nicht zum Streitgegenstand gehören. Darüber
hinaus könne aus einem späteren Verlauf unter anderen tatsächlichen Gegebenheiten keine
aussagekräftigen Schlüsse für frühere Perioden gezogen werden.
H.d.d Weiter
führt die Vorinstanz aus, für eine vergangenheitsbezogene Beurteilung gemäss Kartellgesetz
sei einzig wesentlich, welcher Wettbewerb im Zeitpunkt der missbräuchlichen Verhaltensweise möglich
gewesen wäre sowie dass tatsächlich Wettbewerbsbehinderungen vorlagen. Für die Beurteilung,
ob in der Vergangenheit Wettbewerb möglich gewesen wäre, sei der geltend gemachte Umstand,
die Anpassung des Verhaltens habe nicht zu einer Reaktion der anderen Unternehmen geführt, irrelevant.
Dies gelte insbesondere auch, weil sich vorliegend die heutige Wettbewerbssituation grundlegend von der
damaligen Wettbewerbssituation unterscheide.
H.d.e Mit
Eingabe vom 15. März 2019 nahmen die Beschwerdeführerinnen unaufgefordert zur Stellungnahme
der Vorinstanz vom 5. Februar 2019 Stellung und halten fest, mit den Darstellungen der Vorinstanz nicht
einverstanden zu sein.
H.d.f Der
Verfahrensantrag der Vorinstanz, die Eingabe der Beschwerdeführerinnen vom 16. November 2018 aus
den Akten zu weisen, wurde mit Zwischenverfügung vom 19. Februar 2019 abgewiesen.
H.d.g Mit
Eingabe vom 3. Mai 2019 erklärten die Beschwerdeführerinnen auf Nachfrage der Instruktionsrichterin,
auf die beantragte Durchführung einer öffentlichen Parteiverhandlung i.S.v. Art. 40 VGG zu
verzichten, da bereits ein mehrfacher Austausch über die rechtlichen Standpunkte stattgefunden habe.
An den gestellten Beweisanträgen halten die Beschwerdeführerinnen hingegen weiterhin explizit
fest.
VGG zu
verzichten, da bereits ein mehrfacher Austausch über die rechtlichen Standpunkte stattgefunden habe.
An den gestellten Beweisanträgen halten die Beschwerdeführerinnen hingegen weiterhin explizit
fest.
Das
Bundesverwaltungsgericht zieht in Erwägung:
1. Prozessvoraussetzungen
Ob die Prozessvoraussetzungen gegeben sind und auf eine Beschwerde einzutreten
ist, prüft das
Bundesverwaltungsgericht von Amtes wegen und mit freier Kognition (BVGE 2007/6 E. 1 m.w.H.).
1.1 Sachzuständigkeit
und Anfechtungsobjekt
1.1.1 Das
Bundesverwaltungsgericht beurteilt gemäss Art. 31 des Verwaltungsgerichtsgesetzes vom 17. Juni 2005
(VGG, SR
des Verwaltungsgerichtsgesetzes vom 17. Juni 2005
(VGG, SR 173.32) Beschwerden gegen Verfügungen nach Art. 5
173.32) Beschwerden gegen Verfügungen nach Art. 5 VwVG, welche von einer der in Art. 33
VwVG, welche von einer der in Art. 33 VGG aufgeführten Vorinstanzen erlassen wurden, soweit keine der in Art. 32
VGG aufgeführten Vorinstanzen erlassen wurden, soweit keine der in Art. 32 VGG genannten
Ausnahmen gegeben sind.
VGG genannten
Ausnahmen gegeben sind.
1.1.2 Die
Vorinstanz stellt eine eidgenössische Kommission im Sinne von Art. 33 Bst. f VGG dar (Art. 18
VGG dar (Art. 18 f.
KG, Art. 2 Abs. 3
f.
KG, Art. 2 Abs. 3 und Art. 57a
und Art. 57a Regierungs- und Verwaltungsorganisationsgesetz vom 21. März 1997
[RVOG, SR
Regierungs- und Verwaltungsorganisationsgesetz vom 21. März 1997
[RVOG, SR 172.010], Art. 7a
172.010], Art. 7a und Art. 8a
und Art. 8a Regierungs- und Verwaltungsorganisationsverordnung vom 25.
November 1998 [RVOV, SR
Regierungs- und Verwaltungsorganisationsverordnung vom 25.
November 1998 [RVOV, SR 172.010.01]).
172.010.01]).
1.1.3 Als
Verfügungen im Sinne von Art. 5 VwVG gelten Anordnungen von Behörden, welche gestützt
auf öffentliches Recht des Bundes entweder gegenüber dem Verfügungsadressaten dessen Rechte
und Pflichten begründen, inhaltlich bestimmen, ändern, aufheben oder feststellen oder ein entsprechendes
Begehren des Verfügungsadressaten abweisen oder darauf nicht eintreten.
VwVG gelten Anordnungen von Behörden, welche gestützt
auf öffentliches Recht des Bundes entweder gegenüber dem Verfügungsadressaten dessen Rechte
und Pflichten begründen, inhaltlich bestimmen, ändern, aufheben oder feststellen oder ein entsprechendes
Begehren des Verfügungsadressaten abweisen oder darauf nicht eintreten.
1.1.4 Die
Vorinstanz hat mit der Verfügung vom 19. Dezember 2016 gegenüber den Beschwerdeführerinnen
festgestellt, dass die Galenica mittels ihrer Tochtergesellschaft HCI auf zwei bestimmten Märkten
über eine marktbeherrschende Stellung im Sinne von Art. 4 Abs. 2 KG verfüge. Zudem hat sie
bestimmte Verhalten als gemäss Art. 49a Abs. 1
KG verfüge. Zudem hat sie
bestimmte Verhalten als gemäss Art. 49a Abs. 1 KG zu sanktionierende unzulässige Verhaltensweisen
nach Art. 7
KG zu sanktionierende unzulässige Verhaltensweisen
nach Art. 7 KG beurteilt und infolge dessen in Ziffer 2 und 3 des Dispositivs Massnahmen zur Beseitigung
der festgestellten unzulässigen Wettbewerbsbeschränkungen angeordnet. Die Vorinstanz belastete
die Beschwerdeführerinnen mit einer Verwaltungssanktion von Fr. 4'564'123.- unter
solidarischer Haftbarkeit. Weiter verpflichtete die Vorinstanz die Beschwerdeführerinnen Verfahrenskosten
von Fr. [...] zu bezahlen.
KG beurteilt und infolge dessen in Ziffer 2 und 3 des Dispositivs Massnahmen zur Beseitigung
der festgestellten unzulässigen Wettbewerbsbeschränkungen angeordnet. Die Vorinstanz belastete
die Beschwerdeführerinnen mit einer Verwaltungssanktion von Fr. 4'564'123.- unter
solidarischer Haftbarkeit. Weiter verpflichtete die Vorinstanz die Beschwerdeführerinnen Verfahrenskosten
von Fr. [...] zu bezahlen.
1.1.5 Dadurch
wurden die geschäftlichen Handlungsmöglichkeiten der Beschwerdeführerinnen eingeschränkt.
Die Vorinstanz hat den Beschwerdeführerinnen gestützt auf öffentliches Recht des Bundes,
hoheitlich, in verbindlicher und erzwingbarer Weise Pflichten auferlegt und somit im Sinne von Art. 5
Abs. 1 Bst. a VwVG verfügt.
VwVG verfügt.
1.1.6 Eine
Ausnahme gemäss Art. 32 VGG liegt nicht vor.
VGG liegt nicht vor.
1.1.7 Das
Bundesverwaltungsgericht ist daher für die Behandlung der vorliegenden Beschwerde sachlich zuständig.
1.2 Beschwerdelegitimation
und übrige Eintretensvoraussetzungen
1.2.1 Die
Beschwerdelegitimation setzt gemäss Art. 48 VwVG voraus, dass (i) der Beschwerdeführer am vorinstanzlichen
Verfahren teilgenommen hat bzw. ihm keine Möglichkeit zur Teilnahme eingeräumt wurde, er durch
die angefochtene Verfügung besonders berührt ist und ein schutzwürdiges Interesse an deren
Aufhebung hat, oder (ii) dass ein Bundesgesetz dem Beschwerdeführer dieses Recht ausdrücklich
einräumt.
VwVG voraus, dass (i) der Beschwerdeführer am vorinstanzlichen
Verfahren teilgenommen hat bzw. ihm keine Möglichkeit zur Teilnahme eingeräumt wurde, er durch
die angefochtene Verfügung besonders berührt ist und ein schutzwürdiges Interesse an deren
Aufhebung hat, oder (ii) dass ein Bundesgesetz dem Beschwerdeführer dieses Recht ausdrücklich
einräumt.
1.2.2 Die
Beschwerdeführerinnen haben als Parteien am vorinstanzlichen Untersuchungsverfahren teilgenommen
(Art. 48 Abs. 1 Bst. a VwVG). Als Verfügungsadressatinnen, deren Anträge im vorinstanzlichen
Verfahren zumindest teilweise abgewiesen wurden, sind sie durch die angefochtene Verfügung besonders
berührt. Zudem sind die Beschwerdeführerinnen durch die angefochtene Verfügung infolge
der Feststellung der marktbeherrschenden Stellung (Ziff. 1 des Dispositivs), der im Sinne von Art. 30
VwVG). Als Verfügungsadressatinnen, deren Anträge im vorinstanzlichen
Verfahren zumindest teilweise abgewiesen wurden, sind sie durch die angefochtene Verfügung besonders
berührt. Zudem sind die Beschwerdeführerinnen durch die angefochtene Verfügung infolge
der Feststellung der marktbeherrschenden Stellung (Ziff. 1 des Dispositivs), der im Sinne von Art. 30 KG angeordneten Massnahmen (Ziff. 2 und 3) sowie der Verpflichtung zur Bezahlung einer Verwaltungssanktion
(Ziff. 4) und von Verfahrenskosten (Ziff. 5) besonders berührt (Art. 48 Abs. 1 Bst. b
KG angeordneten Massnahmen (Ziff. 2 und 3) sowie der Verpflichtung zur Bezahlung einer Verwaltungssanktion
(Ziff. 4) und von Verfahrenskosten (Ziff. 5) besonders berührt (Art. 48 Abs. 1 Bst. b VwVG)
und haben ein als schutzwürdig anzuerkennendes Interesse an deren Aufhebung oder Änderung (Art. 48
Abs. 1 Bst. c
VwVG)
und haben ein als schutzwürdig anzuerkennendes Interesse an deren Aufhebung oder Änderung (Art. 48
Abs. 1 Bst. c VwVG). Die Beschwerdeführerinnen sind somit gestützt auf Art.
48 Abs. 1
VwVG). Die Beschwerdeführerinnen sind somit gestützt auf Art.
48 Abs. 1 VwVG zur Beschwerde legitimiert.
VwVG zur Beschwerde legitimiert.
1.2.3 Die
Beschwerdeführerinnen rügen mit der Beschwerde die unrichtige bzw. unvollständige Feststellung
des rechtserheblichen Sachverhalts, verschiedene Verletzungen von Bundesrecht sowie Unangemessenheit.
Bei diesen Rügen handelt es sich um zulässige Beschwerdegründe im Sinne von Art. 49 VwVG.
VwVG.
1.2.4 Die
gemäss Art. 50 VwVG zu beachtende Beschwerdefrist wurde unter Berücksichtigung des Fristenstillstandes
nach Art. 22a Abs. 1 Bst. a
VwVG zu beachtende Beschwerdefrist wurde unter Berücksichtigung des Fristenstillstandes
nach Art. 22a Abs. 1 Bst. a VwVG mit der Beschwerde vom 4. Mai 2017 gewahrt (Versanddatum der Verfügung:
20. März 2017). Zudem erfüllt die Beschwerdeschrift die gesetzlichen Anforderungen an Inhalt
und Form (Art. 52
VwVG mit der Beschwerde vom 4. Mai 2017 gewahrt (Versanddatum der Verfügung:
20. März 2017). Zudem erfüllt die Beschwerdeschrift die gesetzlichen Anforderungen an Inhalt
und Form (Art. 52 VwVG) und die Vertreter haben sich rechtsgenüglich ausgewiesen (Art. 11
VwVG) und die Vertreter haben sich rechtsgenüglich ausgewiesen (Art. 11 VwVG).
VwVG).
1.2.5 Der
Kostenverschluss wurde fristgemäss bezahlt (Art. 63 Abs. 4 VwVG). Die übrigen Sachurteilsvoraussetzungen
sind erfüllt. Auf die Beschwerde ist einzutreten.
VwVG). Die übrigen Sachurteilsvoraussetzungen
sind erfüllt. Auf die Beschwerde ist einzutreten.
2. Geltungsbereich
des Kartellgesetzes
Massgebend für die Beurteilung der streitigen Angelegenheit ist das Kartellgesetz. Dessen Anwendung
setzt voraus, dass der persönliche und sachliche Anwendungsbereich sowie der räumliche und
zeitliche Anwendungs- und Geltungsbereich gegeben sind.
2.1 Persönlicher
Geltungsbereich
2.1.1 Gemäss
Art. 2 Abs. 1 KG gilt das Kartellgesetz in persönlicher Hinsicht für Unternehmen
des privaten und des öffentlichen Rechts. Normadressaten des Kartellgesetzes sind somit "Unternehmen".
Als solche gelten gemäss der Legaldefinition von Art. 2 Abs. 1
KG gilt das Kartellgesetz in persönlicher Hinsicht für Unternehmen
des privaten und des öffentlichen Rechts. Normadressaten des Kartellgesetzes sind somit "Unternehmen".
Als solche gelten gemäss der Legaldefinition von Art. 2 Abs. 1 bis
KG sämtliche Nachfrager oder Anbieter von Gütern und Dienstleistungen im Wirtschaftsprozess,
unabhängig von ihrer Rechts- oder Organisationsform.
bis
KG sämtliche Nachfrager oder Anbieter von Gütern und Dienstleistungen im Wirtschaftsprozess,
unabhängig von ihrer Rechts- oder Organisationsform.
2.1.2 Über
den Wortlaut von Art. 2 Abs. 1 bis
KG hinaus muss ein Teilnehmer am Wirtschaftsprozess über wirtschaftliche Selbständigkeit verfügen,
um als Normadressat des Kartellgesetzes erfasst zu werden. Die wirtschaftliche Selbständigkeit stellt
eine konstitutive Voraussetzung des Unternehmensbegriffs dar. Das heisst, dass Gebilde, die sich nicht
autonom am Wirtschaftsprozess beteiligen, auch nicht als Unternehmen im Sinne des Kartellgesetzes zu
qualifizieren sind (Urteil des BVGer B-2977/2007 vom 27. April 2010, Publigroupe,
E. 8.2.2; Reto Heizmann/Michael Mayer, in: Zäch/Arnet/Baldi/Kiener/Schaller/Schraner/Spühler
[Hrsg.], DIKE-Kommentar KG, 2018, Art. 2 N 20 [nachfolgend zit.: {Autor}, DIKE-KG]).
Das Vorliegen von wirtschaftlicher Selbständigkeit setzt voraus, dass ein Teilnehmer am Wirtschaftsprozess
sein wirtschaftliches Verhalten ohne relevante Fremdeinwirkung eigenverantwortlich bestimmen kann (Marc
Amstutz/Ramin Silvan Gohari, in: Amstutz/Reinert [Hrsg.], Basler Kommentar zum Kartellgesetz,
2. Aufl., 2021, Art. 2 N 82 [nachfolgend zit.: {Autor}, BSK-KG]; Bernhard
Rubin/Matthias Courvoisier,
in: Baker & McKenzie, Handkommentar zum Kartellgesetz, 2007, Art. 2
bis
KG hinaus muss ein Teilnehmer am Wirtschaftsprozess über wirtschaftliche Selbständigkeit verfügen,
um als Normadressat des Kartellgesetzes erfasst zu werden. Die wirtschaftliche Selbständigkeit stellt
eine konstitutive Voraussetzung des Unternehmensbegriffs dar. Das heisst, dass Gebilde, die sich nicht
autonom am Wirtschaftsprozess beteiligen, auch nicht als Unternehmen im Sinne des Kartellgesetzes zu
qualifizieren sind (Urteil des BVGer B-2977/2007 vom 27. April 2010, Publigroupe,
E. 8.2.2; Reto Heizmann/Michael Mayer, in: Zäch/Arnet/Baldi/Kiener/Schaller/Schraner/Spühler
[Hrsg.], DIKE-Kommentar KG, 2018, Art. 2 N 20 [nachfolgend zit.: {Autor}, DIKE-KG]).
Das Vorliegen von wirtschaftlicher Selbständigkeit setzt voraus, dass ein Teilnehmer am Wirtschaftsprozess
sein wirtschaftliches Verhalten ohne relevante Fremdeinwirkung eigenverantwortlich bestimmen kann (Marc
Amstutz/Ramin Silvan Gohari, in: Amstutz/Reinert [Hrsg.], Basler Kommentar zum Kartellgesetz,
2. Aufl., 2021, Art. 2 N 82 [nachfolgend zit.: {Autor}, BSK-KG]; Bernhard
Rubin/Matthias Courvoisier,
in: Baker & McKenzie, Handkommentar zum Kartellgesetz, 2007, Art. 2 N 5 [nachfolgend zit.:
{Autor}, Handkommentar KG]; Rolf H. Weber/Stephanie Volz, Fachhandbuch Wettbewerbsrecht,
2013, Rz. 1.58). Grundsätzlich führt bereits die Einflussnahme auf strategische Angelegenheiten
zum Bestehen einer wirtschaftlichen Einheit im Sinne des kartellrechtlichen Unternehmensbegriffs. Die
Einflussnahme eines kontrollierenden Dritten auf den operativen und damit wettbewerbssensiblen Geschäftsbereich
ist hierfür nicht zwingende Voraussetzung (Urteil des BVGer B-8399/2010 vom 23. September 2014,
Baubeschläge Siegenia-Aubi, E. 2.7).
N 5 [nachfolgend zit.:
{Autor}, Handkommentar KG]; Rolf H. Weber/Stephanie Volz, Fachhandbuch Wettbewerbsrecht,
2013, Rz. 1.58). Grundsätzlich führt bereits die Einflussnahme auf strategische Angelegenheiten
zum Bestehen einer wirtschaftlichen Einheit im Sinne des kartellrechtlichen Unternehmensbegriffs. Die
Einflussnahme eines kontrollierenden Dritten auf den operativen und damit wettbewerbssensiblen Geschäftsbereich
ist hierfür nicht zwingende Voraussetzung (Urteil des BVGer B-8399/2010 vom 23. September 2014,
Baubeschläge Siegenia-Aubi, E. 2.7).
2.1.3 Der
persönliche Geltungsbereich ist demnach an den Unternehmensbegriff geknüpft. In casu stellt
sich die Frage des Unternehmensbegriffs insbesondere im Kontext eines Konzernsachverhalts. Ein
Konzern stellt einen besonderen Gesellschaftsverbund dar, der im weitesten Sinne auf einer Zusammenfassung
verschiedener, rechtlich selbständiger Organisationseinheiten zu einer eigenständigen wirtschaftlichen
Einheit unter einer übergeordneten Gruppenführung beruht (Urteil des BVGer
B-831/2011
vom 18. Dezember 2018, SIX, E. 39).
2.1.4 Bei
Konzernen stellen die rechtlich selbstständigen Konzerngesellschaften mangels wirtschaftlicher
Selbstständigkeit keine Unternehmen im Sinne von Art. 2 Abs. 1 bis
KG dar. Als Unternehmen gilt in solchen Fällen der Konzern als Ganzes, nicht eine bestimmte Gruppengesellschaft
(Urteil des BGer 2C_484/2010 vom 29. Juni 2012, Publigroupe, E.
3 [in BGE 139 I 72 nicht publiziert]; Urteile des BVGer B-7633/2009 vom 14. September 2015, ADSL
II, E. 29; B-581/2012 vom 16. September 2016, Nikon, E. 4.1.3;
B-2977/2007, Publigroupe, E. 4.1; Ralf
Michael Straub, Der Konzern als Kartellrechtssubjekt, in: Festschrift für Anton K. Schnyder
zum 65. Geburtstag, 2018, S. 1269 ff., S. 1278 ff.; Heizmann/Mayer,
DIKE-KG, Art. 2 N 31; Jürg Borer,
Wettbewerbsrecht I, Schweizerisches Kartellgesetz, 3. Aufl. 2011, Art. 2 Rz. 11).
bis
KG dar. Als Unternehmen gilt in solchen Fällen der Konzern als Ganzes, nicht eine bestimmte Gruppengesellschaft
(Urteil des BGer 2C_484/2010 vom 29. Juni 2012, Publigroupe, E.
3 [in BGE 139 I 72 nicht publiziert]; Urteile des BVGer B-7633/2009 vom 14. September 2015, ADSL
II, E. 29; B-581/2012 vom 16. September 2016, Nikon, E. 4.1.3;
B-2977/2007, Publigroupe, E. 4.1; Ralf
Michael Straub, Der Konzern als Kartellrechtssubjekt, in: Festschrift für Anton K. Schnyder
zum 65. Geburtstag, 2018, S. 1269 ff., S. 1278 ff.; Heizmann/Mayer,
DIKE-KG, Art. 2 N 31; Jürg Borer,
Wettbewerbsrecht I, Schweizerisches Kartellgesetz, 3. Aufl. 2011, Art. 2 Rz. 11).
2.1.5 Die
Vorinstanz erwog, Galenica und HCI (sowie auch Documed und e-mediat bis 2016) seien rechtlich selbständige,
im Wirtschaftsprozess als Nachfragerinnen und Nachfrager oder Anbieterinnen und Anbieter von Gütern
und/oder Dienstleistungen auftretende Gesellschaften (gewesen). Documed und e-mediat seien insbesondere
bei den Offerten für die neuen Verträge mit den Zulassungsinhaberinnen ab 2013 offiziell gemeinsam
aufgetreten, womit das fragliche Verhalten entweder ihnen gemeinsam respektive HCI als Managementgesellschaft
der beiden oder Documed einer- und e-mediat andererseits zugeordnet werden könne. Infolge des Fusionsvertrags
per 1. Januar 2016 habe HCI den Geschäftsbetrieb von Documed und e-mediat übernommen. Von ihnen
sei das zu beurteilende Verhalten ausgegangen. Weiter sei denkbar, dass sie in die Gesamtstrategie des
Galenica-Konzerns eingebettet gewesen seien und unter der Leitung der Konzernmutter stünden. Die
in jüngster Zeit vorgenommenen verschiedenen Umstrukturierungen im Konzern liessen darauf schliessen,
dass Galenica als Muttergesellschaft nicht nur die Möglichkeit der Einflussnahme habe, sondern diese
zumindest teilweise auch wahrnehme. Als kartellrechtliches Unternehmenssubjekt werde deshalb die Gesamtheit
aller zusammengefassten Gesellschaften und somit der Konzern als Ganzes erfasst.
2.1.6 Diese
Erwägungen der Vorinstanz sind nicht zu beanstanden. Die Vorinstanz hat aufgrund der vorliegenden
Umstände zu Recht darauf geschlossen, die ehemalige Galenica-Gruppe als Ganzes als das massgebliche
Unternehmen im Sinne von Art. 2 Abs. 1 bis
KG zu betrachten. Das Vorliegen einer wirtschaftlichen Organisationseinheit der ehemaligen Galenica-Gruppe
im Sinne des kartellrechtlichen Unternehmensbegriffs wird von den Beschwerdeführerinnen auch nicht
in Frage gestellt. Im Übrigen gibt auch der Wechsel der Muttergesellschaft im Jahr 2017 keinen Anlass,
den persönlichen Geltungsbereich anders zu beurteilen (vgl. dazu E. 3.18),
dieser wird jedoch bei der Prüfung der kartellrechtlichen Massnahmen in E. 14
zu berücksichtigen sein.
bis
KG zu betrachten. Das Vorliegen einer wirtschaftlichen Organisationseinheit der ehemaligen Galenica-Gruppe
im Sinne des kartellrechtlichen Unternehmensbegriffs wird von den Beschwerdeführerinnen auch nicht
in Frage gestellt. Im Übrigen gibt auch der Wechsel der Muttergesellschaft im Jahr 2017 keinen Anlass,
den persönlichen Geltungsbereich anders zu beurteilen (vgl. dazu E. 3.18),
dieser wird jedoch bei der Prüfung der kartellrechtlichen Massnahmen in E. 14
zu berücksichtigen sein.
2.1.7 Während
der persönliche Geltungsbereich des Kartellgesetzes somit im vorstehenden Sinne bejaht werden kann,
sind die Verfügungsadressaten und damit die Sanktionssubjekte erst in einem weiteren Schritt zu
bestimmen (s. unten E. 3),
da auch im Anwendungsbereich des schweizerischen Kartellrechts Verfügungsadressat nur sein kann,
wer selbst Subjekt mit Rechtspersönlichkeit und somit Träger von Rechten und Pflichten ist
(Urteile B-8399/2010, Baubeschläge Siegenia-Aubi, E. 2.8;
B-7633/2009, ADSL II,
E. 65 ff.). Dem Konzern kommt im Kartellverfahren mangels
eigener Rechtspersönlichkeit praxisgemäss keine Parteistellung zu (Urteile
B-7633/2009,
ADSL II, E. 68 ff.; B-581/2012, Nikon,
E. 4.1.4; B-2977/2007, Publigroupe, E. 4.1 ff.).
2.2 Sachlicher
Geltungsbereich des Kartellgesetzes
2.2.1
Massgebliche
Wettbewerbsbeschränkung
2.2.1.1 In
sachlicher Hinsicht ist das Kartellgesetz anwendbar, wenn Unternehmen gemäss Art. 2 Abs. 1 KG
Kartell- oder andere Wettbewerbsabreden treffen, Marktmacht ausüben oder sich an Unternehmenszusammenschlüssen
beteiligen (Urteil des BVGer B-506/2010 vom 19. Dezember 2013, Gaba,
E. 3.2.1).
KG
Kartell- oder andere Wettbewerbsabreden treffen, Marktmacht ausüben oder sich an Unternehmenszusammenschlüssen
beteiligen (Urteil des BVGer B-506/2010 vom 19. Dezember 2013, Gaba,
E. 3.2.1).
2.2.1.2 Im
vorliegenden Fall ist die Variante von Ausübung von Marktmacht von Bedeutung. Mit dieser Variante
werden die Fälle einer unzulässigen Ausübung von wirtschaftlicher Stärke durch einen
Marktteilnehmer mittels bestimmter verpönter Verhaltensweisen angesprochen. Das Kartellgesetz kennt
keine Legaldefinition der Marktmacht. Der Begriff findet sich auch nicht in Art. 7 KG, der den materiellen
Tatbestand einer unzulässigen Ausübung von wirtschaftlicher Stärke statuiert. Diese Vorschrift
stellt nicht auf eine Ausübung von Marktmacht, sondern auf das Merkmal eines marktbeherrschenden
Unternehmens ab, was durch Art. 4 Abs. 2
KG, der den materiellen
Tatbestand einer unzulässigen Ausübung von wirtschaftlicher Stärke statuiert. Diese Vorschrift
stellt nicht auf eine Ausübung von Marktmacht, sondern auf das Merkmal eines marktbeherrschenden
Unternehmens ab, was durch Art. 4 Abs. 2 KG inhaltlich spezifiziert wird. Es wird angenommen, dass Marktmacht
zwischen normalem Markteinfluss, den fast jedes Unternehmen erreichen kann, und Marktbeherrschung gemäss
Art. 4 Abs. 2
KG inhaltlich spezifiziert wird. Es wird angenommen, dass Marktmacht
zwischen normalem Markteinfluss, den fast jedes Unternehmen erreichen kann, und Marktbeherrschung gemäss
Art. 4 Abs. 2 KG, die nur Unternehmen mit einer gewissen Machstellung zukommt, einzuordnen sei (Heizmann/Mayer,
DIKE-KG, Art. 2 N 50 m.w.H.).
KG, die nur Unternehmen mit einer gewissen Machstellung zukommt, einzuordnen sei (Heizmann/Mayer,
DIKE-KG, Art. 2 N 50 m.w.H.).
2.2.1.3 Das
vorliegende Kartellverfahren und die angefochtene Verfügung beziehen sich namentlich auf die angeblich
ungerechtfertigte Einschränkung des Absatzes der Konkurrenten sowie auf die angeblich ungerechtfertigte
Koppelung von Bedingungen an den Abschluss von Verträgen durch ein Unternehmen mit einer besonderen
Marktstellung und damit auf eine angeblich unzulässige Ausübung von Marktmacht.
2.2.2
Vorbehaltene
Vorschriften
2.2.2.1 Gemäss
Art. 3 Abs. 1 KG sind dem Kartellgesetz Vorschriften vorbehalten, soweit sie auf einem Markt für
bestimmte Waren oder Leistungen Wettbewerb nicht zulassen, insbesondere Vorschriften, die eine staatliche
Markt- oder Preisordnung begründen, und solche, die einzelne Unternehmen zur Erfüllung öffentlicher
Aufgaben mit besonderen Rechten ausstatten. Ebenso nicht unter das Gesetz fallen Wettbewerbswirkungen,
die sich ausschliesslich aus der Gesetzgebung über das geistige Eigentum ergeben. Hingegen unterliegen
Einfuhrbeschränkungen, die sich auf Rechte des geistigen Eigentums stützen, der Beurteilung
nach dem Kartellgesetz (Art. 3 Abs. 2
KG sind dem Kartellgesetz Vorschriften vorbehalten, soweit sie auf einem Markt für
bestimmte Waren oder Leistungen Wettbewerb nicht zulassen, insbesondere Vorschriften, die eine staatliche
Markt- oder Preisordnung begründen, und solche, die einzelne Unternehmen zur Erfüllung öffentlicher
Aufgaben mit besonderen Rechten ausstatten. Ebenso nicht unter das Gesetz fallen Wettbewerbswirkungen,
die sich ausschliesslich aus der Gesetzgebung über das geistige Eigentum ergeben. Hingegen unterliegen
Einfuhrbeschränkungen, die sich auf Rechte des geistigen Eigentums stützen, der Beurteilung
nach dem Kartellgesetz (Art. 3 Abs. 2 KG).
KG).
2.2.2.2 Dem
Vorbehalt von Art. 3 Abs. 1 KG ist gemäss der Rechtsprechung des Bundesgerichts in den Entscheiden
in Sachen Hors-Liste Medikamente (Publikumspreisempfehlungen betreffend
Cialis, Levitra und Viagra) nur in restriktiver Weise Geltung zu verschaffen. Ein Ausschluss des
Kartellgesetzes ist gemäss dieser Rechtsprechung nur gestützt auf eine klare gesetzliche Grundlage
möglich, die ein wettbewerbsbehinderndes Verhalten verordnet oder zulässt (Urteile des BGer
2C.75/2014; 2C.77/2014; 2C.79/2014 und 2C.80/2014, Hors-Liste Medikamente,
vom 28. Januar 2015 je E. 2.2.3 m.H. auf BGE 129 II 497 E.3.3.3). Weiter behält Art. 3 Abs. 1
KG ist gemäss der Rechtsprechung des Bundesgerichts in den Entscheiden
in Sachen Hors-Liste Medikamente (Publikumspreisempfehlungen betreffend
Cialis, Levitra und Viagra) nur in restriktiver Weise Geltung zu verschaffen. Ein Ausschluss des
Kartellgesetzes ist gemäss dieser Rechtsprechung nur gestützt auf eine klare gesetzliche Grundlage
möglich, die ein wettbewerbsbehinderndes Verhalten verordnet oder zulässt (Urteile des BGer
2C.75/2014; 2C.77/2014; 2C.79/2014 und 2C.80/2014, Hors-Liste Medikamente,
vom 28. Januar 2015 je E. 2.2.3 m.H. auf BGE 129 II 497 E.3.3.3). Weiter behält Art. 3 Abs. 1 KG
gemäss dieser Rechtsprechung nur Normen vor, welche den gleichen Sachverhalt unter den gleichen
Gesichtspunkten unterschiedlich beurteilen, wenn also eine Normkollision vorliegt. Normen, welche demgegenüber
einen Sachverhalt nach unterschiedlichen Gesichtspunkten regeln, gelangen nebeneinander zur Anwendung
und schliessen sich nicht gegenseitig aus (Urteile 2C.75/2014; 2C.77/2014; 2C.79/2014 und 2C.80/2014,
Hors-Liste Medikamente, je E. 2.4.1 m.H. auf BGE 137 II 199, Terminierung
Mobilfunk, E. 3.4 und Urteil des BGer 2A.142/2003 vom 5. September 2003 E. 4.1.3).
KG
gemäss dieser Rechtsprechung nur Normen vor, welche den gleichen Sachverhalt unter den gleichen
Gesichtspunkten unterschiedlich beurteilen, wenn also eine Normkollision vorliegt. Normen, welche demgegenüber
einen Sachverhalt nach unterschiedlichen Gesichtspunkten regeln, gelangen nebeneinander zur Anwendung
und schliessen sich nicht gegenseitig aus (Urteile 2C.75/2014; 2C.77/2014; 2C.79/2014 und 2C.80/2014,
Hors-Liste Medikamente, je E. 2.4.1 m.H. auf BGE 137 II 199, Terminierung
Mobilfunk, E. 3.4 und Urteil des BGer 2A.142/2003 vom 5. September 2003 E. 4.1.3).
2.2.2.3 Die
Bestimmungen bezüglich der Arzneimittelinformationen im Heilmittelgesetz und der Arzneimittel-Verordnung
(Art. 11 Abs. 1 Bst. f und Abs. 3 sowie Art. 16 HMG, Art. 14 f. AMZV) begründen keinen
Vorbehalt i.S.v. Art. 3 Abs. 1
f. AMZV) begründen keinen
Vorbehalt i.S.v. Art. 3 Abs. 1 KG. Ebenso verhält es sich bei den Weisungen von Swissmedic, gemäss
welchen die Zulassungsinhaberinnen die Arzneimittelinformationen auf AIPS publizieren müssen. Denn
vorliegend geht es nicht um die Publikation auf AIPS, sondern um die Kommerzialisierung der Arzneimittelinformationen.
Letzteres wird durch diese Bestimmungen nicht geregelt. Auch die Prüf- und Sorgfaltspflichten im
Umgang mit Arzneimittel auf Stufe der Leistungserbringerinnen und -erbringer (Art. 3 und 26 HMG) begründen
betreffend Kommerzialisierung von Medikamenteninformationen keinen Vorbehalt i.S.v. Art. 3 Abs. 1
KG. Ebenso verhält es sich bei den Weisungen von Swissmedic, gemäss
welchen die Zulassungsinhaberinnen die Arzneimittelinformationen auf AIPS publizieren müssen. Denn
vorliegend geht es nicht um die Publikation auf AIPS, sondern um die Kommerzialisierung der Arzneimittelinformationen.
Letzteres wird durch diese Bestimmungen nicht geregelt. Auch die Prüf- und Sorgfaltspflichten im
Umgang mit Arzneimittel auf Stufe der Leistungserbringerinnen und -erbringer (Art. 3 und 26 HMG) begründen
betreffend Kommerzialisierung von Medikamenteninformationen keinen Vorbehalt i.S.v. Art. 3 Abs. 1 KG.
Denn diese betreffen nicht die Publikation der Arzneimittelinformationen als solche oder eine nachgelagerte
Kommerzialisierung dieser Daten.
KG.
Denn diese betreffen nicht die Publikation der Arzneimittelinformationen als solche oder eine nachgelagerte
Kommerzialisierung dieser Daten.
2.2.2.4 Zudem
ist kein Urheberrechtsschutz der Beschwerdeführerinnen an den Daten der INDEX-Datenbanken dargetan,
weshalb eine Prüfung des Verhältnisses zwischen dem Bundesgesetz über das Urheberrecht
und verwandte Schutzrechte vom 9. Oktober 1992 (Urheberrechtsgesetz, URG, SR 231.1) und dem Kartellgesetz
unterbleiben kann. Überdies unbestritten ist, dass auch kein Schutz durch andere Immaterialgüterrechte
besteht (Art. 3 Abs. 2
231.1) und dem Kartellgesetz
unterbleiben kann. Überdies unbestritten ist, dass auch kein Schutz durch andere Immaterialgüterrechte
besteht (Art. 3 Abs. 2 KG, s. unten E. 12.6.17).
KG, s. unten E. 12.6.17).
2.2.2.5 Insgesamt
ist damit mit der Vorinstanz festzustellen, dass in den hier zu beurteilenden Märkten keine Vorschriften
ersichtlich sind, die einen Vorbehalt gemäss Art. 3 KG begründen können. Ein solcher wurde
im Übrigen von den Beschwerdeführerinnen auch nicht geltend gemacht.
2.2.2.6 Der
sachliche Anwendungsbereich des Kartellgesetzes ist somit gegeben. Im Rahmen der rechtlichen Prüfung
ist zu beurteilen, ob die Beschwerdeführerinnen Marktmacht im Sinne von Art. 2 Abs. 1 KG
ausgeübt haben. Die Anwendung des Kartellgesetzes ist nicht aufgrund eines ausdrücklichen Vorbehalts
zu Gunsten sonstiger Vorschriften oder des Grundsatzes der lex specialis ausgeschlossen.
KG
ausgeübt haben. Die Anwendung des Kartellgesetzes ist nicht aufgrund eines ausdrücklichen Vorbehalts
zu Gunsten sonstiger Vorschriften oder des Grundsatzes der lex specialis ausgeschlossen.
2.2.3
Exkurs:
Revision des Heilmittelgesetzes
2.2.3.1 Der
Bundesrat hat am 7. November 2012 die Botschaft zur Änderung des Heilmittelgesetzes an das Parlament
überwiesen (Botschaft zur Änderung des Heilmittelgesetzes vom 7. November 2012, [BBl 2013 1]).
National- und Ständerat haben die Vorlage in der Folge beraten und das revidierte Heilmittelgesetz
in der Schlussabstimmung am 18. März 2016 verabschiedet (BBl 2016 1953). Die Referendumsfrist ist
am 7. Juli 2016 unbenutzt abgelaufen (AS 2017 2745).
2.2.3.2 Von
der Revision betroffen ist auch Art. 67 HMG. Dessen verabschiedete Absätze 3-9 lauten wie folgt:
3 Die Zulassungsinhaberinnen, die Vertreterinnen und Vertreter
der interessierten Medizinalberufe, die Personen mit einer eigenverantwortlichen Abgabekompetenz nach
Artikel 25 sowie die Patientinnen und Patienten oder deren Verbände führen gemeinsam eine Einrichtung
in Form einer Stiftung, welche ein elektronisches Verzeichnis mit den gesetzlich vorgeschriebenen Inhalten
der Arzneimittelinformationen im Human- und Veterinärbereich betreibt.
4 Die Einrichtung veröffentlicht im elektronischen Verzeichnis
nach Absatz 3 den Inhalt der Arzneimittelinformationen der Zulassungsinhaberinnen vollständig und
aktuell in geeigneter und strukturierter Form auf deren Kosten. Ein einfaches Verzeichnis mit den vollständigen
und aktuellen Arzneimittelinformationen ist für alle öffentlich und kostenlos zugänglich.
5 Die Zulassungsinhaberinnen liefern der Einrichtung die gesetzlich
vorgeschriebenen Inhalte der Arzneimittelinformationen in der dafür vorgesehenen Form. Kommen die
Zulassungsinhaberinnen dieser Pflicht nicht nach, so erstellt die Einrichtung die Strukturierung auf
deren Kosten.
6 Die Einrichtung legt unter Einbezug des Instituts und der
Personen mit der Kompetenz zur eigenverantwortlichen Abgabe nach Artikel 25 die Anforderungen an Umfang
und Struktur der Daten nach Absatz 4 und deren Lieferung nach Absatz 5 fest. Sie berücksichtigt
dafür soweit möglich die einschlägigen internationalen Standards.
7 Die zuständigen Bundesstellen können über den
Verzeichnisdienst weitere behördlich veröffentlichte Informationen zugänglich machen.
8 Kommt die Einrichtung ihrer Aufgabe nicht nach, veröffentlicht
das Institut die gesetzlich vorgeschriebenen Inhalte der Arzneimittelinformationen auf Kosten der Zulassungsinhaberinnen
in Form eines elektronischen Verzeichnisses. Das Institut kann die Erstellung und den Betrieb des Verzeichnisses
an Dritte übertragen.
9 Das Institut veröffentlicht, sobald es ein Gesuch um
Zulassung eines Arzneimittels erhalten hat, die Indikation, die Wirkstoffe dieses Arzneimittels sowie
Name und Adresse des Gesuchstellers, sofern der Veröffentlichung keine schützenswerten Geheimhaltungsinteressen
entgegenstehen.
2.2.3.3 Der
Entwurf des Bundesrates sah die Absatze 3-9 des Art. 67
nHMG noch nicht vor, sondern
schlug in Art. 67 Abs. 1bis E-HMG was folgt
vor (BBl 2013 131, 143 f.):
Das Institut kann die Fach- und Patienteninformationen (Arzneimittelinformationen)
auf Kosten der
Zulassungsinhaberinnen in Form eines elektronischen Verzeichnisses veröffentlichen. Es überträgt
die Erstellung und den Betrieb des Verzeichnisses an Dritte.
2.2.3.4 Die
revidierten Bestimmungen sind per 1. Januar 2019 in Kraft getreten. Zufolge Art. 67 Abs. 3 nHMG ist die
Stiftung Refdata seit 1. Januar 2019 mit der Publikation der Fach- und Publikumsinformation bezüglich
Human- und Tierarzneimitteln betraut. Refdata löst damit Swissmedic von ihrer bisherigen Verantwortung
ab. Es ist nun Aufgabe der Stiftung Refdata sicherzustellen, dass die Zulassungsinhaberinnen über
eine Publikationsplattform verfügen, mit der sie ihre diesbezüglichen Pflichten kostengünstig
erfüllen kann. Die Stiftung Refdata hat die bisherigen Partner mit dem Betrieb der Publikationsplattformen
für Human- und Tierarzneimittel beauftragt: für Humanarzneimittel HCI und für Tierarzneimittel
die Veterinärpharmakologie und -toxikologie, Vetsuisse Fakultät, in Zürich (www.refdata.ch/de/faq
und https://www.refdata.ch/de/kontakt [abgerufen am 24.08.2020]).
nHMG ist die
Stiftung Refdata seit 1. Januar 2019 mit der Publikation der Fach- und Publikumsinformation bezüglich
Human- und Tierarzneimitteln betraut. Refdata löst damit Swissmedic von ihrer bisherigen Verantwortung
ab. Es ist nun Aufgabe der Stiftung Refdata sicherzustellen, dass die Zulassungsinhaberinnen über
eine Publikationsplattform verfügen, mit der sie ihre diesbezüglichen Pflichten kostengünstig
erfüllen kann. Die Stiftung Refdata hat die bisherigen Partner mit dem Betrieb der Publikationsplattformen
für Human- und Tierarzneimittel beauftragt: für Humanarzneimittel HCI und für Tierarzneimittel
die Veterinärpharmakologie und -toxikologie, Vetsuisse Fakultät, in Zürich (www.refdata.ch/de/faq
und https://www.refdata.ch/de/kontakt [abgerufen am 24.08.2020]).
2.3 Räumlicher
Geltungsbereich
2.3.1 Das
Kartellgesetz beansprucht Geltung auf dem Hoheitsgebiet der Schweiz und findet gemäss dem in Art. 2 Abs. 2
KG ausdrücklich statuierten Auswirkungsprinzip auf alle Sachverhalte Anwendung, die sich in der
Schweiz auswirken. Dies gilt selbst dann, wenn sie im Ausland veranlasst wurden.
2.3.2 Vorliegend
beziehen sich sowohl das zu untersuchende Verhalten als auch die sich daraus ergebenden Folgen auf die
Schweiz. Der räumliche Geltungs- und Anwendungsbereich des Kartellgesetzes ist demzufolge gegeben.
2.4 Zeitlicher
Geltungsbereich
2.4.1 Das
Kartellgesetz trat am 1. Juli 1996 in Kraft, wobei zwischenzeitlich verschiedene Gesetzesänderungen
vorgenommen wurden. Art. 49a KG, der die Rechtsgrundlage einer Sanktionierung der Beschwerdeführerinnen
bildet, wurde durch das Bundesgesetz vom 20. Juni 2003 in das Kartellgesetz eingefügt und trat am
1. April 2004 in Kraft.
KG, der die Rechtsgrundlage einer Sanktionierung der Beschwerdeführerinnen
bildet, wurde durch das Bundesgesetz vom 20. Juni 2003 in das Kartellgesetz eingefügt und trat am
1. April 2004 in Kraft.
2.4.2 Die
vorliegend zu beurteilenden Verhaltensweisen der Beschwerdeführerinnen begannen frühestens
im September 2012. Der zeitliche Geltungsbereich des Kartellgesetzes ist damit gegeben.
3. Rechtmässige
Verfügungsadressaten
3.1 Die
Vorinstanz erwog, die ehemalige Galenica-Gruppe könne nicht Verfügungsadressatin sein, da sie
als Konzern gemäss schweizerischem Recht kein Rechtssubjekt sei. Es sei deshalb sachgerecht, neben
den direkt involvierten Tochtergesellschaften Documed, e-mediat und HCI aufgrund der konzernmässigen
Verbundenheit der Gesellschaften auch die Konzernmutter Galenica als Verfügungsadressatin zu behandeln.
Zu beachten sei ferner, dass Documed und e-mediat auf den 1. Januar 2016 in HCI fusioniert worden seien
und rechtlich nur noch HCI bestehe.
3.2 Die
Beschwerdeführerinnen bringen vor, aufgrund der Umstrukturierungen der Galenica-Gruppe (s. oben
E. B.a)
bestehe heute kein konzernmässiges Verhältnis zwischen HCI und Galenica mehr. Bereits zum Zeitpunkt
der Eröffnung der angefochtenen Verfügung sei HCI keine Tochtergesellschaft der Galenica mehr
gewesen. Die Beschwerdeinstanz habe ihren Entscheid auf denjenigen Sachverhalt zu stützen, der im
Zeitpunkt ihres Entscheides massgebend sei. Die Beschwerdeführerin 1 sei nicht mehr die Muttergesellschaft
der Beschwerdeführerin 2. Die heutige Galenica-Gruppe und die heutige Vifor-Pharma-Gruppe seien
je selbständige, börsenkotierte Konzerne, wobei erstere hauptsächlich im Vertrieb und
Verkauf von Arzneimitteln in der Schweiz tätig sei und zweitere international ausgerichtet sei und
Eisenpräparate herstelle. Es mache daher keinen Sinn, die Beschwerdeführerin 1 zu einer Sanktion
zu verurteilen, die nichts mit ihrer Geschäftstätigkeit zu tun habe, und ihr Verhaltensvorschriften
aufzuerlegen, welche keinen Zusammenhang zu ihr aufweisen würden. Ebenfalls sinnlos sei eine Marktbeherrschungsfeststellung
der Beschwerdeführerin 1.
3.3 Die
Vorinstanz hielt hierzu in ihrer Vernehmlassung fest, aus dem Sacheinlagevertrag sei zwar ersichtlich,
dass HCI auf die am 13. Februar 2017 gegründete Galenica Santé, unterdessen wiederum firmierend
unter Galenica AG, übertragen worden sei. Aber aus kartellrechtlicher Sicht habe sich zu diesem
Zeitpunkt nichts geändert, da die Galenica Santé zum Zeitpunkt der Gründung eine 100%ige
Tochtergesellschaft der damaligen Galenica, heute firmierend unter Vifor Pharma AG, gewesen sei. Gemäss
[...] habe die Sacheinlegerin, das heisse die Beschwerdeführerin 1, als Gegenleistung für
die Sacheinlage 50'000'000 Namenaktien, mithin 100% der Aktien erhalten. Es handle sich beim
Sacheinlagevertrag vom 13. Februar 2017 somit um eine konzerninterne Restrukturierung, die keinen Einfluss
auf die Kontrollmöglichkeiten der Beschwerdeführerin 1 über die Beschwerdeführerin
2 gehabt habe. Erst am 7. April 2016 seien 97,5% der Aktien der Galenica Santé, mittlerweile wieder
firmierend unter Galenica AG, an der Börse veräussert worden. Seit diesem Zeitpunkt könne
die Beschwerdeführerin 1 keine Kontrolle mehr über die Galenica Santé ausüben.
3.4
Verfügungsadressat kann im Anwendungsbereich des schweizerischen Kartellrechts grundsätzlich
nur sein, wer selbst Subjekt mit Rechtspersönlichkeit und somit Träger von Rechten und Pflichten
ist. Ein Konzern stellt in Hinblick auf eine Teilnahme am Verfahren als Partei sowie den Erlass von kartellrechtlichen
Verfügungen kein taugliches Rechtssubjekt dar, weil er selbst nicht Träger von Rechten und
Pflichten sein kann. Bei Konzernsachverhalten fallen demzufolge das massgebliche Verfahrenssubjekt als
Beurteilungsobjekt und der Verfügungsadressat als Partei eines Kartellverfahrens zwangsläufig
auseinander (Urteile B-831/2011, SIX, E. 121; B-7633/2009,
ADSL II, E. 68). Entsprechend sind einer nicht rechtsfähigen Gruppe mehrerer Gesellschaften
oder einem Konzern aufzuerlegende Kartellrechtssanktionen den massgeblichen rechtsfähigen Rechtssubjekten
innerhalb der gegebenen wirtschaftlichen Strukturen zuzuweisen. Verfügungsadressaten können
nur einzelne rechtlich selbständige Gruppengesellschaften sein bzw. nur an diese können Sanktionen
gerichtet werden (Urteile des BVGer B-771/2012 vom 25. Juni 2018, Cellere,
E 9.5.1;
B-581/2012, Nikon, E. 4.1.4 und
8.2.6; B-7633/2009, ADSL II, E. 67 f.;
B-8399/2010,
Baubeschläge Siegenia-Aubi,
E. 2.8; Heinemann,
Konzerne als Adressaten des Kartellrechts, in: Hochreutener/Stoffel/Amstutz [Hrsg.], Wettbewerbsrecht:
Jüngste Entwicklungen in der Rechtsprechung, Konzernsachverhalte und Konzernbegriff aus kartellrechtlicher
Sicht, 2015, S. 49 und 53).
3.5 Hinsichtlich
der konkreten Zuweisung einer Sanktion an die rechtsfähigen Rechtssubjekte innerhalb des Unternehmens
hat das Bundesgericht im Urteil 2C_484/2010 i.S. Publigroupe festgehalten,
es sei grundsätzlich nicht zu beanstanden, wenn die Sanktion für den von Tochtergesellschaften
der Unternehmenseinheit begangenen Kartellrechtsverstoss der Muttergesellschaft als hierfür verantwortliches
Rechtssubjekt auferlegt werde. Gemäss den Erwägungen des Bundesgerichts dürfen die Anforderungen
an die strafrechtliche Zuordnung kartellrechtlich verpönten Verhaltens an juristische Personen,
die eine Organisationseinheit bilden, nicht überzogen werden (vgl. Urteile 2C_484/2010, Publigroupe,
E. 3.4 [nicht publizierte Erwägung in BGE 139 I 72]; B-771/2012, Cellere,
E. 9.5.2).
3.6 Diese
Rechtsprechung führte das Bundesverwaltungsgericht dahingehend weiter, als es für die rechtmässige
Heranziehung von Rechtssubjekten als Verfügungsadressaten einerseits fordert, dass die Vorinstanz
das ihr diesbezüglich zukommende Ermessen im Einzelfall pflichtgemäss ausübt. Andererseits
hat das Bundesverwaltungsgericht gefolgert, dass es in der Regel sachgerecht sein dürfte, neben
der Obergesellschaft, von der die übergeordnete Leitungsmacht ausgeht, auch diejenigen Gruppengesellschaften
als Verfügungsadressatinnen heranzuziehen, welche an dem relevanten Wettbewerbsverhalten beteiligt
waren. Die alleinige Heranziehung der Muttergesellschaft ist grundsätzlich nicht ausreichend, wobei
es im Einzelfall aus Gründen der Prozessökonomie aber auch genügen kann, nur eine Gruppengesellschaft
in die Pflicht zu nehmen. Dies etwa, wenn die handelnde Konzerngesellschaft in der Schweiz domiziliert
ist, die Obergesellschaft und alle weiteren beteiligten Konzerngesellschaften aber einen Sitz im Ausland
aufweisen (Urteil B-7633/2009, ADSL II, E. 72 ff.) Daran
anknüpfend bestätigte das Bundesverwaltungsgericht im Urteil
B-581/2012
i.S. Nikon die (einzig) einer schweizerischen Konzernniederlassung
auferlegte Kartellsanktion; dies unter anderem mit dem Hinweis, dass eine Tochtergesellschaft selbst
gegenüber Sachverhalten, welche von der Mutter- oder einer Schwestergesellschaft veranlasst werden,
nicht ohne Weiteres unter Berufung auf die eigene Rechtspersönlichkeit einwenden kann, es handle
sich um fremdes Verhalten (Urteil B-581/2012, Nikon, E. 4.1.5 und 8.2.6).
3.7 Vorliegend
hat die Vorinstanz die kartellrechtliche Verfügung zum einen an die Beschwerdeführerin 1 als
Obergesellschaft der ehemaligen Galenica-Gruppe und ehemaligen Muttergesellschaft der Beschwerdeführerin
2 sowie an die Beschwerdeführerin 2 als Gruppengesellschaft, welche am relevanten Wettbewerbsverhalten
beteiligt war, gerichtet.
3.8 Dass
die Beschwerdeführerin 2 nicht als Verfügungsadressatin zu betrachten wäre, wird weder
geltend gemacht, noch sind hierfür nach dem Gesagten Gründe ersichtlich. Documed und e-mediat
wurden per 1. Januar 2016 in die Beschwerdeführerin 2 fusioniert. Entsprechend besteht rechtlich
nur noch letztere und diese hat sich unbestrittenermassen die Verhaltensweisen von Documed und e-mediat
anrechnen zu lassen.
3.9 Was
die vorinstanzliche Auswahl der Beschwerdeführerin 1 als Verfügungsadressatin betrifft, sind
die bis zur Verfügungseröffnung erfolgten Umstrukturierungen zu berücksichtigen. Die angefochtene
Verfügung ist mit Begleitschreiben vom 20. März 2017 am 21. März 2017 bei den Beschwerdeführerinnen
eingegangen. Die Beschwerdeführerin 2 wurde am 13. Februar 2017 auf die gleichentags gegründete
Galenica Santé, unterdessen wiederum firmierend unter Galenica AG, übertragen. Wie die Vorinstanz
aber zutreffend vorbrachte, war die Galenica Santé zum Zeitpunkt ihrer Gründung und auch zum
Zeitpunkt der Eröffnung der angefochtenen Verfügung eine 100%ige Tochtergesellschaft der Beschwerdeführerin
1. Denn aus [...] geht hervor, dass die Beschwerdeführerin 1 als Gegenleistung für die
Sacheinlage 50'000'000 Namenaktien, mithin 100% der Aktien erhält. Bis zur Veräusserung
der Aktien der Galenica Santé am 7. April 2017 lag lediglich eine konzerninterne Re-strukturierung
vor. Die Beschwerdeführerin 1 verfügte nach wie vor über die Kontrollmöglichkeiten
über die Beschwerdeführerin 2 und stellte nach wie vor die Obergesellschaft der ehemaligen
Galenica-Gruppe dar. Die Beschwerdeführerin 2 kann zum Zeitpunkt der Eröffnung der vorinstanzlichen
Verfügung als Enkelgesellschaft der Beschwerdeführerin 1 bezeichnet werden. Im Ergebnis ist
die vorinstanzliche Auswahl an Verfügungsadressatin aus damaliger Sicht somit nicht zu beanstanden.
3.10 Aus
heutiger Sicht gilt allerdings zu beachten, dass am 7. April 2017 97,5% der Aktien der Galenica Santé,
mittlerweile wieder firmierend unter Galenica AG, an der Börse veräussert wurden. Gemäss
Medienmitteilung der Galenica-Gruppe vom 7. April 2017 werde die Gruppe künftig keine Aktien mehr
von Galenica Santé halten. Der verbleibende Aktienanteil von 2,5% werde für den Aktienumtausch
für bezugsberechtigte Mitarbeitende von Galenica Santé reserviert. Die Beschwerdeführerin
1 kann somit seither keine Kontrolle mehr über die Galenica Santé (neue Galenica) und damit
über die Beschwerdeführerin 2 ausüben. Die Beschwerdeführerin 2 gehört nicht
mehr demselben Konzern wie die Beschwerdeführerin 1 an.
3.11 Es
stellt sich somit die Frage, was diese Umstrukturierung für die heutige Festlegung der rechtmässigen
Verfügungsadressaten bedeutet. In der europäischen Union hat sich im Zusammenhang mit solchen
Umstrukturierungen zunächst das Konzept der wirtschaftlichen Kontinuität entwickelt. Sowohl
im Fall Zucker (Urteil des EuGH vom 16. Dezember 1975 C-40/73
Suiker Unie et. al./Kommission,
Slg. 1975 S. 1663) als auch im Fall Rheinzink (Urteil des EuGH
vom 28. März 1984 C-29/83 Rheinzink/Kommission, Slg. 1984
S. 1679) gelangte der EuGH zum Ergebnis, dass das neue Unternehmen als wirtschaftlicher Nachfolger
des "Täterunternehmens" anzusehen sei. Die Verantwortlichkeit für Wettbewerbsverstösse
folgte der übertragenen Geschäftstätigkeit, ohne dass die Frage des Fortbestehens des
Rechtsträgers des Täterunternehmens eine Rolle gespielt hätte. Die Geldbusse wurde gegen
denjenigen Unternehmensträger verhängt, der zum Zeitpunkt des Entscheids Eigentümer des
sich seinerzeit wettbewerbswidrig verhaltenden Geschäftsbereichs war (Anna
Antonia Skoczylas, Verantwortlichkeit für kartellrechtliche Verstösse im Konzern, 2011,
S. 90; Damian K. Graf, Zurechnung von Unternehmensbussen,
in: Gesellschafts- und Kapitalmarktrecht, GesKR 2015, S. 356, 364 f.).
3.12 Diese
Praxis wurde später modifiziert und die Kommission führte den Grundsatz ein, dass solange die
Rechtspersönlichkeit des Täterunternehmens fortbestehe, zunächst einmal derjenige Unternehmensträger
für eine Zuwiderhandlung einzustehen habe, welcher das fragliche Unternehmen geleitet habe, als
die Zuwiderhandlung geschehen sei (Entscheidung 86/398/EWG der Kommission vom 23. April 1986 betreffend
ein Verfahren nach Artikel 85 des EWG-Vertrags, COMP/IV/31.149 Polypropylen,
Abl. 230/1 Rn. 96; Skoczylas, a.a.O., S. 91). Der EuGH
bestätigte diese Praxismodifikation und stellte fest, dass das Kriterium der wirtschaftlichen Kontinuität
"nur dann" zum Zuge kommen könne, wenn der Unternehmensträger, dem das sich wettbewerbsrechtswidrig
verhaltende Unternehmen im Zeitpunkt des Verstosses zuzuordnen gewesen sei, aufgehört habe, rechtlich
zu existieren. Solange der Rechtsträger des Täterunternehmens weiter existiere, bestehe kein
Bedürfnis, den Erwerber für etwas zu sanktionieren, was er nicht begangen habe (Urteil des
EuGH vom 8. Juli 1999 C-49/92 P Anic Partecipazioni SpA/Kommission,
Slg. 1999 I-4162 Rn. 78 und 145; vgl. auch GA Kokott, Schlussanträge vom 3. Juli 2007, Slg. 2007
I-10896 Rn. 78, betreffend: Urteil des EuGH vom 11. Dezember 2007 C-280/06 ETI/Kommission,
Slg. 2007 I-10925; Skoczylas, a.a.O., S. 91; Graf,
a.a.O., S. 364 f.). Dieses Prinzip gilt im EU-Wettbewerbsrecht bis heute (Skoczylas,
a.a.O., S. 91 m.w.H.).
3.13 Die
Schweizerische Lehre und Rechtsprechung hat sich bisher nur wenig mit der Kartellbussenzurechnung bzw.
den rechtmässigen Verfügungsadressaten nach erfolgter Umstrukturierungen auseinandergesetzt.
Im Urteil B-771/2012 vom 25. Juni 2018 i.S. Cellere hatte das
Bundesverwaltungsgericht den Fall zu beurteilen, wonach während hängigem Beschwerdeverfahren
die Aktiven und Passiven der Tochtergesellschaft infolge Fusion auf eine andere Gruppengesellschaft übergegangen
sind und in der Folge die Muttergesellschaft (Beschwerdeführerin 2) der Beschwerdeführerin
1 im Handelsregister gelöscht wurde. Das Bundesverwaltungsgericht kam zum Schluss, dass anstelle
der weggefallenen Muttergesellschaft (ehemalige Beschwerdeführerin 2) für sämtliche erwiesenen
Abredebeteiligungen der (ehemaligen) Beschwerdeführerin 2 deren rechtsfähige Rechtsnachfolgerin
und Gruppengesellschaft als Sanktionsadressatin heranzuziehen sei. Zur Begründung wurde im Wesentlichen
festgehalten, dass es sich offensichtlich um eine Umstrukturierung innerhalb der "Gruppe" handle.
Die Übernahme der Aktiven und Passiven der ehemaligen Beschwerdeführerin 2 sei in voller Kenntnis
der gegenüber der übernommenen Gruppengesellschaft ausgesprochenen Sanktion erfolgt. Es könne
nicht angehen, dass die Gruppe, welche die fraglichen Kartellrechtsverstösse zu verantworten habe,
mit der Liquidierung einer Gruppengesellschaft die Durchsetzung der Sanktionsforderung vereitele, welche
im Zeitpunkt der unternehmensinternen Umstrukturierung eine bekannte (über Rückstellungen abzusichernde)
Passivposition der übernommenen Gruppengesellschaft dargestellt habe (Urteil B-771/2012, Cellere,
E. 9.5.5 f.).
3.14 Im
Urteil B-831/2011 vom 18. Dezember 2018 i.S. SIX erachtete das
Bundesverwaltungsgericht die dortige Beschwerdeführerin 1 als sachgerechte Verfügungsadressatin.
Die dortige Beschwerdeführerin 1 als Konzernobergesellschaft war erst nach den zur Last gelegten
Verhaltensweisen durch den Zusammenschluss der SIX-Gruppe entstanden. Sie wurde zudem erst relativ spät
im Untersuchungsverfahren in das Verfahren miteinbezogen, hatte aber die Möglichkeit, die durch
den Eintritt in die Parteistellung vermittelten Verfahrensrechte bis zum Abschluss des Kartellverwaltungsverfahrens
in sachgerechter Weise auszuüben (Urteil
B-831/2011, SIX,
E. 132 ff.).
3.15 Tagmann/Zirlick
vertreten die Auffassung, grundsätzlich sei und bleibe ein verantwortliches Unternehmen so
lange haftbar, als es als juristische Person existiere. Existiere sie infolge Übernahme nicht mehr,
sei die Busse dem Rechtsnachfolger aufzuerlegen. Ob der Veräusserer oder der Erwerber oder beide
in anteilsmässiger Aufteilung die Sanktion zu tragen haben, wenn das haftbare Unternehmen lediglich
den Geschäftsteil, von dem die Zuwiderhandlung ausgegangen sei, veräussere, lassen sie hingegen
offen (Tagmann/Zirlick, BSK-KG, Art. 49a N 100).
3.16 Skoczylas
verweist auf Tagmann/Zirlick und hält ebenfalls fest, bei Umstrukturierungen sei ein verantwortliches
Unternehmen in der Regel so lange haftbar, wie es als juristische Person existiere. Gehe es infolge Fusion
in einem anderen Unternehmen auf, sei eine allfällige Geldbusse diesem aufzuerlegen. Veräussere
ein herrschendes Unternehmen seine gesamte operative Tätigkeit und werde es dadurch zu einer reinen
Holdinggesellschaft, solle entsprechend der Praxis der EU der Erwerber des betreffenden Betriebsteils
zur Verantwortung gezogen werden (Skoczylas, a.a.O., S.
135 m.H. auf S. 92 f.).
3.17 Graf
vertritt schliesslich die Auffassung, solange der Veräusserer noch existiere, habe in jedem Fall
dieser die kartellstrafrechtlichen Konsequenzen zu tragen. Eine Sanktionierung des Erwerbers falle in
jedem Fall ausser Betracht, selbst wenn er das gesamte operative Geschäft des delinquierenden Veräusserers
übernommen habe oder der kriminelle Unternehmensträger durch Umstrukturierung untergegangen
sei (Graf, a.a.O., S. 364 f.).
3.18 Vorliegend
existiert mit der Beschwerdeführerin 1 die im Zeitpunkt der Zuwiderhandlung für den Betrieb
des Täterunternehmens HCI verantwortliche juristische Person fort. Entsprechend scheint es sachgerecht,
analog dem vorerwähnten Prinzip des EU-Wettbewerbsrechts neben der Beschwerdeführerin 2 die
Beschwerdeführerin 1 als Verfügungs- und Sanktionsadressatin heranzuziehen. Dies entspricht
auch dem in der Schweizerischen Literatur vertretenen Grundsatz, dass ein verantwortliches Unternehmen
so lange haftbar bleibt, als es als juristische Person existiert.
3.19 Zur
Rüge der Beschwerdeführerinnen, es mache keinen Sinn, die Beschwerdeführerin 1 zu einer
Sanktion zu verurteilen, die nichts mit ihrer Geschäftstätigkeit zu tun habe, ist festzuhalten,
dass es nicht angehen kann, dass die Durchsetzung einer allfälligen Sanktion, mit solchen Umstrukturierungen
vereitelt oder erschwert wird. Dies hat im Übrigen unabhängig davon zu gelten, ob die Umstrukturierung
- wie von den Beschwerdeführerinnen vorgebracht - in keinem Zusammenhang mit dem laufenden
Verfahren steht und Teil einer übergeordneten Strategie ist oder ob eine solche Umstrukturierung
gerade im Zusammenhang mit einer kartellrechtlichen Untersuchung und einer drohenden Sanktionierung an
die Hand genommen wird. Insofern vermag dieses Vorbringen nicht überzeugen.
3.20 Auf
das Vorbringen der Beschwerdeführerinnen, die Marktbeherrschungsfeststellung im Dispositiv mache
betreffend die Beschwerdeführerin 1 aufgrund der erfolgten Umstrukturierungen keinen Sinn mehr,
wird unter E. 10
einzugehen sein. Auf das Vorbringen, es sei sinnlos, der Beschwerdeführerin 1 Verhaltensweisen aufzuerlegen,
die keinen Zusammenhang zur ihr aufweisen würden, wird in E. 14
zurückgekommen.
4. Rechtmässigkeit
des vorinstanzlichen Verfahrens
4.1 Die
Beschwerdeführerinnen rügen hinsichtlich verschiedener Aspekte, die Vorinstanz habe den Sachverhalt
unvollständig ermittelt. Damit machen sie implizit eine Verletzung des Untersuchungsgrundsatzes
geltend.
4.2 So
bringen sie insbesondere vor, die Vorinstanz habe bei der Beurteilung der Markstellung betreffend die
Marktgegenseite der Leistungserbringer, Vertriebsunternehmen und Softwarehäuser keine Befragung
der Leistungserbringerinnen und -erbringer durchgeführt, obwohl eine solche wesentlich gewesen wäre,
um die Position der HCI richtig zu erfassen. Die Vorinstanz habe weiter Inhalt und Bedeutung der angeblich
gekoppelten Dienstleistung (Qualitätssicherung und Upload) nicht untersucht. Auch habe es die Vorinstanz
unterlassen die Leistungserbringerinnen und -erbringer zu ihren Qualitätsanforderungen an die Datenbanken
zu befragen. Ebenfalls unterlassen habe die Vorinstanz die Zulassungsinhaberinnen zu befragen, ob sie
die Dienstleistung des Uploads separat nachfragen würden und die Behinderungswirkungen der Koppelung
anhand von Fragebogen oder Befragungen zu überprüfen.
4.3 Weiter
rügen die Beschwerdeführerinnen, die Vorinstanz habe verschiedene Aspekte unzureichend begründet
bzw. die von ihr vorgebrachten entlastenden Argumente zwar in der Verfügung erwähnt, sich inhaltlich
aber nicht damit auseinandergesetzt (vgl. Beschwerde, insb. Rz. 92, 122, 152, 167, 176 f., 183, 185,
192, 194, 233). Damit machen die Beschwerdeführerinnen eine Verletzung der Begründungspflicht
geltend.
4.4
Schliesslich machen die Beschwerdeführerinnen geltend, die Vorinstanz habe den Grundsatz
in dubio pro reo verletzt (vgl. Beschwerde Rz. 6). Aufgrund der ungenügenden Abklärung
des Sachverhalts durch die Vorinstanz sei dieser gemäss der aus der Unschuldsvermutung resultierenden
Beweiswürdigungsregel "in dubio pro
reo" zugunsten der betroffenen Parteien darzustellen.
Zudem scheine die Vorinstanz in der gesamten Sanktionsbegründung implizit davon auszugehen, dass
den Verhaltensweisen, welche nicht als unzulässig qualifiziert worden seien, gleichwohl ein Unrechtsgehalt
beiliege, der bei der Sanktionsbemessung zu berücksichtigen sei.
4.5 Die
Vorinstanz entgegnet, die Vorwürfe der Beschwerdeführerinnen seien unbegründet. Sie habe
dem Untersuchungsgrundsatz sowie dem erforderlichen Beweismass genügt.
4.6 Sowohl
im Kartellverwaltungsverfahren als auch im Beschwerdeverfahren vor dem Bundesverwaltungsgericht ist gemäss
Art. 12 VwVG i.V.m. Art. 39 KG bzw. Art. 37
KG bzw. Art. 37 VGG der Sachverhalt von Amtes
wegen zu untersuchen (Untersuchungsgrundsatz). Im Rahmen des Untersuchungsgrundsatzes sind von der Vorinstanz
die rechtserheblichen Tatsachen abzuklären, also jene faktischen Entscheidgrundlagen, die für
die Regelung des in Frage stehenden Rechtsverhältnisses relevant sind. Die behördliche Untersuchungspflicht
wird ergänzt durch die Mitwirkungspflichten der Parteien nach Art. 13
VGG der Sachverhalt von Amtes
wegen zu untersuchen (Untersuchungsgrundsatz). Im Rahmen des Untersuchungsgrundsatzes sind von der Vorinstanz
die rechtserheblichen Tatsachen abzuklären, also jene faktischen Entscheidgrundlagen, die für
die Regelung des in Frage stehenden Rechtsverhältnisses relevant sind. Die behördliche Untersuchungspflicht
wird ergänzt durch die Mitwirkungspflichten der Parteien nach Art. 13 VwVG (BGE 143 II 425
E. 5.1; 129 II 18, Buchpreisbindung, E. 7.1; Urteil des BGer 2A.430/2006
vom 6. Februar 2007, Sammelrevers, E. 10.2; Urteile des BVGer
B-771/2012, Cellere, E.6.4.1; B-5685/2012 vom 17. Dezember 2015,
Altimum, E. 4.5.1; B-7633/2009,
ADSL II, E. 185 ff.,
B-8430/2010 vom 23. September 2014, Baubeschläge Koch,
E. 5.1.1;
VwVG (BGE 143 II 425
E. 5.1; 129 II 18, Buchpreisbindung, E. 7.1; Urteil des BGer 2A.430/2006
vom 6. Februar 2007, Sammelrevers, E. 10.2; Urteile des BVGer
B-771/2012, Cellere, E.6.4.1; B-5685/2012 vom 17. Dezember 2015,
Altimum, E. 4.5.1; B-7633/2009,
ADSL II, E. 185 ff.,
B-8430/2010 vom 23. September 2014, Baubeschläge Koch,
E. 5.1.1;
B-8399/2010, Baubeschläge
Siegenia-Aubi, E. 4.1.1; B-8404/2010 vom 23. September
2014, Baubeschläge SFS unimarket, E. 3.2.4; Krauskopf/Emmenegger/Babey,
in: Waldmann/Weissenberger, Praxiskommentar zum Bundesgesetz über das Verwaltungsverfahren, 2. Aufl.
2016 [nachfolgend zit.: [Autor], Praxiskommentar VwVG], Art. 12 N 22 und 88).
4.7 Nach
Art. 33 Abs. 1 VwVG nimmt die Behörde die ihr angebotenen Beweise ab, wenn diese
zur Abklärung des Sachverhalts tauglich erscheinen. Hierfür massgebliches Kriterium ist, ob
das Beweismittel geeignet ist, den rechtserheblichen Sachverhalt zu erhellen. In diesem Sinne müssen
angebotene Beweise nicht abgenommen werden, wenn sie eine für die rechtliche Beurteilung unerhebliche
Frage betreffen (BGE 144 II 194, BMW, E. 4.4.2; antizipierte
Beweiswürdigung).
VwVG nimmt die Behörde die ihr angebotenen Beweise ab, wenn diese
zur Abklärung des Sachverhalts tauglich erscheinen. Hierfür massgebliches Kriterium ist, ob
das Beweismittel geeignet ist, den rechtserheblichen Sachverhalt zu erhellen. In diesem Sinne müssen
angebotene Beweise nicht abgenommen werden, wenn sie eine für die rechtliche Beurteilung unerhebliche
Frage betreffen (BGE 144 II 194, BMW, E. 4.4.2; antizipierte
Beweiswürdigung).
4.8 Den
in Art. 49a KG vorgesehenen direkten Sanktionen kommt ein strafrechtsähnlicher Charakter zu
(BGE 143 II 297, Gaba, E. 9.1; 139 I 72, Publigroupe,
E. 2.2.2). Die Qualifizierung hat zur Folge, dass im kartellrechtlichen Sanktionsverfahren die verfassungs-
und EMRK-rechtlichen Garantien grundsätzlich zu beachten sind, welche auch für das Strafverfahren
gelten (BGE 139 I 72, Publigroupe, E. 2.2.2). Allerdings zählt das Kartell-sanktionsverfahren
primär zum Verwaltungsrecht (Urteil des BGer 2C_1065/2014 vom 26. Mai 2016, Publikation
Sanktionsverfügung in Sachen Nikon, E. 8.2 [nicht publizierte Erwägung in BGE 142
II 268]), weshalb die Verfahrensgarantien der Konvention vom 4. November 1950 zum Schutze der Menschenrechte
und Grundfreiheiten (EMRK, SR
KG vorgesehenen direkten Sanktionen kommt ein strafrechtsähnlicher Charakter zu
(BGE 143 II 297, Gaba, E. 9.1; 139 I 72, Publigroupe,
E. 2.2.2). Die Qualifizierung hat zur Folge, dass im kartellrechtlichen Sanktionsverfahren die verfassungs-
und EMRK-rechtlichen Garantien grundsätzlich zu beachten sind, welche auch für das Strafverfahren
gelten (BGE 139 I 72, Publigroupe, E. 2.2.2). Allerdings zählt das Kartell-sanktionsverfahren
primär zum Verwaltungsrecht (Urteil des BGer 2C_1065/2014 vom 26. Mai 2016, Publikation
Sanktionsverfügung in Sachen Nikon, E. 8.2 [nicht publizierte Erwägung in BGE 142
II 268]), weshalb die Verfahrensgarantien der Konvention vom 4. November 1950 zum Schutze der Menschenrechte
und Grundfreiheiten (EMRK, SR 0.101) nicht in voller Strenge zur Anwendung gelangen und im Übrigen
nicht absolute Geltung beanspruchen, sondern in eine einzelfallbezogene Interessenabwägung einzubeziehen
sind (BGE 140 II 384, Spielbank, E. 3.3.5 m.w.H.; Urteil
des Europäischen Gerichtshofs für Menschenrechte (EGMR) Jussila
gegen Finnland vom 23. November 2006, 73053/01 Ziff. 43; vgl. Urteile
0.101) nicht in voller Strenge zur Anwendung gelangen und im Übrigen
nicht absolute Geltung beanspruchen, sondern in eine einzelfallbezogene Interessenabwägung einzubeziehen
sind (BGE 140 II 384, Spielbank, E. 3.3.5 m.w.H.; Urteil
des Europäischen Gerichtshofs für Menschenrechte (EGMR) Jussila
gegen Finnland vom 23. November 2006, 73053/01 Ziff. 43; vgl. Urteile
B-581/2012,
Nikon, E. 5.1 und 8.1.1; B-7633/2009,
ADSL II, E. 651).
4.9 Zur
angerufenen Begründungspflicht ist festzuhalten, dass der verfassungsmässige Anspruch auf rechtliches
Gehör gemäss Art. 29 Abs. 2 BV das Recht des Betroffenen, sich vor Erlass eines in seine Rechtsstellung
eingreifenden Akts zur Sache äussern zu können, umfasst (BGE 136 I 184 E. 2.2.1; 122 II 274
E. 6b). Er verlangt von der Behörde, dass sie seine Vorbringen tatsächlich hört, ernsthaft
prüft und in ihrer Entscheidfindung angemessen berücksichtigt (BGE 136 I 184 E. 2.2.1; 123 I 31
E. 2c). Die Begründung muss so abgefasst sein, dass der Betroffene den Entscheid gegebenenfalls
sachgerecht anfechten kann. Sie muss kurz die wesentlichen Überlegungen nennen, von denen sich das
Gericht hat leiten lassen und auf die es seinen Entscheid stützt. Nicht erforderlich ist, dass sich
die Begründung mit allen Parteistandpunkten einlässlich auseinandersetzt und jedes einzelne
Vorbringen ausdrücklich widerlegt (BGE 136 I 184 E. 2.2.1; 133 III 439 E. 3.3). Sie kann sich
vielmehr auf die für den Entscheid wesentlichen Gesichtspunkte beschränken (BGE 141 V 557 E.
3.2; 134 I 83 E. 4.1).
BV das Recht des Betroffenen, sich vor Erlass eines in seine Rechtsstellung
eingreifenden Akts zur Sache äussern zu können, umfasst (BGE 136 I 184 E. 2.2.1; 122 II 274
E. 6b). Er verlangt von der Behörde, dass sie seine Vorbringen tatsächlich hört, ernsthaft
prüft und in ihrer Entscheidfindung angemessen berücksichtigt (BGE 136 I 184 E. 2.2.1; 123 I 31
E. 2c). Die Begründung muss so abgefasst sein, dass der Betroffene den Entscheid gegebenenfalls
sachgerecht anfechten kann. Sie muss kurz die wesentlichen Überlegungen nennen, von denen sich das
Gericht hat leiten lassen und auf die es seinen Entscheid stützt. Nicht erforderlich ist, dass sich
die Begründung mit allen Parteistandpunkten einlässlich auseinandersetzt und jedes einzelne
Vorbringen ausdrücklich widerlegt (BGE 136 I 184 E. 2.2.1; 133 III 439 E. 3.3). Sie kann sich
vielmehr auf die für den Entscheid wesentlichen Gesichtspunkte beschränken (BGE 141 V 557 E.
3.2; 134 I 83 E. 4.1).
4.10 Der
Anspruch auf rechtliches Gehör ist formeller Natur, womit seine Verletzung ungeachtet der materiellen
Begründetheit des Rechtsmittels zur Gutheissung der Beschwerde und zur Aufhebung des angefochtenen
Entscheides führt (BGE 135 I 187 E. 2.2; 125 I 113 E. 3; 122 II 464 E. 4a). Nach der Rechtsprechung
ist die Heilung einer - nicht besonders schwerwiegenden - Gehörsverletzung aber ausnahmsweise
dann möglich, wenn die betroffene Person die Möglichkeit erhält, sich vor einer Beschwerdeinstanz
zu äussern, die sowohl den Sachverhalt wie die Rechtslage frei überprüfen kann (BGE 133
I 201 E. 2.2, m.H. auf BGE 127 V 431 E. 3d/aa).
4.11 Die
von den Beschwerdeführerinnen angerufene Unschuldsvermutung ist in der Verfassung in Art. 32
Abs. 1 BV und im Strafprozessrecht in Art. 10 Abs. 1
BV und im Strafprozessrecht in Art. 10 Abs. 1 der Schweizerischen Strafprozessordnung
vom 5. Oktober 2007 (StPO, SR
der Schweizerischen Strafprozessordnung
vom 5. Oktober 2007 (StPO, SR 312.0) verankert. Danach gilt jede Person bis zur rechtskräftigen
Verurteilung als unschuldig. Die EMRK verbrieft die Unschuldsvermutung in Art. 6 Ziff. 2. Die Unschuldsvermutung
hat Auswirkungen auf die Verteilung der Beweislast sowie auf das Beweismass (BGE 139 I 72, Publigroupe,
E. 8.3; Urteile B-581/2012, Nikon, E. 5.5.1;
B-8399/2010, Baubeschläge Siegenia-Aubi, E. 6.4.4;
Esther Tophinke, in: Niggli/Heer/Wiprächtiger,
Basler Kommentar zur Schweizerischen Strafprozessordung/Jugendstrafprozessordung, Art. 1- 195, 2. Aufl.,
2014, Art. 10 N 79). Als Beweislastregel besagt die Unschuldsvermutung, dass es Sache der Behörde
ist, die Schuld zu beweisen. Als Beweismassregel folgt daraus, dass das Gericht eine Tatsache nur als
gegeben voraussetzen darf, wenn es an deren Vorhandensein keine unüberwindlichen Zweifel hegt; andernfalls
hat das Gericht von dem für den Beschuldigten günstigeren Sachverhalt auszugehen (Art. 10
Abs. 3
312.0) verankert. Danach gilt jede Person bis zur rechtskräftigen
Verurteilung als unschuldig. Die EMRK verbrieft die Unschuldsvermutung in Art. 6 Ziff. 2. Die Unschuldsvermutung
hat Auswirkungen auf die Verteilung der Beweislast sowie auf das Beweismass (BGE 139 I 72, Publigroupe,
E. 8.3; Urteile B-581/2012, Nikon, E. 5.5.1;
B-8399/2010, Baubeschläge Siegenia-Aubi, E. 6.4.4;
Esther Tophinke, in: Niggli/Heer/Wiprächtiger,
Basler Kommentar zur Schweizerischen Strafprozessordung/Jugendstrafprozessordung, Art. 1- 195, 2. Aufl.,
2014, Art. 10 N 79). Als Beweislastregel besagt die Unschuldsvermutung, dass es Sache der Behörde
ist, die Schuld zu beweisen. Als Beweismassregel folgt daraus, dass das Gericht eine Tatsache nur als
gegeben voraussetzen darf, wenn es an deren Vorhandensein keine unüberwindlichen Zweifel hegt; andernfalls
hat das Gericht von dem für den Beschuldigten günstigeren Sachverhalt auszugehen (Art. 10
Abs. 3 StPO).
StPO).
Die Unschuldsvermutung gilt grundsätzlich auch im Verwaltungssanktionsverfahren (BGE 105 Ib
117 E. 1.a; Kiener/Rütsche/Kuhn,
Öffentliches Verfahrensrecht, 2. Aufl. 2015, Rz. 728; Kölz/Häner/Bertschi,
Verwaltungsverfahren und Verwaltungsrechtspflege des Bundes, 3. Aufl. 2013,
Rz. 486). Allerdings gilt sie (auch) im Kartellverfahren
nicht absolut, und zwar unbesehen des Umstands, dass die strafrechtlichen Verfahrensgarantien im Verwaltungssanktionsverfahren
nicht in voller Schärfe zur Anwendung gelangen (BGE 140 II 384, Spielbank,
E. 3.3.4 f.). Es ist mithin im Einzelfall ein sachverhaltsbezogener Ausgleich zu finden. Unzulässig
wäre eine Beweislastumkehr zulasten des Unternehmens, gegen welches sich die Untersuchung richtet
(Urteil B-581/2012, Nikon, E. 5.5.2 f.).
4.12 Die
Vorbringen der Beschwerdeführerinnen zur angeblichen Verletzung des Untersuchungsgrundsatzes, der
Begründungspflicht und der Unschuldsvermutung haben einen engen Bezug zum Inhalt der angefochtenen
Verfügung. Hinweise auf eine Rechtsverletzung der Vorinstanz im formellen Sinn sind nicht ersichtlich.
Denn die Vorinstanz hat nicht nur ihre Pflicht zur Feststellung des Sachverhalts von Amtes wegen, sondern
auch ihre Beweisführungslast sowie das zu erfüllende Beweismass zu jedem Zeitpunkt ausdrücklich
anerkannt. Der Vorinstanz kann auch nicht vorgeworfen werden, eine unzulässige Beweislastumkehr
zulasten der Beschwerdeführerinnen praktiziert zu haben.
4.13
Die Rügen der Beschwerdeführerinnen, die Vorinstanz habe ihre Vorbringen nicht berücksichtigt
oder sich nicht objektiv und ernsthaft mit ihnen befasst, beschlagen in der Hauptsache die rechtliche
Würdigung der Sache durch die Vorinstanz. Diese mag zu einem anderen als dem von den Beschwerdeführerinnen
beantragten Ergebnis geführt haben. Die Rechtmässigkeit dieser abweichenden Rechtsauffassung
stellt jedoch keine Frage des Gehörsanspruchs dar. Vielmehr geht es dabei um die im Folgenden zu
behandelnden materiellen Fragen.
4.14
Im Übrigen kommt dem Bundesverwaltungsgericht als Beschwerdeinstanz in kartellrechtlichen
Sanktionsverfahren eine vollständige Entscheidungsgewalt mit umfassender Prüfungszuständigkeit
zu, weshalb es über die gleiche Kognition in Rechts- und Sachverhaltsfragen wie die Vorinstanz verfügt.
Die Beschwerdeführerinnen konnten im Beschwerdeverfahren denn auch sämtliche Aspekte einbringen,
mit denen sie eine Verletzung ihres Anspruchs auf rechtliches Gehör durch die Vorinstanz gerügt
haben. Ein allfällig bestehender Verfahrensmangel wäre demnach durch die im Rahmen des Beschwerdeverfahrens
erfolgte Möglichkeit zur umfassenden Stellungnahme ohnehin geheilt worden.
4.15
Im Einzelnen werden die Vorbringen der Beschwerdeführerinnen im Rahmen der materiellen Beurteilung,
d.h. nicht in einem separaten Abschnitt unter dem Gesichtspunkt eines formellen Rechtsfehlers, zu prüfen
sein (vgl. in diesem Sinne bereits die BVGE 2011/32, Terminierung Mobilfunk,
E. 1.1.2; Urteile B-8430/2010 und B-8404/2010, Baubeschläge
Koch und SFS unimarket, E. 3.2.1 bzw.
E. 3.2.5; B-581/2012, Nikon, E. 5.5; B-771/2012,
Cellere, E. 5.3; B-831/2011, SIX,
E. 206).
5. Erforderliches
Beweismass
5.1 Für
die Prüfung der Beweislage entscheidend ist die Frage, welches Beweismass erfüllt sein muss,
um einen rechtserheblichen Sachumstand als bewiesen erachten zu können.
5.2 Als
Regelbeweismass qualifiziert die Praxis grundsätzlich den Überzeugungsbeweis (vgl. Urteile
B-7633/2009, ADSL II, E. 155 ff.; B-771/2012, Cellere,
E. 6.4.4.1; B-831/2011, SIX, E. 1217; Max
B. Berger/Roman Nogler, Beweisrecht - die Last mit dem Beweis(en), recht 2012, 171; Stefan
Bilger, Das Verwaltungsverfahren zur Untersuchung von Wettbewerbsbeschränkungen, 2002, S.
305; Jürgen Brönnimann, in: Berner Kommentar,
Schweizerische Zivilprozessordnung, Bd. II, 2012, Art. 157 Rz. 40; Rhinow/Koller/Kiss/Thurnherr/Brühl-Moser,
Öffentliches Prozessrecht, 3. Aufl. 2014, Rz. 999). Danach ist ein Beweis erbracht, wenn das
Gericht nach objektiven Gesichtspunkten von der Richtigkeit einer Sachbehauptung überzeugt ist.
Dabei wird allerdings keine absolute Gewissheit vorausgesetzt. Denn die Verwirklichung der Tatsache braucht
nicht mit Sicherheit festzustehen; vielmehr ist es ausreichend, wenn das Gericht am Vorliegen der behaupteten
Tatsache keine ernsthaften Zweifel mehr hat oder allenfalls verbleibende Zweifel als leicht erscheinen
(vgl. BGE 130 III 321 E. 3.2; Urteil des BGer 2A.500/2002 vom 24. März 2003 E. 3.5;
Urteile
B-831/2011, SIX, E. 1217; B-771/2012,
Cellere, E. 6.4.4.1; B-5685/2012, Altimum,
E. 4.5.3.1; B-7633/2009, ADSL
II, E. 157; B-8399/2010, Baubeschläge
Siegenia-Aubi, E. 4.3.3; B-8430/2010, Baubeschläge Koch,
E. 5.3.3).
5.3 Der
Wahrscheinlichkeitsbeweis stützt sich demgegenüber auf das Beweismass der überwiegenden
Wahrscheinlichkeit, wobei für die Richtigkeit der Sachbehauptung nach objektiven Gesichtspunkten
derart gewichtige Gründe sprechen, dass andere denkbare Möglichkeiten vernünftigerweise
nicht massgeblich in Betracht fallen (BGE 140 III 610 E. 4.1; 132 III 715 E. 3.1; Urteile B-831/2011,
SIX, E. 1218; B-771/2012, Cellere,
E. 6.4.4.2; B-7633/2009, ADSL II, E. 155 ff.).
5.4 Das
Bundesgericht hat hinsichtlich der Feststellung einer Marktbeherrschung und einer Marktabgrenzung in
grundlegender Weise klargestellt, dass bei komplexen wirtschaftlichen Sachverhalten ein Nachweis auf
der Grundlage der Gewissheit in ausreichender Weise nicht herbeigeführt werden kann und demzufolge
auch nicht erforderlich ist (BGE 139 I 72, Publigroupe,
E. 8.3.2 und 9.2.3.5). Diese Einschätzung gilt nicht nur in Bezug auf die Feststellung
der Marktbeherrschung oder der Marktabgrenzung, sondern letztlich für alle Tatbestandsmerkmale eines
wettbewerbswidrigen Verhaltens, soweit im Einzelfall multiple Wirkungszusammenhänge bestehen und
daher eine entsprechende Wettbewerbskomplexität gegeben ist. Für einen rechtsgenüglichen
Nachweis von kartellrechtlichen Tatbestandsmerkmalen ist bei Vorliegen der Wettbewerbskomplexität
aufgrund von multiplen Wirkungszusammenhängen demzufolge das Beweismass der überwiegenden Wahrscheinlichkeit
ausreichend und nicht ein Überzeugungsbeweis erforderlich (Urteile B-831/2011, SIX,
E. 1219; B-771/2012, Cellere, E. 6.4.4.4; B-7633/2009, ADSL
II, E. 80).
5.5 Dieses
Ergebnis entspricht den Prinzipien zur Anwendung des Überzeugungsbeweises als Regelbeweis und den
hierzu anerkannten Ausnahmen, bei denen ein Überzeugungsbeweis nach der Natur der Sache nicht möglich
oder zumutbar ist (Urteile B-831/2011, SIX, E. 1220; B-7633/2009,
ADSL II, E. 158). Denn im Rahmen einer Prüfung von einzelnen
Tatbeständen des Kartellgesetzes sind vielfach Einschätzungen mit einzubeziehen, die sich auf
zukünftige oder alternativ denkbare Ereignisse oder Auswirkungen beziehen. Dies entspricht einer
Berücksichtigung von hypothetischen Kausalzusammenhängen (Urteil B-831/2011, SIX,
E. 1220; im Ergebnis so bereits Urteile des BGer 2A.327/2006 vom 22. Februar 2007, 20Minuten,
E. 5.4; 2A.430/2006, Sammelrevers, E. 10.4). Für den Nachweis
des natürlichen Kausalzusammenhangs oder bei hypothetischen Kausalzusammenhängen gilt das Beweismass
der überwiegenden Wahrscheinlichkeit (Urteile B-831/2011, SIX,
E. 1218; B-7633/2009, ADSL II, E. 155, mit Verweis auf BGE
128 III 271 E. 2b/aa; 121 III 358 E. 5; 107 II 269 E. 1b). Weiter ist es offensichtlich, dass mit zunehmender
Komplexität einer Materie auch die Anzahl aller denkbaren Varianten eines Geschehensablaufs um ein
Vielfaches zunimmt. Der Grad und das Ausmass einer gerichtlichen Überzeugung verändern sich
daher notwendigerweise mit zunehmender Komplexität und den sich daraus ergebenden Interdependenzen
einer Materie. Bei Vorliegen von derartigen Aspekten kann im Einzelfall daher von vornherein keine Gewissheit
hergestellt werden, weshalb ein Wahrscheinlichkeitsbeweis für den erforderlichen Nachweis massgebend
ist (Urteile B-831/2011, SIX, E. 1220; B-807/2012 vom 25. Juni
2018, Erne, E. 8.4.4.4; B-7633/2009, ADSL
II, E.163).
6. Beweisanträge
6.1 Die
Beschwerdeführerinnen beantragen in ihrer Vernehmlassung und Replik, H._______ ([...] of HCI),
K._______ ([...] der HCI) und O._______ ([...] der HCI) zu befragen.
6.2 Die
Befragung von H._______ wird beantragt zu folgenden Punkten:
- zu
den INDEX-Datenbanken und deren Nutzer,
- zur
Qualität der INDEX-Datenbanken und der Datenbanken der Konkurrenten,
- zu
den Gründen für den Erfolg von HCI,
- zu
den von den Beschwerdeführerinnen vorgebrachten Gründen für die Verwendung der Klauseln
A und B in den Verträgen mit den Softwarehäusern, insbesondere zur Befürchtung betreffend
UWG-Verletzungen,
- zum
geltend gemachten Umstand, [...] Softwarehäusern erlaubt zu haben, die Datenbank [...] zu
benutzen und sie darin aktiv unterstützt zu haben,
- zum
geltend gemachten Umstand, den Zulassungsinhaberinnen die Inanspruchnahme der Qualitätskontrolle
bzw. Überprüfung der Arzneimittelinformationen auch separat angeboten zu haben,
- zum
vorgebrachten Argument, es sei für HCI nicht ersichtlich gewesen, weshalb anders als im Fall Documed,
wo die Verbindung der Qualitätssicherung und der Publikation nicht als Koppelung angesehen worden
sei, dies vorliegend der Fall sein soll,
- zum
Vorbringen, die Umstrukturierung der ehemaligen Galenica-Gruppe sei in keinem Zusammenhang mit der laufenden
Untersuchung der WEKO gestanden,
- zum
geltend gemachten Umstand, erhebliche Marktzu- und austrittsschranken seien nicht vorhanden,
- [...],
- zum
geltend gemachten Umstand, einige Zulassungsinhaberinnen hätten zwischenzeitlich keine Verträge
mit HCI abgeschlossen,
- zum
geltend gemachten Umstand, Documed und e-mediat hätten auch auf anderen (nicht relevanten) Märkten
Umsätze erzielt.
6.3 Die
Befragung von K._______ wird beantragt
- zu
den INDEX-Datenbanken,
- zur
Qualität der INDEX-Datenbanken und der Datenbanken der Konkurrenten,
- zur
Qualitätskontrolle der Arzneimittelinformationen im Rahmen der Aufnahme der Daten in das Kompendium
und die INDEX-Daten sowie deren Bedeutung für HCI, die Zulassungsinhaberinnen und die Leistungserbringer,
- zum
geltend gemachten Umstand, dass die Qualitätskontrolle, die HCI im Rahmen der Integration der Daten
ins Kompendium und die INDEX-Datenbank erbringe, nicht mit der Qualitätskontrolle von Dritten für
die Pflege eines Swissmedic-Zulassungsdossier vergleichbar sei,
- zum
konkreten Ablauf des Uploads auf AIPS bzw. zum geltend gemachten Umstand, der Upload dauere nur einige
Sekunden bzw. max. drei Minuten,
- zum
geltend gemachten Umstand, dass HCI auch bezüglich der zusätzlichen Datenelemente, die nicht
in den von Swissmedic geprüften Fachinformationen enthalten sind, eine Qualitätskontrolle vornehme,
sowie
- zum
geltend gemachten Umstand, HCI überprüfe auch die Aktualität der gelieferten Fachinformationen,
da es vorkomme, dass auf AIPS nicht die aktuellsten Versionen aufgeschaltet seien.
6.4 Die
Befragung von O._______ wird schliesslich beantragt zum geltend gemachten Umstand, [...] und einige
Pharmaunternehmen zwischenzeitlich keine Verträge mit HCI abgeschlossen hätten bzw. dass HCI
auf die Zusammenarbeit der Zulassungsinhaberinnen angewiesen sei, sowie zum geltend gemachten Umstand,
seit 2013 keine Anfrage für separate Qualitätssicherungsdienstleistungen erhalten zu haben.
6.5
In ihrer Replik beantragen die Beschwerdeführerinnen weiter die Befragung von Q._______ ([...]
der HCI) und zwar zu folgenden Punkten:
- zum
Vorbringen, dass 2013 rund [...] der Zulassungsinhaberinnen keinen Vertrag mit HCI abgeschlossen
hätten,
- zu
den einzelnen geltend gemachten Abzügen von den Umsätzen von Documed und e-mediat, welche nicht
auf den relevanten Märkten erzielt worden seien,
- zum
Vorbingen, dass es sich bei den geltend gemachten Erlösminderungen um Erlösminderungen i.S.v.
Art. 4 Abs. 1 Verordnung über die Kontrolle von Unternehmenszusammenschlüssen vom 17.
Juni 1996 (VKU, SR
Verordnung über die Kontrolle von Unternehmenszusammenschlüssen vom 17.
Juni 1996 (VKU, SR 251.4) handle bzw. zum Vorbringen, mit diesen Abzügen nicht zweimal die gleichen
Abzüge geltend zu machen.
251.4) handle bzw. zum Vorbringen, mit diesen Abzügen nicht zweimal die gleichen
Abzüge geltend zu machen.
6.6 Mit
Eingabe vom 16. November 2018 beantragen die Beschwerdeführerinnen weiter, Q._______ zum geltend
gemachten Umstand zu befragen, die Softwarehäuser im April 2017 darüber informiert zu haben,
dass sie nicht mehr an die Klausel B gebunden seien sowie über das Ausbleiben von Veränderungen
der Wettbewerbsverhältnisse seither. Weiter sei K._______ darüber zu befragen, dass HCI die
Qualitätskontrolle unterdessen optional anbiete, jedoch nur ein geringer Prozentsatz auf die Qualitätskontrolle
verzichte und HCI in diesen Fällen bei der Weiterverarbeitung der Daten im INDEX dennoch eine nahezu
gleichumfassende Qualitätskontrolle durchführen müsse. Zum geltend gemachten Ausbleiben
von Markteintritten von Unternehmen, die die Qualitätskontrolle in Konkurrenz zum Angebot von HCI
erbringen würden, sei schliesslich Q._______ zu befragen.
6.7 Die
Vorinstanz beantragt (eventualiter) letztere Beweisanträge abzuweisen. Die Beweisanträge seien
verspätet und es handle sich eher um Beweisofferten. Zudem seien diese Beweisofferten für den
Verfahrensausgang inhaltlich nicht relevant.
6.8 Das
Bundesverwaltungsgericht hat die von den Parteien angebotenen Beweis abzunehmen, wenn sie zur Abklärung
des Sachverhalts tauglich erscheinen (Art. 33 Abs. 1 VwVG; BGE 137 V 270 E. 3.2). Bei der Beurteilung
dieser Frage kommt dem Gericht allerdings ein gewisser Ermessensspielraum zu, denn es hat auch den Grundsatz
der Prozessökonomie zu beachten. Das Gericht ist namentlich dann nicht gehalten, Beweise abzunehmen,
wenn die zu beweisende Tatsache nicht entscheidwesentlich ist oder aufgrund der Akten oder anderer Beweismittel
bereits als bewiesen gelten kann (BGE 130 II 475 E. 2.2; Moser/Beusch/Kneubühler,
Prozessieren vor dem Bundesverwaltungsgericht, 2. Aufl. 2013, Rz. 3.123c). Diesfalls werden von den Parteien
gestellte Beweisanträge im Rahmen einer antizipierten Beweiswürdigung abgewiesen. Das ist zulässig,
wenn das Gericht aufgrund bereits erhobener Beweise oder aus anderen Gründen den rechtserheblichen
Sachverhalt für genügend geklärt hält und überzeugt ist, seine rechtliche Überzeugung
würde durch weitere Beweiserhebungen nicht geändert (BGE 134 I 148 E. 5.3; 131 I 157 E. 3;
130 II 429 E. 2.1; BVGE 2011/47 E. 2.3; Moser/Beusch/Kneubühler,
a.a.O., Rz. 3.144).
VwVG; BGE 137 V 270 E. 3.2). Bei der Beurteilung
dieser Frage kommt dem Gericht allerdings ein gewisser Ermessensspielraum zu, denn es hat auch den Grundsatz
der Prozessökonomie zu beachten. Das Gericht ist namentlich dann nicht gehalten, Beweise abzunehmen,
wenn die zu beweisende Tatsache nicht entscheidwesentlich ist oder aufgrund der Akten oder anderer Beweismittel
bereits als bewiesen gelten kann (BGE 130 II 475 E. 2.2; Moser/Beusch/Kneubühler,
Prozessieren vor dem Bundesverwaltungsgericht, 2. Aufl. 2013, Rz. 3.123c). Diesfalls werden von den Parteien
gestellte Beweisanträge im Rahmen einer antizipierten Beweiswürdigung abgewiesen. Das ist zulässig,
wenn das Gericht aufgrund bereits erhobener Beweise oder aus anderen Gründen den rechtserheblichen
Sachverhalt für genügend geklärt hält und überzeugt ist, seine rechtliche Überzeugung
würde durch weitere Beweiserhebungen nicht geändert (BGE 134 I 148 E. 5.3; 131 I 157 E. 3;
130 II 429 E. 2.1; BVGE 2011/47 E. 2.3; Moser/Beusch/Kneubühler,
a.a.O., Rz. 3.144).
Die beantragten Parteibefragungen von H._______, O._______, K._______
und Q._______ sind in diesem Sinne in antizipierter Beweiswürdigung abzuweisen. Soweit Aussagen
zu einzelnen der oben erwähnten Umstände überhaupt entscheidrelevant sind, erachtet das
Gericht den Sachverhalt als genügend geklärt. H._______ wurde bereits am 20. Februar 2013 anlässlich
einer Parteieinvernahme durch das Sekretariat befragt, ebenso G._______, [...] von e-mediat und Documed.
Des Weiteren haben die Parteien im Laufe des Untersuchungsverfahrens zu mehreren Auskunftsbegehren Stellung
genommen und wiederholt unaufgefordert Informationen zur Sachverhaltsermittlung eingereicht. Die Vorinstanz
hat am 24. Oktober 2016 anlässlich der Anhörung von HCI auch H._______ und K._______ befragt.
Schliesslich haben die Parteien im Beschwerdeverfahren ihre Standpunkte und Schilderungen zum Sachverhalt
im Rahmen eines umfangreichen Schriftenwechsels und in unaufgeforderten Eingaben ausführlich darlegt.
7. Weitere
Anträge der Beschwerdeführerinnen
Die Beschwerdeführerinnen stellen fünf als "Verfahrensanträge" bezeichnete
Begehren (s. oben E. H.a.b),
welche sich auf die ordnungsgemässe Führung dieses Verfahrens beziehen.
7.1 Beizug
von Akten
7.1.1 Mit
dem ersten "Verfahrensantrag" beantragen die Beschwerdeführerinnen, es seien die Akten
der Untersuchung 32-0249 bei der Vorinstanz einzuholen. Dieser Antrag ist kein Verfahrens-, sondern ein
Beweisantrag. Im Rahmen des Beschwerdeverfahrens, das vom Untersuchungsprinzip (Art. 12 VwVG) beherrscht
wird, ist über Beweisanträge weder im Zusammenhang mit den Prozessvoraussetzungen noch in allgemeiner,
von konkreten Sachfragen losgelöster Weise zu befinden. Vielmehr sind Beweisanträge immer nur
bezogen auf bestimmte Fragestellungen und konkret zu bezeichnende Unterlagen zu prüfen, wenn die
Erwägungen zur Sache anzustellen sind.
7.1.2 Das
Bundesverwaltungsgericht hat die Akten der Vorinstanz im Sinne des Beweisantrags der Beschwerdeführerinnen
beigezogen.
7.2 Anordnung
eines zweiten Schriftenwechsels und Durchführung einer öffentlichen Verhandlung und/oder Instruktionsverhandlung
7.2.1 Die
Beschwerdeführerinnen beantragen weiter die Anordnung eines zweiten Schriftenwechsels (Verfahrensantrag
2) sowie die Durchführung einer öffentlichen Parteiverhandlung und/oder einer Instruktionsverhandlung
(Verfahrensantrag 3).
7.2.2 Gemäss
Art. 57 Abs. 2 VwVG kann die Beschwerdeinstanz die Parteien auf jeder Stufe des Verfahrens zu einem weiteren
Schriftenwechsel einladen oder eine mündliche Verhandlung mit ihnen anberaumen. Die Durchführung
eines zweiten Schriftenwechsels kommt in der Praxis häufig vor und ist jedenfalls nötig, wenn
der Anspruch auf Wahrung des rechtlichen Gehörs oder die Pflicht der Abklärung des entscheidrelevanten
Sachverhaltes dies erfordern. Eine mündliche Verhandlung kann hilfreich sein, sobald vertiefte oder
umfangreiche Abklärungen nötig sind und zu erwarten ist, dass schriftliche Eingaben nicht zu
allen massgebenden Gesichtspunkten genügend Aufschluss geben (Seetaler/Plüss,
Praxiskommentar VwVG, Art. 57
VwVG kann die Beschwerdeinstanz die Parteien auf jeder Stufe des Verfahrens zu einem weiteren
Schriftenwechsel einladen oder eine mündliche Verhandlung mit ihnen anberaumen. Die Durchführung
eines zweiten Schriftenwechsels kommt in der Praxis häufig vor und ist jedenfalls nötig, wenn
der Anspruch auf Wahrung des rechtlichen Gehörs oder die Pflicht der Abklärung des entscheidrelevanten
Sachverhaltes dies erfordern. Eine mündliche Verhandlung kann hilfreich sein, sobald vertiefte oder
umfangreiche Abklärungen nötig sind und zu erwarten ist, dass schriftliche Eingaben nicht zu
allen massgebenden Gesichtspunkten genügend Aufschluss geben (Seetaler/Plüss,
Praxiskommentar VwVG, Art. 57 VwVG N 35 und 57).
VwVG N 35 und 57).
7.2.3 Soweit
zivilrechtliche Ansprüche oder strafrechtliche Anklagen im Sinne von Art. 6 Abs. 1 EMRK zu beurteilen
sind, ordnet der Instruktionsrichter bzw. die Instruktionsrichterin eine öffentliche Parteiverhandlung
an, wenn dies von einer Partei verlangt wird (Art. 40 Abs. 1 Bst. a
EMRK zu beurteilen
sind, ordnet der Instruktionsrichter bzw. die Instruktionsrichterin eine öffentliche Parteiverhandlung
an, wenn dies von einer Partei verlangt wird (Art. 40 Abs. 1 Bst. a VGG). Im schriftlichen
Verfahren hat der rechtssuchende Private (hier also die Beschwerdeführerinnen) jeweils das letzte
Wort, was einerseits im verfassungsmässigen Anspruch auf rechtliches Gehör gemäss Art. 29
Abs. 2
VGG). Im schriftlichen
Verfahren hat der rechtssuchende Private (hier also die Beschwerdeführerinnen) jeweils das letzte
Wort, was einerseits im verfassungsmässigen Anspruch auf rechtliches Gehör gemäss Art. 29
Abs. 2 BV und andererseits im Grundsatz des "fair trial" gemäss Art. 6 Abs. 1
BV und andererseits im Grundsatz des "fair trial" gemäss Art. 6 Abs. 1 EMRK
seine Grundlage findet (Moser/Beusch/Kneubühler, a.a.O., Rz. 3.47
und 3.50).
EMRK
seine Grundlage findet (Moser/Beusch/Kneubühler, a.a.O., Rz. 3.47
und 3.50).
7.2.4 Betreffend
die Anträge der Beschwerdeführerinnen auf einen zweiten Schriftenwechsel sowie auf die Durchführung
einer öffentlichen Parteiverhandlung und/oder einer Instruktionsverhandlung kann auf die sachverhaltlichen
Ausführungen zum Verfahren vor dem Bundesverwaltungsgericht verwiesen werden (s. oben E. H.c
und H.d).
Ein zweiter Schriftenwechsel wurde durchgeführt und auf eine öffentliche Parteiverhandlung
haben die Beschwerdeführerinnen mit Schreiben vom 3. Mai 2019 verzichtet.
7.2.5 Betreffend
den Antrag auf Durchführung einer Instruktionsverhandlung ist auf E. 6.9
oben zu verweisen. Das Gericht weist auch den Antrag auf Parteibefragungen von H._______, O._______,
K._______ und Q._______ ab, weil die zu beweisenden Tatsachen, sofern sie überhaupt entscheidwesentlich
sind, aufgrund der Akten und der umfangreichen Parteieingaben bereits als genügend bewiesen angesehen
werden. Angesichts dessen erscheint die Durchführung einer Instruktionsverhandlung wenig sinnvoll,
da sie kaum noch etwas zur Klärung beizutragen vermag. Auf die Durchführung einer Instruktionsverhandlung
wird somit verzichtet.
7.3 Wahrung
von Geschäftsgeheimnissen
7.3.1 Schliesslich
beantragen die Beschwerdeführerinnen, die in der Beschwerde und den Beilagen zur Beschwerde enthaltenen
Informationen Dritten nicht offenzulegen, da diese Geschäftsgeheimnisse enthalten (Verfahrensantrag
4) sowie im Falle einer Entscheidpublikation den zu publizierenden Text vor Veröffentlichung zur
Prüfung auf allfällige Geschäftsgeheimnisse den Beschwerdeführerinnen zuzustellen
(Verfahrensantrag 5).
7.3.2 Diese
beiden Anträge, mit denen die Wahrung von Geschäftsgeheimnissen sichergestellt werden soll,
sind im Rahmen der Verfahrensführung zu berücksichtigen. Das Bundesverwaltungsgericht hat Entscheide
grundsätzlich in anonymisierter Form zu veröffentlichen (vgl. Art. 29 Abs. 2 VGG i.V.m. Art.
4 Abs. 2 und Art. 8 des Informationsreglements für das Bundesverwaltungsgericht vom 11. Dezember
2006 [SR
VGG i.V.m. Art.
4 Abs. 2 und Art. 8 des Informationsreglements für das Bundesverwaltungsgericht vom 11. Dezember
2006 [SR 173.320.4]), und es wird die für die Wettbewerbsbehörden nach Art. 25 Abs. 1
173.320.4]), und es wird die für die Wettbewerbsbehörden nach Art. 25 Abs. 1 und 4
und 4 KG ex lege geltende Pflicht zur Wahrung von Geschäftsgeheimnissen sinngemäss ebenfalls zu befolgen
haben.
KG ex lege geltende Pflicht zur Wahrung von Geschäftsgeheimnissen sinngemäss ebenfalls zu befolgen
haben.
7.4 Fazit
zu den Beweisanträgen und verfahrensrechtlichen Anträgen
7.4.1 Im
Sinne eines Zwischenfazits ist damit festzuhalten, dass die Akten der Vorinstanz beigezogen und ein zweiter
Schriftenwechsel angeordnet wurde. Zudem sind die Anträge der Beschwerdeführerinnen, mit denen
die Wahrung von Geschäftsgeheimnissen sichergestellt werden soll, im Rahmen der Verfahrensführung
zu berücksichtigen.
7.4.2 Im
Übrigen sind die Beweisanträge und verfahrensrechtlichen Anträge der Beschwerdeführerinnen
abzuweisen. Im Folgenden sind die materiellen Rügen zu prüfen.
8. Relevanter
Markt
Für die Feststellung einer marktbeherrschenden Stellung gemäss Art. 7 i.V.m.
Art. 4 Abs. 2
i.V.m.
Art. 4 Abs. 2 KG ist es erforderlich, in einem ersten Schritt den relevanten Markt, auf dem diese marktbeherrschende
Stellung eingenommen wird, abzugrenzen, bevor in einem zweiten Schritt die Marktstellung ermittelt werden
kann (BGE 139 I 72, Publigroupe, E. 9.1; Urteil des BGer 2C_113/2017
vom 12. Februar 2020, Hallenstadion, E. 5.1; Urteile
KG ist es erforderlich, in einem ersten Schritt den relevanten Markt, auf dem diese marktbeherrschende
Stellung eingenommen wird, abzugrenzen, bevor in einem zweiten Schritt die Marktstellung ermittelt werden
kann (BGE 139 I 72, Publigroupe, E. 9.1; Urteil des BGer 2C_113/2017
vom 12. Februar 2020, Hallenstadion, E. 5.1; Urteile
B-831/2011,
SIX, E. 229; B-7633/2009, ADSL
II, E. 256; David/Jacobs, a.a.O., Rz. 696; Stäuble/Schraner,
DIKE-KG, Art. 4 N 7 f.).
N 7 f.).
Das Kartellgesetz enthält weder eine Definition des relevanten Markts noch statuiert es einzelne
Kriterien für dessen Bestimmung. Allerdings weist die Verordnung des Bundesrates vom 17. Juni 1996
über die Kontrolle von Unternehmenszusammenschlüssen (VKU, SR 251.4) in Art. 11 Abs. 1 und 3
sachliche, räumliche und zeitliche Aspekte zur Beurteilung von einzelnen Zusammenschlussvorhaben
auf. Demzufolge lassen sich der sachlich, der räumlich und der zeitlich relevante Markt unterscheiden.
Nach ständiger Rechtsprechung finden diese Abgrenzungskriterien auch für die Beurteilung anderer
Wettbewerbsbeschränkungen Anwendung (BGE 139 I 72, Publigroupe,
E. 9.1; Urteile 2C_113/2017, Hallenstadion, E. 5.1;
251.4) in Art. 11 Abs. 1 und 3
sachliche, räumliche und zeitliche Aspekte zur Beurteilung von einzelnen Zusammenschlussvorhaben
auf. Demzufolge lassen sich der sachlich, der räumlich und der zeitlich relevante Markt unterscheiden.
Nach ständiger Rechtsprechung finden diese Abgrenzungskriterien auch für die Beurteilung anderer
Wettbewerbsbeschränkungen Anwendung (BGE 139 I 72, Publigroupe,
E. 9.1; Urteile 2C_113/2017, Hallenstadion, E. 5.1;
B-831/2011,
SIX, E. 230; B-506/2010, Gaba,
E. 9; B-7633/2009, ADSL II, E. 256 f.).
8.1 Sachlich
relevanter Markt
Der sachlich relevante Markt umfasst alle Waren und Leistungen, die von der Marktgegenseite
hinsichtlich
ihrer Eigenschaften und ihres vorgesehenen Verwendungszwecks als substituierbar angesehen
werden (Art.
11 Abs. 3 Bst. a VKU). Wesentliche Grundlage zur Abgrenzung des sachlich relevanten Marktes
bildet in Bezug auf Absatzmärkte das Konzept der Nachfragesubstituierbarkeit (auch sog. Konzept
der funktionellen Austauschbarkeit bzw. Bedarfsmarktkonzept; vgl. Art. 11 Abs. 3 VKU).
Massgebend ist dabei, welche anderen Waren oder Dienstleistungen mit dem in Frage stehenden Produkt in
Wettbewerb stehen. Dies ist immer dann der Fall, wenn die Austauschbarkeit der verschiedenen Produkte
gegeben ist, weil sie aufgrund ihrer Eigenschaften, Preise und dem vorgesehenen Verwendungszweck von
den Nachfragern als gleichwertig angesehen werden (BGE 139 I 72, Publigroupe,
E. 9.2.3.1; Urteile B-831/2011, SIX, E. 253; B-7633/2009,
ADSL II, E. 270; B-506/2010, Gaba,
E. 9 und 9.1.4.1).
Das Bedarfsmarktkonzept fokussiert auf die Marktgegenseite (Urteil 2C_113/2017,
Hallenstadion,
E. 5.2.4). Die Definition des sachlichen Marktes
erfolgt somit aus Sicht der Gegenseite desjenigen Unternehmens,
welchem das unzulässige Verhalten vorgeworfen wird (Borer,
a.a.O., Art. 5 Rz. 11; Reto A. Heizmann, Der Begriff des marktbeherrschenden
Unternehmens im Sinne von Art. 4 Abs. 2 in Verbindung mit Art. 7
in Verbindung mit Art. 7 KG, 2005, Rz. 280). Auszugehen
ist vom Durchschnittsverbraucher, vom vernünftig durchschnittlichen Nachfrager (Urteil 2C_113/2017,
Hallenstadion, E. 5.2.4).
KG, 2005, Rz. 280). Auszugehen
ist vom Durchschnittsverbraucher, vom vernünftig durchschnittlichen Nachfrager (Urteil 2C_113/2017,
Hallenstadion, E. 5.2.4).
Massgebend ist, welche Produkte aus dieser Sicht den Bedarf in akzeptabler Weise
zufriedenstellend
erfüllen. Für eine zufriedenstellende Erfüllung ist es dabei einerseits nicht erforderlich,
dass die Leistung in identischer Weise erbracht wird, andererseits ist eine bloss teilweise Austauschbarkeit
nicht ausreichend (BGE 139 I 72, Publigroupe, E. 9.2.3.5;
Urteile B-831/2011, SIX, E. 253; B-3618/2013 vom 24. November
2016, Hallenstadion, E. 55; B-7633/2009, ADSL
II, E. 270). Die Austauschbarkeit eines Produkts ist insbesondere aufgrund von funktionalen
Sachüberlegungen, allgemeinen Verbraucherpräferenzen, bestehenden Marktstrukturen sowie von
konkreten Marktbeobachtungen aller in Betracht kommenden ähnlichen Produkten zu bewerten. Zudem
können auch modellhafte Überlegungen, wie etwa der sog. SSNIP-Test (small
but significant and nontransitory increase in price-Test), zur Abgrenzung herangezogen werden
(BVGE 2011/32, Terminierung Mobilfunk, E. 9.5.3; Urteile
B-831/2011, SIX, E. 253; B-7633/2009, ADSL
II, E. 270).
Ein SSNIP-Test stellt eine modellhafte Verhaltensanalyse dar, bei der mittels
geringer, aber spürbarer
und nicht nur vorübergehender Preiserhöhung im Rahmen von 5% bis 10% untersucht wird, bei welcher
Preiserhöhung die Nachfrager das zu beurteilende Produkt durch welche vergleichbaren Produkte ersetzen.
Der SSNIP-Test stellt jedoch keine zwingende Voraussetzung einer Marktabgrenzung dar. Er bildet nur ein
Mittel, das zur Ermittlung der massgeblichen Gruppe an austauschbaren Produkten zusätzlich herangezogen
werden kann, soweit die Austauschbarkeit im Hinblick auf den Verwendungszweck nicht bereits aufgrund
eines Vergleichs der Produktmerkmale der verfügbaren Produkte oder des bisherigen Ausweichverhaltens
der Nutzer festgestellt werden kann. Diese ergänzende Funktion folgt bereits daraus, dass ein SSNIP-Test
selbst immanente Schwächen und ein gewisses Fehlerpotential in sich birgt und für bestimmte
Sachverhaltskonstellationen nicht anwendbar ist. Angesichts dessen stellt ein SSNIP-Test kein Mittel
dar, welches im Rahmen einer Marktabgrenzung in jedem Fall uneingeschränkt zur Anwendung gelangen
kann oder muss (Urteil B-831/2011, SIX, E. 269-275 m.w.H.).
8.1.1
Marktgegenseite
8.1.1.1 Ausgehend
vom Verfahrensgegenstand ist die Marktgegenseite zu bestimmen, aus deren Sicht der relevante Markt abzugrenzen
ist. Verfahrensgegenstand ist vorliegend die Kommerzialisierung von elektronischen Medikamenteninformationen.
8.1.1.2 Die
Vorinstanz erwog, HCI sei im Bereich der Datenveredelung, d.h. der Aufbereitung von ökonomischen
und wissenschaftlichen Daten, welche für den Vertrieb, die Abgabe und Abrechnung von Arzneimitteln
benötigt werden, tätig. Auf der Marktgegenseite ständen die Leistungserbringerinnen und
-erbringer, welchen die Datenprodukte bei der Verschreibung der Arzneimittel, der Beratung, den Abrechnungsprozessen,
etc. dienen, sowie die Vertriebsunternehmen und Kostenträger betreffend Bestellprozess und Rechnungsprüfung.
Weiter würden den Datenveredler die Softwarehäuser gegenüberstehen, welche Arztpraxisadministrationssysteme,
Waren- und Wirtschaftssysteme etc. anböten. Diese würden betreffend Nutzung der Daten und den
entsprechenden Schnittstellen mit den Datenveredlern in vertraglicher Beziehung stehen, womit sie in
Bezug auf die Integration der Datenbanken in die Softwarelösung ebenfalls Marktgegenseite seien.
8.1.1.3 Weiter
erwog die Vorinstanz, auch die Zulassungsinhaberinnen würden zur Marktgegenseite zählen. Bis
Ende 2012 hätten die Zulassungsinhaberinnen zwar ausschliesslich die Publikation ihrer Arzneimittelinformationen
und damit formal rein die Aufnahme ins Kompendium nachgefragt und bezahlt, ab 2013 habe HCI den Zulassungsinhaberinnen
die Aufnahme der Arzneimittelinformationen in ihre Datensätze gegen Entgelt angeboten. Damit seien
die Zulassungsinhaberinnen Nachfragerinnen und Marktgegenseite für die Aufnahme der Medikamenteninformationen
in die INDEX-Produkte von HCI geworden.
8.1.1.4 Die
Beschwerdeführerinnen bestreiten nicht, dass die Zulassungsinhaberinnen sowie Leistungserbringerinnen
und -erbringer, Vertriebsunternehmen und Kostenträger die Marktgegenseite darstellen. Nicht Marktgegenseite
seien jedoch die Softwarehäuser. Denn die Leistungserbringerinnen und -erbringer würden die
Medikamenteninformationen für Vertrieb, Verschreibung, Abgabe und Abrechnung von Medikamenten nachfragen.
Die Lizenzverträge schliesse HCI - ausser bei medINDEX - nicht mit den Softwarehäusern,
sondern direkt mit den Leistungserbringerinnen und -erbringern ab. Bei allen INDEX-Produkten ausser medINDEX
seien die Softwarehäuser nicht Marktgegenseite, sondern nur Vermittler.
8.1.1.5 Als
Marktgegenseite gelten die Nachfrager bzw. Abnehmer eines durch das marktbeherrschende Unternehmen abgesetzten
Produkts (Urteil B-7633/2009, ADSL II, E. 270).
8.1.1.6 Dass
die Leistungserbringerinnen und -erbringer, die Kostenträger und die Grossisten zur Marktgegenseite
zählen, ist unbestritten. Gleiches gilt für die Zulassungsinhaberinnen.
8.1.1.7 Die
Softwarehäuser fragen die elektronischen Medikamenteninformationen zwar nicht als Endabnehmer zur
Nutzung nach. Sie fragen jedoch die Integration der Datenbanken in ihre Softwarelösungen nach. Dies
ist für die Softwarehäuser wichtig, um den Endabnehmern eine deren Bedürfnissen entsprechende
Softwarelösung anbieten zu können. Die Softwarehäuser stehen bezüglich Integration
der Datenbanken in ihre Software, wie von der Vorinstanz zutreffend ausgeführt, ebenfalls in einer
vertraglichen Beziehung zu HCI. Dies ist bei allen Softwarehäusern der Fall und nicht nur bei denjenigen,
die für den medINDEX die Lizenzverträge direkt mit den Leistungserbringerinnen und -erbringer
abschliessen. Entsprechend ist die Vorinstanz zutreffend zum Schluss gekommen, dass auch die Softwarehäuser
Marktgegenseite darstellen und zwar unabhängig davon, ob sie - wie beim medINDEX - mit
den Leistungserbringerinnen und -erbringern direkt Lizenzverträge abschliessen oder die Lizenzverträge
mit den Leistungserbringerinnen und -erbringern von HCI abgeschlossen werden.
8.1.1.8 Die
Abgrenzung des sachlich relevanten Marktes ist in der Folge je separat für die Marktgegenseite der
Leistungserbringerinnen und -erbringer, Vertriebsunternehmen, Kostenträger und Softwarehäuser
einerseits (s. unten E. 8.1.2)
sowie für die Marktgegenseite der Zulassungsinhaberinnen andererseits vorzunehmen (s. unten E. 8.1.3).
8.1.2
Sachlich
relevanter Markt betreffend die Marktgegenseite der Leistungserbringerinnen und -erbringer, Vertriebsunternehmen,
Kostenträger und Softwarehäuser
8.1.2.1 Die
Vorinstanz zog das Angebot von HCI an die Leistungserbringerinnen und -erbringer, Vertriebsunternehmen,
Kostenträger und Softwarehäuser als Ausgangspunkt für die Marktabgrenzung heran. Demzufolge
würden "Medikamenteninformationen für den Vertrieb, die Verschreibung, die Abgabe und
Abrechnung von Medikamenten" nachgefragt werden. Diese Informationen könne die Marktgegenseite
in verschiedenen Formen und über verschiedene Kanäle beziehen, namentlich gedruckt in Printmedien,
online oder aggregiert als veredelte maschinenlesbare Datensammlungen.
8.1.2.2 Betreffend
den Bezug der Medikamenteninformationen aus den Printmedien kam die Vorinstanz zum Schluss, dass dies
kein Substitut für veredelte, maschinenlesbare Datensätze darstelle. Denn die Leistungserbringerinnen
und -erbringer könnten mit dem ausschliesslichen Bezug solcher gedruckten Publikationen ihrer Sorgfaltspflicht
nicht umfassend bzw. nur mit erheblichem Mehraufwand nachkommen und die Funktionen, die ein veredelter
Datensatz erfülle, würden über die in den Printmedien vorhandenen Datensätze hinausgehen.
Die Arzneimittelinformationen seien seit dem Verzicht auf das Erfordernis der gedruckten Publikation
nicht mehr aktuell in den Printmedien verfügbar.
8.1.2.3 Beim
Online-Bezug der Medikamenteninformationen aus unveredelten Datensätzen müssten die Informationen
aus verschiedensten Quellen manuell zusammengetragen werden und gewisse kommerzielle Informationen wie
die MwSt.-Nr. direkt bei den Zulassungsinhaberinnen nachgefragt werden. Entsprechend könne zwar
der Umstieg von der manuellen Recherche aus verschiedenen Quellen auf eine Softwarelösung als Alternative
betrachtet werden, nicht aber der Umstieg von einer Softwarelösung auf die manuelle Recherche aus
verschiedenen Quellen mit dem Verlust der anwenderspezifischen Features der Software. Für diejenigen
Leistungserbringerinnen und -erbringer, Vertriebsunternehmen und Kostenträger, welche bereits mit
elektronischen Systemen arbeiten würden, seien unveredelte, nicht maschinenlesbare Daten keine Substitute.
8.1.2.4 Entsprechend
ging die Vorinstanz davon aus, dass die Marktgegenseite, also die Leistungserbringerinnen und -erbringer,
Vertriebsunternehmen und Kostenträger, im Zusammenhang mit EDV-basierten Tätigkeiten veredelte,
maschinenlesbare Daten nachfragen würden, weshalb von einem entsprechenden sachlichen Markt für
veredelte, maschinenlesbare Daten betreffend Medikamenteninformationen auszugehen sei.
8.1.2.5 Schliesslich
erwog die Vorinstanz, auch die Softwarehäuser würden für ihre Dienstleistung veredelte
Daten in maschinenlesbarer Form benötigen, auf welche ihre Software je nach gewünschter Funktion
zugreifen könne. Ihre Software und ihre Schnittstellen seien auf derartige Datenbanken angepasst
und eine Verwendung der Software ohne Daten sei nicht möglich. Zudem müssten die Softwarehäuser
den Endabnehmern veredelte, maschinenlesbare Daten liefern, weshalb die Softwarehäuser ebendiese
als Ausgangsprodukt nachfragten. Somit sei auch betreffend die Marktgegenseite der Softwarehäuser
von einem Markt für veredelte, maschinenlesbare Daten betreffend Medikamenteninformationen auszugehen.
8.1.2.6 Es
ist nichts ersichtlich, was gegen diese Abgrenzung des sachlich relevanten Marktes sprechen würde.
Auch die Beschwerdeführerinnen haben dagegen keine Einwände vorgebracht. Die Vorinstanz hat
die Substituierbarkeit der verschiedenen Formen des Bezuges der Medikamenteninformationen zutreffend
dargelegt.
8.1.3
Sachlich
relevanter Markt betreffend die Marktgegenseite der Zulassungsinhaberinnen
8.1.3.1 Die
Vorinstanz stellte fest, dass HCI den Zulassungsinhaberinnen den Abschluss eines Vertrages für die
Aufnahme von deren Medikamenteninformationen in ihre Datensätze (INDEX-Produkte) anbiete. Gleichzeitig
biete HCI zwar auch eine Reihe von anderen Dienstleistungen an, die inhaltlich nicht mit der Aufnahme
in die Datenbank zusammenhingen, aber nicht unabhängig davon gebucht werden könnten. Prima
Vista betreffe der wesentliche sachlich relevante Markt den Zugang zu elektronischen Datensätzen,
welche die Leistungserbringerinnen und -erbringer konsultieren bzw. benutzen. Der relevante Markt sei
deshalb der Markt für den Zugang zu elektronischen Datensätzen betreffend Medikamenteninformationen
für die Leistungserbringerinnen und -erbringer, Vertriebsunternehmen und Kostenträger.
8.1.3.2 Die
Beschwerdeführerinnen bringen vor, der sachlich relevante Markt umfasse nicht nur den Markt für
den "Zugang" zu elektronischen Datensätzen betreffend Medikamenteninformationen, sondern
auch für die Aufbereitung und Kontrolle der Daten sowie die Aufnahme und der Erhalt bzw. den Unterhalt
in den elektronischen Datensätzen und gleichzeitig die Nutzung einer aufgebauten Infrastruktur,
da die Zulassungsinhaberinnen ein Interesse an prozessintegrierten Daten für ihre Produkte hätten.
8.1.3.3 Wie
die Vorinstanz zutreffend erwog, fragen die Zulassungsinhaberinnen bei HCI insbesondere den Abschluss
eines Vertrages für die Aufnahme ihrer Medikamenteninformationen in ihre Datensätze betreffend
Medikamenteninformationen (INDEX-Produkte) nach. Daneben fragen die Zulassungsinhaberinnen auch den Erhalt
ihrer Medikamenteninformationen in diesen Datensätzen nach.
8.1.3.4 Soweit
die Vorinstanz gestützt hierauf zum Schluss kommt, der sachlich relevante Markt sei somit der Zugang
zu elektronischen Daten-sätzen betreffend Medikamenteninformationen, welche die Leistungserbringerinnen
und -erbringer konsultieren und nutzen, erscheint der Begriff "Zugang" nicht treffend. Denn
die Zulassungsinhaberinnen fragen nicht den Zugang bzw. Zugriff zu einer Datenbank mit elektronischen
Datensätzen betreffend Medikamenteninformationen nach, sondern es geht - wie oben bereits
festgehalten - um die Aufnahme der Medikamenteninformationen der Zulassungsinhaberinnen in Datenbanken
mit elektronischen Datensätzen betreffend Medikamenteninformationen, die von Leistungserbringerinnen
und -erbringern genutzt werden.
8.1.3.5 Offensichtlich
ist, dass die Zulassungsinhaberinnen daneben auch den Erhalt ihrer Medikamenteninformationen in diesen
Datensätzen nachfragen. Somit ist der sachlich relevante Markt als Markt für die Aufnahme und
den Erhalt in elektronischen Datensätzen betreffend Medikamenteninformationen zu definieren.
8.1.3.6 Soweit
jedoch die Beschwerdeführerinnen den sachlich relevanten Markt noch weiter fassen und die Elemente
der Aufbereitung, der Kontrolle und des Unterhalts der Daten berücksichtigt haben möchten,
ist der Vorinstanz zuzustimmen, dass es sich hierbei um keine Kriterien der Marktdefinition handelt,
sondern um Charakteristika des spezifischen Angebotes von HCI. Dies stellt ein Teil der Marktstellungsproblematik
dar (s. unten E. 9).
8.2 Räumlich
relevanter Markt
8.2.1 Der
räumlich relevante Markt umfasst das geographische Gebiet, innerhalb dessen die wechselseitig substituierbaren
Produkte der sachlich relevanten Produktgruppe von den jeweiligen Wettbewerbern unter hinreichend gleichwertigen
Wettbewerbsbedingungen abgesetzt werden (Art. 11 Abs. 3 lit. b VKU; BGE 139 I 72,
Publigroupe, E. 9.2.1; Urteile 2C_113/2017,
Hallenstadion, E. 5.4.1; B-831/2011, SIX,
E. 320;
B-7633/2009, ADSL II, E. 302).
8.2.2 Die
Vorinstanz ging sowohl für veredelte, maschinenlesbare Daten betreffend Medikamenteninformationen
als auch für den Zugang zu elektronischen Datensätzen betreffend Medikamenteninformationen
von einem nationalen Markt aus. Denn die Rahmenbedingungen des Gesundheitswesens seien durch die nationale
Gesetzgebung geprägt. Arzneimittel würden spezifisch für die Schweiz zugelassen werden,
wodurch Datensätze mit Medikamenteninformationen den nationalen Begebenheiten Rechnung tragen müssten.
Von einer engeren sprachregionalen Abgrenzung könne abgesehen werden, da die Zulassungsinhaberinnen
verpflichtet seien, die Arzneimittelinformationen in Deutsch, Französisch und Italienisch auf AIPS
zu publizieren und die Struktur der Medikamenteninformationen sprachunabhängig vorgegeben und auch
in veredelten Datenbanken identisch sei. Die Kosten aufgrund mehrerer Sprachen seien relativ gering und
die INDEX-Produkte würden schweizweit angeboten werden.
8.2.3 Die
Beschwerdeführerinnen rügen, beim räumlich relevanten Markt sei zu berücksichtigen,
dass Anbieter auch aus dem Ausland stammen könnten und sich der Markt zukünftig weiter öffnen
werde, da in der Schweiz die Daten künftig nach den Standards der EU geliefert werden müssten.
8.2.4 Massgebend
für die Abgrenzung des räumlich relevanten Markts ist, ob in einem bestimmten geographischen
Gebiet spürbar unterschiedliche Wettbewerbsbedingungen gegenüber denjenigen in den angrenzenden
Gebieten vorzufinden sind. Der räumlich relevante Markt kann dadurch im Einzelfall lokal, regional,
national, international oder weltweit abzugrenzen sein (Urteile B-831/2011, SIX,
E. 321; B-3618/2013, Hallenstadion, E. 149; B-7633/2009,
ADSL II, E. 302; Stäuble/Schraner,
DIKE-KG, Art. 4 Abs. 2 N 98; Weber/Volz,
a.a.O., Rz. 2.45;
Borer, a.a.O., Art. 5 Rz. 15).
8.2.5 Wichtige
Indizien für unterschiedliche räumliche Märkte sind insbesondere ein unterschiedliches
Preisniveau, sprachliche Unterschiede, gesetzliche Vorschriften, Handelshemmnisse, Verbraucherpräferenzen
etc. (Urteil des BVGer B-3332/2012 vom 13. November 2015, BMW,
E. 7.2; Beat Zirlick/Marc Blatter/Simon Bangartner, Äpfel
mit Birnen vergleichen?, in: Jusletter 11. September 2017, Rz. 27; Reinert/Wälchli,
BSK-KG, Art. 4 Abs. 2 N 218 ff.).
8.2.6 Betreffend
die zeitliche Dimension ist im Wesentlichen von den Verhältnissen in der massgeblichen Zeitperiode
auszugehen. Die Berücksichtigung nachträglicher Entwicklungen ist nur bedingt möglich,
nämlich dann, wenn diese zwingend Schlüsse auf die frühere Situation zulassen. Im Übrigen
ist entscheidend, dass es um die kartellrechtliche Sanktionierung eines in der Vergangenheit liegenden
Marktverhaltens geht. Gerade mit Blick auf den strafrechtlichen Charakter des Sanktionsverfahrens verbietet
sich eine zeitliche Vermischung der massgeblichen Umstände mit Ereignissen aus anderen Zeitperioden
(BGE 139 I 72, Publigroupe, E.9.2.2; Rz. 560 der Verfügung
der Vorinstanz vom 9. Mai 2016 in Sachen Sport im Pay-TV [veröffentlicht
in: RPW 2016/4 S. 920 ff., 991 f.]).
8.2.7 Die
Vorinstanz grenzte den räumlich relevanten Markt vorliegend zutreffend national ab. Ihren Erwägungen
kann vollumfänglich gefolgt werden. Denn das Vorbringen der Beschwerdeführerinnen, Anbieter
könnten auch aus dem Ausland stammen und der Markt werde sich in Zukunft weiter öffnen, verfängt
nicht. Die Beschwerdeführerinnen folgern dies aus den Änderungen, die sich aufgrund der Revision
des HMG ergaben. Damit wollen sie jedoch eine nachträgliche Entwicklung berücksichtigt wissen.
Die neuen Bestimmungen des revidierten Heilmittelgesetzes traten erst per 1. Januar 2019 in Kraft
(s. oben E. 2.2.3).
Der Bundesrat hat zwar bereits am 7. November 2012 die Botschaft zur Revision des Heilmittelgesetzes
zuhanden des Parlamentes verabschiedet. Daraus kann aber vorliegend nichts gefolgert werden. Denn der
bundesrätliche Entwurf sah noch nicht die Zuständigkeit einer Stiftung für das Zugänglichmachen
der Arzneimittelinformationen vor, ebenso wenig die Berücksichtigung von internationalen Standards
bei Umfang und Struktur der Daten.
8.2.8 Die
mit der Revision des HMG verbundenen möglichen Änderungen auf dem Markt sind für die hier
massgebliche Zeitperiode von Ende September 2013 bis Mitte Mai 2016 somit nicht entscheidend. Eine allfällige
zukünftige Öffnung des Marktes in internationaler Hinsicht ist aus diesen Gründen vorliegend
nicht zu berücksichtigen. Der räumlich relevante Markt ist sowohl für veredelte, maschinenlesbare
Daten betreffend Medikamenteninformationen als auch für die Aufnahme und den Erhalt in elektronischen
Datensätzen betreffend Medikamenteninformationen national abzugrenzen.
8.3 Zeitlich
relevanter Markt
8.3.1 Im
Rahmen der zeitlichen Marktbestimmung ist zu klären,
während welcher Dauer bzw. zu welchem Zeitpunkt substituierbare Angebote im massgeblichen geografischen
Gebiet verfügbar bzw. nachgefragt sind. Der zeitliche Aspekt der Marktabgrenzung erlangt immer
dann Bedeutung, wenn Nachfrage oder Angebot jeweils lediglich während bestimmter Zeitspannen gegeben
sind (Urteile B-831/2011, SIX, E. 338; B-3618/2013, Hallenstadion,
E. 165; B-7633/2009, ADSL II, E. 302.; Stäuble/Schraner,
DIKE-KG, Art. 4 Abs. 2 N 115 f.).
8.3.2 Die
Klärung der zeitlichen Dimension des Marktes ist nicht immer notwendig. Im Normalfall darf von "Dauermärkten"
ausgegangen werden (Zirlick/Blatter/Bangartner, a.a.O.,
Rz. 31; vgl. auch Stäuble/Schraner, DIKE-KG, Art. 4 Abs. 2 N 115).
8.3.3 Bei
den vorliegend relevanten Märkten handelt es sich unbestrittenermassen um sogenannte "Dauermärkte",
weshalb an sich keine Abgrenzung des zeitlich relevanten Marktes vorzunehmen wäre. Vorliegend ist
jedoch aufgrund des Wechsels der Muttergesellschaft der Beschwerdeführerin 2 und der Bejahung der
Passivlegitimation der Beschwerdeführerin 1 (vgl. E. 3.18)
der zeitliche relevante Markt auf den Zeitraum bis zum 7. April 2017 zu beschränken.
8.4 Zwischenergebnis
Aufgrund der vorstehenden Feststellungen ist für die Ermittlung der Marktstellung der Beschwerdeführerinnen
der Markt für veredelte, maschinenlesbare Daten betreffend Medikamenteninformationen in der Schweiz
sowie der Markt für die Aufnahme und den Erhalt in elektronischen Daten-sätzen betreffend Medikamenteninformationen
in der Schweiz während des massgeblichen Zeitraums zugrunde zu legen.
9. Marktstellung
9.1 Grundlagen
9.1.1 Nach
Art. 4 Abs. 2 KG gelten als marktbeherrschende Unternehmen einzelne oder mehrere Unternehmen, die auf
einem Markt als Anbieter
oder Nachfrager in der Lage sind, sich von anderen Marktteilnehmern
(Mitbewerbern, Anbietern oder Nachfragern) in wesentlichem Umfang unabhängig zu verhalten, insbesondere
wenn diese keine zumutbaren Ausweichmöglichkeiten haben; entscheidend ist die Möglichkeit des
unabhängigen Verhaltens eines Unternehmens in einem bestimmten Markt (BGE 139 I 72,
Publigroupe, E. 9.3.1 m.H. auf BGE 129 II 497 E. 6.3.1; Urteil
2C_113/2017, Hallenstadion, E. 5.5.1; Roger
Zäch, Verhaltensweisen marktbeherrschender Unternehmen, in: von Büren/David, Schweizerisches
Immaterial- und Wettbewerbsrecht, Kartellrecht, 2000, S. 172; Roland Köchli/Philippe
M. Reich in: Baker & McKenzie, Stämpflis Handkommentar SHK, Kartellgesetz, 2007, Art.
4 N 31 und 34; Stäuble/Schraner, DIKE-KG, Art. 4 Abs. 2 N 175).
9.1.2 Art.
4 Abs. 2 KG verlangt nicht, dass sich ein marktbeherrschendes Unternehmen von anderen Marktteilnehmern
vollständig unabhängig verhalten kann, sondern dass sie sich von anderen Marktteilnehmern nur
in wesentlichen Umfang unabhängig verhalten können (BGE 139 I 72, Publigroupe,
E. 9.3.3.2; Urteil B-831/2011, SIX, E. 405). Die Fähigkeit
eines Unternehmens zu einem in wesentlichem Umfang unabhängigen Verhalten äussert sich in einem
besonderen Verhaltensspielraum gegenüber anderen Marktteilnehmern, der es ihm zumindest ermöglicht,
auf bestehende Wettbewerbsbedingungen keine Rücksicht nehmen zu müssen, um beachtenswerte Nachteile
zu vermeiden, oder der es ihm darüberhinausgehend ermöglicht, die Wettbewerbsbedingungen immerhin
merklich zu beeinflussen oder sogar zu bestimmen. Ein solch besonderer Verhaltensspielraum besteht hingegen
regelmässig nicht, wenn ein Unternehmen durch ausreichenden Wettbewerbsdruck in seinem Verhalten
diszipliniert wird (BGE 139 I 72, Publigroupe, E. 9.3.1;
Urteile B-831/2011, SIX, E. 402;
B-7633/2009,
ADSL II, E. 311; B-2977/2007, Publigroupe,
E. 6.1; Roger Zäch,
Schweizerisches Kartellrecht, 2. Aufl. 2005, Rz. 532 und 572; Stäuble/Schraner,
DIKE-KG, Art. 4 Abs. 2 N 172).
9.1.3 Ob
eine marktbeherrschende Stellung besteht, ist im Einzelfall mit Blick auf die konkreten Verhältnisse
auf dem relevanten Markt zu entscheiden (BGE 139 I 72, Publigroupe,
E. 9.3.1 m.w.H.). Massgebend für die Beurteilung der Stellung eines Unternehmens auf dem relevanten
Markt ist eine wertende Beurteilung aller relevanten Aspekte, die im Einzelfall für
oder
gegen die Möglichkeit eines unabhängigen Verhaltens sprechen (Urteil 2C_113/2017, Hallenstadion,
E. 5.5.1). Im Rahmen einer derartigen Gesamtanalyse kommt keinem der prinzipiell zu berücksichtigenden
Aspekte ein absoluter Vorrang aufgrund allgemeiner Umstände zu. Wesentliche Grundlage dieser Beurteilung
bildet vielmehr eine Untersuchung der Marktstruktur, bei der regelmässig die Aspekte des aktuellen
Wettbewerbs, des potentiellen Wettbewerbs, der Stellung der Marktgegenseite sowie des Einflusses eines
zusammenhängenden Markts zu beachten sind. Des Weiteren sind im Hinblick auf die Unternehmensstruktur
spezifische Merkmale und Eigenschaften des jeweiligen Unternehmens abzuklären, die es ihm gerade
ermöglichen, sich unabhängig von anderen Marktteilnehmern zu verhalten (Urteile B-831/2011,
SIX, E. 403 f.; B-7633/2009, ADSL
II, E. 312).
9.1.4 Die
Gründe für die Entwicklung einer marktbeherrschenden Stellung sind für die kartellrechtliche
Beurteilung nach Art. 7 KG unerheblich (Urteile B-831/2011, SIX,
E. 404; B-7633/2009, ADSL II, E. 313). Daher ist es nicht
von Bedeutung, ob ein marktbeherrschendes Unternehmen seine kartellrechtlich relevante Macht aufgrund
besserer Leistung im Wettbewerb oder durch organisatorische Massnahmen erlangt hat (Heizmann,
a.a.O., Rz. 300; Stäuble/Schraner, DIKE-KG,
Art. 4 Abs. 1 N 181).
9.2 Markt
für veredelte, maschinenlesbare Daten betreffend Medikamenteninformationen
9.2.1 Aktueller
Wettbewerb
im relevanten Zeitraum
9.2.1.1 Unter
dem Gesichtspunkt des aktuellen Wettbewerbs ist festzustellen, in welchem Ausmass das betreffende Unternehmen
unmittelbar einem Wettbewerbsdruck durch Konkurrenten, die bereits tatsächlich auf dem relevanten
Markt tätig sind, ausgesetzt ist (Urteil B-831/2011, SIX,
E. 423).
9.2.1.2 Die
Vorinstanz führte aus, e-mediat sei bis 2012 mit Galdat die einzige Anbieterin einer umfassenden
veredelten und maschinenlesbaren Datenbank für Medikamenteninformationen gewesen. Datenangebote
anderer Anbieter mit vergleichbaren Funktionalitäten seien weder früher noch heute verfügbar.
Die aktuelle Konkurrenz durch ouwerkerk und ywesee sei nicht genügend gross um einen disziplinierenden
Einfluss auf HCI zu haben.
9.2.1.3 Weiter
erwog die Vorinstanz, Documed sei in einem Schreiben vom Januar 2012 selbst davon ausgegangen, mit den
INDEX-Produkten über eine Marktabdeckung von mehr als 90% zu verfügen. Es sei anzunehmen, dass
die restlichen 10% damals noch nicht auf Softwarelösungen umgestiegen seien und dieser Anteil im
Entscheidzeitpunkt kleiner sei. Zudem würden die Zahlen der Leistungserbringerinnen und -erbringer,
Vertriebsunternehmen und Kostenträger, die mit HCI zusammenarbeiteten, in Relation gesetzt zu den
absoluten Zahlen der in der in der Schweiz tätigen Ärztinnen und Ärzte, Apotheken, etc.
die Marktbeherrschung der Beschwerdeführerinnen auf dem Markt für veredelte, maschinenlesbare
Daten betreffend Medikamenteninformationen bestätigen. Entsprechend sei, wenn, dann nur sehr eingeschränkter
aktueller Wettbewerb vorhanden.
9.2.1.4 Die
Beschwerdeführerinnen machen geltend, mit ywesee sei eine aktuelle Konkurrentin vorhanden. Diese
habe mit dem Produkt MEDIupdate XML in den Ärztemarkt einsteigen können, auch wenn die Qualität
ihrer Daten - unter anderem aufgrund der fehlenden Fachredaktion - nicht mit jener von HCI
vergleichbar sei. Zudem hätten die von ouwerkerk angebotenen Stammdaten, welche in Konkurrenz zu
den INDEX-Produkten gestanden hätten, bei einer grösseren Investition Potenzial gehabt, das
Angebot von HCI unter Druck zu setzen.
9.2.1.5 Ausgangspunkt
für die Prüfung des aktuellen Wettbewerbs bildet der Marktanteil des betreffenden Unternehmens.
Hohe Marktanteile sind nach bundesgerichtlicher Rechtsprechung ein starkes Indiz für eine marktbeherrschende
Stellung, sie schliessen einen wirksamen Wettbewerb aber nicht zwangsläufig aus (BGE 139 I 72, Publigroupe,
E. 9.3.3.2; 130 II 449 E. 5.7.2; Urteil B-831/2011, SIX, E. 440).
9.2.1.6 Daher
sind zudem insbesondere folgende Aspekte ebenfalls zu beachten: (i) die Anzahl der Konkurrenten, (ii)
die Marktanteile der Konkurrenten, (iii) das Verhältnis zwischen dem Marktanteil des betreffenden
Unternehmens und den Marktanteilen der Konkurrenten, sowie (iv) die Entwicklung der Marktanteile. Je
grösser der Abstand zwischen dem Marktanteil des betreffenden Unternehmens und den Marktanteilen
seiner Konkurrenten ist bzw. je kleiner die Marktanteile der Konkurrenten sind, umso eher ist dabei von
einer marktbeherrschenden Stellung auszugehen (Urteile
B-831/2011, SIX,
E. 439; B-7633/2009, ADSL II, E. 331; Reinert/Wälchli,
BSK-KG, Art. 4 Abs. 2 N 275; Weber/Volz, a.a.O., Rz. 2.55).
Hohe stabile Marktanteile sprechen grundsätzlich für eine marktbeherrschende Stellung, während
volatile Marktanteile und gesunkene Marktanteile des untersuchten Unternehmens eher dagegensprechen (Reinert/Wälchli,
BSK-KG, Art. 4 Abs. 2 N 276). Sinkende Marktanteile des jeweiligen Unternehmens schliessen die Feststellung
einer Marktbeherrschung allerdings dann nicht aus, wenn der Marktanteil immer noch hoch bleibt (BGE 139
I 72, Publigroupe, E. 9.3.3.2; Urteil B-831/2011, SIX,
E. 447; Evelyn Clerc/Pranvera Këllezi, in: Martenet/Bovet/Tercier
[Hrsg.], Commentaire Romand, Droit de la concurrence, 2. Aufl. 2013, Art. 4 Abs. 2 N 276 [nachfolgend
zit.: {Autor}, CR-Concurrence]).
9.2.1.7 Schliesslich
zu berücksichtigen ist die Wirtschaftskraft der Konkurrenten. In diesem Zusammenhang erlangt regelmässig
auch die Unternehmensstruktur des betreffenden Unternehmens Bedeutung (Urteil
B-7633/2009,
ADSL II, E. 331). Aus all diesen Aspekten ist zu schliessen,
ob die Konkurrenten in der Lage sind, einen disziplinierenden Einfluss auf das betreffende Unternehmen
auszuüben.
9.2.1.8 Marktanteile
können unterschiedlich ausfallen, je nachdem, ob auf den Umsatz, Stück bzw. Mengenangaben oder
die Anzahl Kunden abgestellt wird (Reinert/Wälchli,
BSK-KG, Art. 4 Abs. 2 N 295). Ein Abstellen auf den Umsatz ist vorliegend insbesondere aufgrund des Fehlens
von genügendem Zahlenmaterial nicht möglich. Es liegen jedoch zahlreiche Angabe betreffend
Anzahl Nutzer bzw. Installationen und Verträge vor.
9.2.1.9 Bereits
im Januar 2012 ging HCI im Rahmen der Offertstellung im Hinblick auf die Übergangsverträge
für das Jahr 2012 davon aus, mittels ihrer INDEX-Datenbanken über eine Marktabdeckung von mehr
als 90% bei den Softwaresystemen der Leistungserbringerinnen und -erbringer zu verfügen (vgl. Vorinstanz,
act. 347, S. 9 und 12). Es würden mit mehr als 110 Softwarehäusern Verträge bestehen und
es gäbe mehr als 11'000 Installationen von medINDEX, mehr als 120 Installationen von hospINDEX
sowie mehr als 1700 Installationen von pharmINDEX. Schliesslich würden mehr als 90% der Kostenträger
insureINDEX nutzen (vgl. Vorinstanz, act. 347, S. 13).
9.2.1.10 Der
Präsentation des neuen Leistungsangebots von HCI im September 2012 lässt sich entnehmen, dass
HCI damals davon ausging, dass mit 115 Softwarehäusern Verträge bestünden und die INDEX-Produkte
wie folgt genutzt würden (vgl. Vorinstanz, act. 54 und 357, S. 22):
- medINDEX
von 16'000 Praxisärztinnen und -ärzten (geschätzt)
- pharmINDEX
von 1730 Apotheken
- drogINDEX
von 430 Drogerien
- hospINDEX
von 200 Spitälern
- careINDEX
von 80 Heimen
- insureINDEX
von 63 Krankenkassen
- logINDEX
von 20 Grossisten.
9.2.1.11 In
der Broschüre "Das Netzwerk für Ihre Produkte, Dienstleistungen und Preise 2017",
führt HCI auf, dass die INDEX-Produkte von 16'000 Arztpraxen, 1700 Apotheken, 320 Spitäler,
320 Drogerien, 180 Heimen und Spitex, 55 Kostenträgern und 20 Grossisten genutzt würden (vgl.
Vorinstanz, act. 1025, S. 4).
9.2.1.12 All
diese Zahlen zeigen eine relativ konstant bleibende, grosse Anzahl Nutzer bzw. Installationen und Verträge
mit HCI betreffend die INDEX-Datenbanken. Sie sprechen bereits für einen erheblichen Marktanteil
von HCI, selbst wenn dabei berücksichtigt wird, dass sie von HCI selbst im Rahmen von Werbetätigkeiten
veröffentlich wurden und deshalb mit einer gewissen Vorsicht zu betrachten sind.
9.2.1.13 Diese
Zahlen betreffend Nutzerinnen und Nutzer können mit der Gesamtanzahl der in der Schweiz tätigen
Leistungserbringerinnen und
-erbringer in Relation gesetzt werden. Bei Letzteren gilt
jedoch zu berücksichtigen, dass es sich um die absoluten Zahlen, der in den entsprechenden Branchen
tätigen Personen und Unternehmen handelt. Es ist davon auszugehen, dass ein Teil - auch wenn
es sich dabei wohl um eine deutliche Minderheit handelt - im relevanten Zeitraum noch nicht auf
digitalisierte Lösungen bzw. Softwarelösungen umgestellt hat. Letztere können bei der
Beurteilung des Marktanteils nicht berücksichtigt werden, da sie im aktuellen Wettbewerb keine Nachfrager
für veredelte, maschinenlesbare Daten darstellen. Dennoch lässt sich aus den nachfolgenden
Zahlen, wenn sie mit den oben genannten in Relation gesetzt werden, schliessen, dass die Beschwerdeführerinnen
sowohl zu Beginn des fraglichen Zeitraumes als auch an dessen Ende über einen erheblichen Marktanteil
verfügten.
9.2.1.14 Den
Statistiken des Bundesamtes für Statistik (BFS) und des Bundesamtes für Gesundheit (BAG) können
betreffend Gesamtanzahl von Ärztinnen und Ärzte, die in einer freien Praxis tätig sind,
Apotheken, Spitälern und Krankenkassen folgende Zahlen entnommen werden (www.bfs.admin.ch/bfs/de/home/statistiken/gesundheit/gesundheitswesen/arztpraxen.
assetdetail.10527135.html;
https://www.bfs.admin.ch/bfs/de/home/statistiken/gesundheit/gesundheitswesen/spitaeler.assetdetail.10647165.html;
www.bag.admin.ch/bag/de/home/zahlen-und-statistiken/statistiken-zur-krankenversicherung/statistik-der-obligatorischen-krankenversicherung.
html
[abgerufen am 24.08.2020]):
- Ärztinnen
und Ärzte: 16'910
(2012)18'473
(2016)
- Apotheken:1'740
(2012)1'792
(2016)
- Spitäler:298
(2012)283
(2016)
- Krankenkassen:61
(2012)56
(2016)
Somit nutzten zwischen 85%
(2016) und 95% (2012) aller Ärztinnen und Ärzte, zwischen 95%
(2016) und 99% (2012) aller Apotheken
sowie zwischen 90% (2016) und 100% (2012) aller Spitäler die
INDEX-Datenbanken. Bei den Zahlen betreffend
Krankenkassen bzw. Kostenträger ist zu berücksichtigen,
dass der insureINDEX auch den Unfall-
und Invalidenversicherungen angeboten wird. Praktisch 100% aller
Kostenträger nutzten folglich die INDEX-Datenbanken.
Gemäss den Angaben des Schweizerischen Drogistenverbandes (SDV) im Jahresbericht 2018 zählte
der Verband Anfang 2012 528 Mitglieder bzw. Anfang 2016 491 Mitglieder (S. 4, abrufbar unter: www.drogoserver.ch/deutsch/Verband/191129_DV_4_Jahresbericht_2018.pdf
[abgerufen am 24.08.2020]). Gemäss SDV sind über 90% aller Schweizer Drogerien Mitglied im
Verband (https://drogistenverband.ch/de/verband [abgerufen am 24.08.2020]). Somit ergibt sich, dass wohl
mindestens zwischen 59% (2016) und 73% (2012) aller Drogerien die INDEX-Datenbanken nutzten.
9.2.1.15 Auf
dem Markt für veredelte, maschinenlesbare Daten betreffend Medikamenteninformationen war im fraglichen
Zeitraum neben HCI ywesee mit dem Produkt MEDIupdate XML tätig. MEDIupdate XML wurde im fraglichen
Zeitraum nach Angaben von ywesee von rund [...] Ärztinnen und Ärzten genutzt. Bei den Apotheken
und Spitälern konnte ywesee nicht in den Markt eintreten (vgl. Vorinstanz, act. 1117, S. 6 und 12).
9.2.1.16 Weiter
war im fraglichen Zeitraum auch ouwerkerk mit dem Produkt just-medical!/med-drugs auf diesem Markt tätig.
Allerdings konnte gemäss Angaben von ouwerkerk trotz Akquise-Tätigkeiten kein Kunde für
just-medical!/med-drugs gefunden werden (vgl. Vorinstanz, act. 1103, S. 6). Weitere aktuelle Konkurrenten
sind weder ersichtlich, noch wird dies von Seiten der Beschwerdeführerinnen geltend gemacht.
9.2.1.17 MedINDEX
wird gemäss HCI von 16'000 Ärztinnen und Ärzten genutzt, MEDIupdate XML gemäss
ywesee von [...], was einem Marktanteil von ca. 5% entspricht. HCI verfügte mit medINDEX trotz
des Konkurrenzangebots von ywesee über einen Marktanteil von über 90%. Der Bereich medINDEX,
bei welchem der Vertrieb direkt über die Softwarehäuser erfolgte, ist für die Beschwerdeführerinnen
gemäss ihren Angaben in der Beschwerde von untergeordneter Bedeutung (S. 38 der Beschwerde). H.______
erklärte im Parteiverhör vom 27. Februar 2013 zudem, die Wertschöpfung im Arztmarkt sei
gering (vgl. Vorinstanz, act. 141, S. 8).
9.2.1.18 Bei
allen anderen Leistungserbringerinnen und -erbringern, Kostenträgern, Vertriebsunternehmen und Softwarehäusern
ist für HCI sogar noch von einem grösseren Marktanteil auszugehen. In diesen Bereichen ist
kein tatsächlicher Konkurrent ersichtlich. Leistungserbringerinnen und -erbringer, welche die INDEX-Datenbanken
nicht nutzten (s. oben E. 9.2.1.14)
sind wohl im fraglichen Zeitraum (noch) nicht auf digitalisierte Lösungen umgestiegen.
9.2.1.19 In
Sinne eines Zwischenfazits kann somit festgehalten werden, dass der Marktanteil der Beschwerdeführerinnen
insgesamt über 90% betrug und damit viel dafürspricht, dass sie im relevanten Zeitraum eine
marktbeherrschende Stellung innehatte. Selbst wenn gewisse sachverhaltliche Unklarheiten bestünden,
wäre die "kritische Schwelle" von 50% jedenfalls bei weitem überschritten (BGE 139
I 72, Publigroupe, E. 9.3.3.2; Urteil 2C_113/2017, Hallenstadion,
E. 5.5.2).
9.2.1.20 Aber
nicht nur der hohe Marktanteil, sondern auch die Aspekte der Anzahl Konkurrenten und deren Marktanteile
sowie die Entwicklung der Marktanteile sprechen für eine marktbeherrschende Stellung.
9.2.1.21 Wie
erwähnt gab es auf dem relevanten Markt zwei aktuelle Konkurrenten, wobei der Marktanteil von ouwerkerk
0% und jener von ywesee auf dem Ärztemarkt etwas mehr als 5% betrug. Auf dem gesamten Markt ist
der Marktanteil von ywesee jedoch ebenfalls verschwindend klein und der Unterscheid zwischen den Marktanteilen
von HCI und ywesee sehr gross.
9.2.1.22 Die
Zahlen unter E. 9.2.1.10
f. und 9.2.1.14
zeigen zudem, dass die Entwicklungen der Marktanteile relativ stabil waren. Soweit die Marktanteile leicht
gesunken sind, schliesst dies die Feststellung der Marktbeherrschung nicht aus, da die Marktanteile hoch
blieben (s. oben E. 9.2.1.6).
9.2.1.23 Das
Vorbringen der Beschwerdeführerinnen, die von ouwerkerk angebotenen Stammdaten hätten bei einer
grösseren Investition Potenzial gehabt, HCI unter Druck zu setzen, ist im Rahmen der Beurteilung
des aktuellen Wettbewerbs nicht stichhaltig. Denn bei der Beurteilung des aktuellen Wettbewerbs sind
die effektiven Verhältnisse zu beurteilen und nicht hypothetische Annahmen, wie grössere Investitionen
oder grössere Wirtschaftskraft von Unternehmen. Betreffend die Wirtschaftskraft der beiden Konkurrenten
ywesee und ouwerkerk ist vielmehr festzuhalten, dass es sich bei beiden Unternehmen um Kleinstunternehmen
handelt.
9.2.1.24 Insgesamt
ist die Vorinstanz somit zu Recht davon ausgegangen, dass auf dem Markt für veredelte, maschinenlesbare
Daten betreffend Medikamenteninformationen, wenn überhaupt, dann nur sehr eingeschränkter aktueller
Wettbewerb vorhanden war.
9.2.2 Potentieller
Wettbewerb
9.2.2.1 Unter
dem Gesichtspunkt des potentiellen Wettbewerbs ist zu untersuchen, in welchem Ausmass das in Frage stehende
Unternehmen mittelbar einem Wettbewerbsdruck ausgesetzt ist durch die Möglichkeit, dass andere Unternehmen,
die dort bislang noch nicht tätig waren, auf dem relevanten Markt als neue Konkurrenten auftreten
könnten. Allein die Möglichkeit eines Markteintritts von weiteren Konkurrenten kann unter gewissen
Voraussetzungen eine disziplinierende Wirkung auch auf ein Unternehmen ausüben, dem aufgrund des
aktuellen Wettbewerbs eine besondere Stellung am Markt zukommt (Urteile B-831/2011, SIX,
E. 459;
B-7633/2009, ADSL II, E. 334;
Reinert/Wälchli, BSK-KG, Art. 4 Abs. 2
N 311 und 342 ff.; Stäuble/Schraner, DIKE-KG,
Art. 4 Abs. 2 N 233).
9.2.2.2 Die
Vorinstanz kam zum Schluss, es bestehe keine potentielle Konkurrenz, welche einen disziplinierenden Einfluss
habe. Zur Begründung führte sie insbesondere aus, ywesee versuche schon seit längerem
HCI zu konkurrieren, was ihr nur im Bereich der Ärztinnen und Ärzte als Nischenanbieterin gelungen
sei. Weiter berücksichtigte die Vorinstanz, dass aufgrund der nationalen Gesetzgebung im Gesundheitswesen
und betreffend die Arzneimittelinformationen Markteintritte von internationalen Unternehmen unwahrscheinlich
seien. Die vom Parlament verabschiedete Revision des Heilmittelgesetzes werde zudem wesentliche Änderungen
zur Folge haben. Insbesondere würden entscheidende Aufgaben einer Stiftung übertragen werden.
Diverse Fragen betreffend die Umsetzung seien aber noch offen. Bis zur deren Klärung seien Investitionen
unwahrscheinlich.
9.2.2.3 Gemäss
der Vorinstanz würden auch nachfolgende Hindernisse, die die Vorinstanz bereits als Faktoren gegen
den aktuellen Wettbewerb aufführte, gegen Änderungen der Wettbewerbsverhältnisse sprechen:
Erstens habe die Galenica-Gruppe die Wertschöpfungskette des Vertriebs der Arzneimittel und der
entsprechenden Medikamenteninformationen vertikal integriert und sei auf allen Marktstufen - teilweise
mit starker Marktstellung - tätig. Insbesondere der physische Vertrieb von Arzneimitteln sei
von Galenica-Gruppengesellschaften abhängig, denn der grösste Prewholesaler, Alloga AG, und
der grösste Grossist, Galexis AG, würden zur Galenica-Gruppe gehören. Zweitens verfüge
HCI mit den Einnahmen von den Zulassungsinhaberinnen über ein Vielfaches an finanziellen Mitteln
als andere Wettbewerber. Drittens sei die Markstellung von HCI seit langem gewachsen. HCI sei aufgrund
ihrer Geschäftsbeziehungen zu den Zulassungsinhaberinnen, Softwarehäusern und Abnehmern der
INDEX-Datenbanken und des Compendiums sowie aufgrund des Umstandes, dass nahezu alle outgesourcten Primärdaten
von ihr betrieben würden, ein unverzichtbarer Partner im Gesundheitswesen. Viertens sei der Umfang
der Datenbank von HCI nicht leicht reproduzierbar. Fünftens sei der Vertrieb an oder über Softwarehäuser
für andere Anbieter erschwert, da alle bestehenden Softwarehäuser mit HCI zusammenarbeiten
würden und keine anderen Schnittstellen vorhanden seien. Die Wechselkosten seien hoch und die Verwendung
der Datenbankstruktur für andere Datenbanken sei den Softwarehäusern teilweise vertraglich
untersagt. Sechstens müssten die Softwarehäuser die hohen Kosten, die bei der Umstellung von
Galdat auf die INDEX-Produkte entstanden seien, erst amortisieren.
9.2.2.4 Demgegenüber
stellen sich die Beschwerdeführerinnen auf den Standpunkt, dass potentielle Konkurrenz vorhanden
sei. Bei der Beurteilung des potentiellen Wettbewerbs sei zudem die vom Parlament verabschiedete Revision
des HMG und deren Auswirkungen zu berücksichtigen. Ebenfalls zu berücksichtigen seien die niedrigen
Sunk Costs und das Fehlen von erheblichen wettbewerbsrelevanten Switching Costs oder anderen Lock-in-Effekten.
Die Generierung der Datenbanken erfolge vor allem aufgrund des Vollständigkeitserfordernisses unter
den Bedingungen eines angreifbaren natürlichen Monopols. Schliesslich würden auf dem fraglichen
Markt Inventionen und Innovationen eine wichtige Rolle spielen. Die diversen Märkte für benutzergruppenspezifische
Arzneimittelinformationen hätten deshalb weitgehend den Charakter von ICT-(Software-)Märkten.
Auf solchen Märkten finde der Wettbewerb in der Regel in Form eines Forschungs- und Entwicklungswettbewerbs
"um den Markt", und nicht in Form eines "Wettbewerbs im Markt" statt.
9.2.2.5 Eine
Berücksichtigung der Möglichkeit eines Markteintritts von weiteren Marktteilnehmern als Konkurrenten
rechtfertigt sich nur dann, wenn der Markteintritt mit hinreichender Wahrscheinlichkeit innerhalb eines
absehbaren Zeitraums durch andere Unternehmen mit hinreichender Konkurrenzwirkung erfolgt (Urteile B-831/2011,
SIX, E. 462; B-7633/2009, ADSL
II, E. 339; Weber/Volz, a.a.O., Rz. 2.76; Stäuble/Schraner,
DIKE-KG, Art. 4 Abs. 2 N 233).
9.2.2.6 Eine
hinreichende Wahrscheinlichkeit für den Markteintritt eines Konkurrenten ist dann gegeben, wenn
aufgrund konkreter wirtschaftlicher, technischer oder sonstiger Anhaltspunkte mit einem entsprechenden
Markteintritt zu rechnen ist. Hingegen stellt allein die theoretische Möglichkeit eines Markteintritts
keine ausreichende Grundlage für eine solche Annahme dar (Urteile B-831/2011, SIX,
E. 463; B-7633/2009, ADSL II, E. 340). Neben einer prospektiven
Schätzung ist hierbei auch die historische Entwicklung der Markteintritte zu berücksichtigen
(Urteil
B-7633/2009, ADSL II, E. 341; Reinert/Wälchli,
BSK-KG, Art. 4 Abs. 2 N 343; Weber/Volz,
a.a.O., Rz. 2.76).
9.2.2.7 Besondere
Beachtung ist zudem den bestehenden Marktzutritts- und Marktaustrittsschranken und der Beurteilung deren
Höhe zu schenken. Dabei handelt es sich um alle Kriterien, die in Bezug auf eine erfolgreiche Etablierung
des jeweiligen Produkts auf dem Markt im Einzelfall bei sachgerechter Würdigung für oder gegen
die Aufnahme des Produktabsatzes im betreffenden Markt und - falls der Markteintritt nicht erfolgreich
gestaltet werden kann - im Rahmen eines darauffolgenden Marktaustritts von einem Unternehmen zu
berücksichtigen sind (Urteile B-831/2011, SIX, E. 464;
B-7633/2009,
ADSL II, E. 341). Marktzutrittsschranken entstehen durch Kosten,
welche ein Unternehmen bei einem Marktzutritt zu tragen hat, die das sich bereits im Markt befindliche
Unternehmen nicht hat (Weber/Volz, a.a.O., Rz. 2.62). Es
handelt sich um Faktoren wie Skalenvorteile und Verbundvorteile, die Notwendigkeit von Investitionen
für den Markteintritt, Produktdifferenzierung, regulatorische Faktoren wie Bewilligungspflichten,
Zölle oder Patente sowie Kostenvorteile der eingesessenen Firma, Netzwerkeffekte, Switching Costs,
Kosten für Beschaffung von Erfahrung und Know-how, Markentreue, etc. (Weber/Volz,
a.a.O., Rz. 264 ff.; Reinert/Wälchli, BSK-KG, Art.
4 Abs. 2 N 313 und 318 ff.). Unter Marktaustrittsschranken sind die Kosten zu verstehen, die bei einem
Marktaustritt entstehen. Das sind insbesondere sogenannte Sunk Costs, d.h. Investitionen, die bei einem
Marktaustritt verloren gehen, weil sie nicht anderweitig verwendet oder die entsprechenden Güter
nicht veräussert werden können (Weber/Volz, a.a.O.,
Rz. 263; Reinert/Wälchli, BSK-KG, Art. 4 Abs. 2 N 317).
9.2.2.8 Die
Voraussetzung des Markteintrittes innerhalb eines absehbaren Zeitraumes wird dann als erfüllt betrachtet,
wenn der Markteintritt rasch erfolgt, d.h. innerhalb von zwei bis drei Jahren (Reinert/Wälchli,
BSK-KG, Art. 4 Abs. 2 N 344; David/Jacobs, a.a.O., Rz. 699;
Weber/Volz, a.a.O., Rz. 2.76). Gemäss Stäuble/Schraner
muss der Marktzutritt bei der Beurteilung von Fällen nach Art. 7 KG innert kürzerer Frist,
d.h. innert weniger Monaten zu erwarten sein (Stäuble/Schraner,
DIKE-KG, Art. 4 Abs. 2 N 233). Der Zeitpunkt muss mit einiger Sicherheit abgeschätzt werden
können und der bis dahin verbleibende Zeitraum darf nicht so lang sein, dass dadurch dem potentiell
marktbeherrschenden Unternehmen die Möglichkeit eröffnet wird, in dieser Zeit seinen Verhaltensspielraum
noch in unangemessener Weise auszunutzen (Urteile B-831/2011, SIX,
E. 465;
B-7633/2009, ADSL II, E. 342).
9.2.2.9 Eine
hinreichende Konkurrenzwirkung setzt den Markteintritt eines oder mehrerer Unternehmen voraus, die alleine
oder zusammen das Angebot auf dem relevanten Markt in einem solchen Umfang erweitern, dass die Marktgegenseite
des potentiell marktbeherrschenden Unternehmens ausreichende Ausweichmöglichkeiten erhalten. Ausreichend
sind die Ausweichmöglichkeiten, wenn eine gewisse Anzahl an Marktteilnehmer die neuen Produkte erlangen
kann mit der Folge, dass das betreffende Unternehmen dieses Ausweichen nicht hinnehmen kann. Andernfalls
besteht für das betreffende Unternehmen keine Notwendigkeit für eine Änderung des eigenen
Verhaltens, weil die Marktgegenseite mangels tatsächlicher Alternativen auch weiterhin ganz überwiegend
auf die Abnahme seiner Produkte angewiesen ist (Urteile B-831/2011, SIX,
E. 466; B-7633/2009, ADSL II, E. 341).
9.2.2.10 Schliesslich
sind bei der Beurteilung der Markstellung auch die Merkmale und Eigenschaften des betreffenden Unternehmens
miteinzubeziehen. Im Rahmen dieser Unternehmensstrukturanalyse wird untersucht, welche individuellen
Merkmale und Eigenschaften eines Unternehmens diesem die Möglichkeit geben, sich unabhängig
von seinen Konkurrenten und Abnehmern zu verhalten (Urteil B-831/2011, SIX,
E. 470; Reinert/Wälchli, BSK-KG, Art. 4 Abs. 2 N 345;
Stäuble/Schraner, DIKE-KG, Art. 4 Abs. 2 N 250). Unternehmensmerkmale
und -eigenschaften, die eine marktbeherrschende Stellung indizieren können, sind beispielsweise
dessen technologischer bzw. kommerzieller Vorsprung gegenüber Konkurrenten, vertikale Integration,
Finanzkraft, Grösse, sein Marktverhalten sowie andere marktspezifische Eigenschaften (Urteile B-831/2011,
SIX, E. 470; B-7633/2009, ADSL
II, E. 350; Reinert/Wälchli, BSK-KG, Art. 4
Abs. 2 N 347 ff.; Clerc/Këllezi, CR-Concurrence, Art.
4 II N 129; Zäch, a.a.O., Rz. 584, 586 f.; Stäuble/Schraner,
DIKE-KG, Art. 4 Abs. 2 N 251).
9.2.2.11 Wie
nachfolgend zu zeigen ist, war vorliegend auf dem Markt für veredelte, maschinenlesbare Daten betreffend
Medikamenteninformationen im massgeblichen Zeitraum kein Eintritt eines weiteren Unternehmens mit ausreichender
Konkurrenzwirkung zu erwarten.
9.2.2.12 Bereits
die historische Entwicklung der Markteintritte spricht gegen eine hinreichende potentielle Konkurrenzentwicklung.
Ywesee versucht schon seit längerem in den Markt einzutreten, konnte sich jedoch nur als Nischenanbieterin
bei Ärztinnen und Ärzten etablieren, wobei sie auch in diesem Sektor lediglich über einen
Marktanteil von etwas mehr als 5% verfügt. Ouwerkerk versuchte ab 2012 ebenfalls in den Markt einzutreten,
was aber offensichtlich trotz finanzieller Unterstützung von Zulassungsinhaberinnen überhaupt
nicht gelang. Dass das Angebot von ouwerkerk bei grösseren Investition möglicherweise Potential
gehabt hätte, HCI unter Druck zu setzen - wie es von den Beschwerdeführerinnen geltend
gemacht wird - , stellt ebenfalls keinen konkreten Anhaltspunkt für die hinreichende Wahrscheinlichkeit
eines ausreichenden Konkurrenzangebots dar. Denn solche grösseren Investitionen wurden damals eben
gerade nicht getätigt und nachdem die Zulassungsinhaberinnen und ouwerkerk bereits damals nicht
mehr in das Konkurrenzprodukt von ouwerkerk investiert haben, erscheint es vor dem Hintergrund der Revision
des HMGs und der in diesem Zusammenhang bestehenden Unklarheiten (s. sogleich unten) unwahrscheinlich,
dass sie dies im hier relevanten Zeitraum machen würden.
9.2.2.13 Daneben
ist im Zusammenhang mit der historischen Entwicklung auch ein weiterer Aspekt zu berücksichtigen.
Bereits oben (s. Erw. C.a.d
f.) wurde dargelegt, dass die Zulassungsinhaberinnen aufgrund der Anordnungen von Swissmedic bis Juni
2011 faktisch verpflichtet waren, die Arzneimittelinformationen kostenpflichtig in der elektronischen
Sammlung von Documed zu publizieren, wobei ab 2008 auch eine elektronische Publikation bei der ywesee
möglich war. Erst ab Juli 2011 verzichtete Swissmedic darauf, von der Zulassungsinhaberin zu verlangen,
die Arzneimittelinformationen in einer dieser beiden elektronischen Sammlungen zu publizieren (vgl. Medienmitteilung
vom 26. Juli 2011, https://www.swissmedic.ch/swissmedic/de/home/news/mitteilungen/archiv/praxisaenderung-betreffend-die-publikation-von-arzneimittelinfor.html
[abgerufen am 07.01.2022]). Denn diese jahrelang andauernde Praxis stellte sich in BVGE 2011/60 als unzulässig
heraus. Das Bundesverwaltungsgericht kam zum Schluss, dass die von Swissmedic auferlegte Pflicht zur
Veröffentlichung der Arzneimittelinformationen bei einem von nur zwei privaten Anbietern nicht aufrechterhalten
werden dürfe. In Ermangelung einer klaren gesetzlichen Grundlage gehe es nicht an, dass Swissmedic
Firmen zum Abschluss eines kostenpflichtigen Vertrages mit Dritten verpflichte, deren Tarifgestaltung
nicht staatlich kontrolliert sei. Die Praxis von Swissmedic sei zur Erfüllung der Informationspflicht
weder geeignet noch notwendig. Durch den Vertragszwang werde zudem die Wirtschaftsfreiheit der Herstellerfirmen
beeinträchtigt. Mit der wachsenden Zahl staatlicher Aufgaben und ihrer zunehmenden Delegation an
Private könne das aktuelle Prozedere von Swissmedic nicht toleriert werden. Es sei nicht einsehbar,
weshalb Swissmedic die Informationen nicht selbst publiziere, zumal es ihr gesetzlich erlaubt sei, dafür
auch eine Entschädigung zu verlangen (BVGE 2011/60).
9.2.2.14 Zwar
soll gemäss Vorbringen der Beschwerdeführerinnen R._______ ein Produkt zur Substitution von
pharmINDEX entwickelt haben. So machen sie geltend, Ende 2016 von einem Mitarbeiter der R._______ erfahren
zu haben, dass R._______ ein Konkurrenzprodukt zum pharmINDEX entwickelt habe und dass dieses demnächst
auf den Markt gebracht werde (vgl. Beilage 7 zur Beschwerde). In der unaufgefordert eingereichten Eingabe
vom 16. November 2018 halten die Beschwerdeführerinnen später aber selbst fest, dass kein zusätzlicher
Drittanbieter von Daten in den Markt eingetreten sei und bestehende Anbieter ihren Marktanteil auch nicht
ausgeweitet hätten. Hinzukommt, dass der "Apotheken-Markt" bzw. pharmINDEX neben den anderen
sechs INDEX-Datenbanken für die anderen Leistungserbringerinnen- und erbringer bzw. Vertriebsunternehmen
und Kostenträgern auf dem hier relevanten Markt nur ein Teilangebot darstellt. Die ehemalige Galenica-Gruppe
und die heutige Galenica-Gruppe, zu welcher auch die Beschwerdeführerin 2 gehört, betrieb bzw.
betreibt im Geschäftssegment Products & Care nach eigenen Angaben das grösste Apothekennetzwerk
der Schweiz mit rund 360 Apotheken (eigene Apotheken und Joint-Venture-Apotheken; https://www.galenica.com/de/ueber-galenica/products-care/pharmacies.php
[abgerufen am 06.12.2021]). All diese Apotheken würden wohl nicht zu einem allfälligen Konkurrenzprodukt
wechseln. Auch unter Berücksichtigung dieser Aspekte wäre ein Markteintritt von R._______ mit
einem Konkurrenzprodukt für Apotheken in den nächsten zwei bis drei Jahren als Konkurrentin
mit hinreichender Konkurrenzwirkung für den gesamten relevanten Markt gegenüber allen Leistungserbringerinnen
und Leistungserbringer, Vertriebsunternehmen, Kostenträgern und Softwarehäusern, äusserst
fraglich.
9.2.2.15 R._______
ist bis heute mit keinem Konkurrenzprodukt in den Markt eingetreten. Weitere Markteintritte oder Ankündigungen
von solchen wurden weder geltend gemacht noch sind sie ersichtlich.
9.2.2.16 Die
Beschwerdeführerinnen wollen die Revision des HMG berücksichtigt wissen. Sie machen geltend,
die Zulassungsinhaberinnen müssten mit Inkrafttreten des neuen HMG die Basisdaten selber codieren
und strukturieren, womit sich der fragliche Markt stark verändern werde. Zudem werde ausländischen
Marktanbietern der Markteintritt erleichtert, da in Zukunft vermehrt auf internationale Standards abgestellt
werde.
9.2.2.17 Die
neue gesetzliche Regelung (Art. 67 nHMG) stellt unbestritten eine Änderung der gesetzlichen Rahmenbedingungen
dar. Solche Änderungen können einen Anhaltspunkt für potenzielle Konkurrenz darstellen.
Allerdings sind die zeitlichen Verhältnisse und Auswirkungen einzubeziehen. Vorliegend wurde 2012
die Botschaft an das Parlament überwiesen, 2016 die Revision vom Parlament verabschiedet und per
1. Januar 2019 trat Art. 67 nHMG in Kraft (s. oben E. 2.2.3).
Betreffend die hier interessierenden Änderungen waren die gesetzlichen Rahmenbedingungen und die
konkrete Ausgestaltung lange Zeit unklar; insbesondere auch noch nach Verabschiedung der Vorlage 2016
durch das Parlament. Bis zur Klärung der gesetzlichen Rahmenbedingungen und der konkreten Ausgestaltung
erscheint ein Markteintritt aber unwahrscheinlich. Insofern kann bereits aus diesem Grund die Revision
des HMG nur bedingt als Argument für potentiellen Wettbewerb herangezogen werden.
9.2.2.18 Art.
67 nHMG sieht vor, dass eine Stiftung ein elektronisches Verzeichnis mit den gesetzlich vorgeschriebenen
Inhalten der Arzneimittelinformationen betreibt. In diesem elektronischen Verzeichnis hat die Stiftung
die Arzneimittelinformationen vollständig und aktuell in strukturierter Form auf Kosten der Zulassungsinhaberinnen
zu veröffentlichen. Die Zulassungsinhaberinnen haben die Arzneimittelinformationen bereits in der
entsprechenden Form zu liefern (s. oben E. 2.2.3).
Weiter hat die Einrichtung gemäss Art. 67 Abs. 6 nHMG betreffend Umfang und Struktur der Daten soweit
möglich die internationalen Standards zu berücksichtigen. Dies stellt zwar eine Erleichterung
für den Markteintritt von internationalen Anbietern dar. Nichtsdestotrotz bleibt der Markt geprägt
von der nationalen Gesetzgebung im Gesundheitswesen und bezüglich Arzneimittelinformationen. Daneben
erschwert auch die in diesem Bereich in der Schweiz erforderliche Mehrsprachigkeit einen potentiellen
Markteintritt von internationalen Anbietern. Schliesslich wollte die Stiftung Refdata auch einen "nahtlosen
Übergang" sicherstellen und hat weiterhin HCI mit dem Betrieb der Publikationsplattform für
Humanarzneimittel beauftragt (s. oben E. 2.2.3).
9.2.2.19 Die
Vorinstanz hat zutreffend auf zahlreiche Hindernisse für den Markteintritt potenzieller Konkurrenten
hingewiesen (s. oben E. 9.2.2.3),
namentlich die vertikale Integration, die grösseren finanziellen Mittel von HCI durch die Einnahmen
von Seiten der Zulassungsinhaberinnen, die starke und vernetzte Stellung von HCI im Gesundheitswesen,
die erschwerte Reproduzierbarkeit des Umfanges der Datenbank sowie den erschwerten Vertrieb an oder über
Softwarehäuser. Hinzu kommt, dass ein Alternativangebot in ausreichendem Ausmass nur erfolgen kann,
wenn eine potentielle Konkurrentin erheblich in den Aufbau einer ebenfalls umfangreichen, vollständigen
und qualitativhochwertigen Datenbank investieren würde. Die Aufbereitung der Arzneimittelinformationen
für die INDEX-Datenbank ist gemäss den Beschwerdeführerinnen nämlich ein arbeitsintensiver
Prozess. Der durchschnittliche Aufwand für die Aufbereitung eines neuen Präparates der INDEX-Daten
betrage ca. [...] Stunden. Zudem muss eine IT-Infrastruktur zur Verfügung stehen.
9.2.2.20 Die
Beschwerdeführerinnen machen geltend, ein Konkurrent sei nur mit niedrigen Sunk Costs und vertraglichen
Bedingungen konfrontiert, da es für die Generierung ihrer Datenbanken keiner dedizierten, spezifischen
Produktionsfaktoren bedürfe, die beim Marktaustritt nicht zu Marktbedingungen anderen Verwendungszwecken
zugeführt werden könnten.
9.2.2.21 Versunkene
Kosten (engl. sunk cost) sind Kosten, die zu einem bestimmten Entscheidungszeitpunkt bereits entstanden
sind und sich (bspw. durch Verkauf) auch nicht mehr rückgängig machen lassen (N.
Gregory Mankiw, Principles of economics, Fort Worth: Dryden Press, 1998, S. 291). Der Begriff
umfasst sowohl Kosten, die bereits tatsächlich angefallen sind, als auch zukünftige Kosten,
die unwiderruflich anfallen werden. Das zentrale Merkmal von versunkenen Kosten ist, dass sie sich vom
Entscheidungsträger weder in der Gegenwart noch in der Zukunft beeinflussen lassen.
9.2.2.22 Die
Beschwerdeführerinnen führen nicht aus, welche "Produktionsfaktoren" ein möglicher
Konkurrent für die Entwicklung und den Betrieb einer Medikamenteninformationsdatenbank konkret benötigen
würde. Produktionsfaktoren sind all jene materiellen und immateriellen Elemente, die im betrieblichen
Leistungserstellungs- und Leistungsverwertungsprozess miteinander kombiniert werden (Jean-Paul
Thommen, Lexikon der Betriebswirtschaft, 4. Aufl., 2008, S. 529). Nebst der menschlichen Arbeit,
den langfristig zur Verfügung stehenden Betriebsmitteln (z.B. Maschinen, IT-Systeme, Betriebsgebäude)
und den sich in der Produktion verbrauchenden Werkstoffen (Rohstoffe, Hilfsstoffe, Betriebsstoffe) werden
insbesondere auch Information und Wissen als eigenständige Produktionsfaktoren betrachtet.
9.2.2.23 Vorliegend
dürften für den eigentlichen Betrieb der Datenbank vor allem Produktionsfaktoren benötigt
würden, die sich relativ einfach am Markt beschaffen lassen und bei einem allfälligen Marktaustritt
auch ohne nennenswerten Wertverlust einem anderen Verwendungszweck zugeführt werden können:
Ist das "informationstechnische Gerüst" einer Datenbank (die sog. Datenbankstruktur) einmal
erstellt und basiert dieses "Gerüst" auf einer gängigen Software, dürften für
den weiteren Betrieb kaum mehr hoch spezifische Informatikkenntnisse notwendig sein. Die tägliche
Arbeit mit der Datenbank setzt zwar voraus, dass sich das Betriebspersonal mit der verwendeten Software
vertraut macht. Da sich das angeeignete "Standardsoftwarewissen" jedoch auch ausserhalb des
aktuellen Arbeitsverhältnisses nutzen lässt, liegen kein eigentliches betriebsspezifisches
Humankapital und damit auch keine wirklichen Sunk Costs vor.
9.2.2.24 Dagegen
ist davon auszugehen, dass sowohl die Entwicklung, als auch der Aufbau einer konkurrierenden Datenbank
mit der Generierung von sehr spezifischem "Wissen" verbunden ist und sich dieses "Wissen"
bei einem Marktaustritt nur bedingt monetisieren lässt. Zudem ist es für einen potenziellen
Konkurrenten im Voraus kaum abschätzbar, ob und zu welchen Bedingungen, das - in diesem Zeitpunkt
erst noch zu entwickelnde - Datenbankgerüst ("Betriebsmittel") und die darin enthaltenen
Daten ("Informationen") bei einem späteren Marktaustritt überhaupt verkauft werden
können.
9.2.2.25 Für
die Entwicklung und den Aufbau einer konkurrierenden Medikamenteninformationsdatenbank sind damit vor
allem Produktionsfaktoren notwendig, die zu irreversiblen Kosten führen. Das pauschale Argument
der Beschwerdeführerinnen, für die Generierung einer konkurrierenden Datenbank bedürfe
es keiner dedizierten, spezifischen Produktionsfaktoren, die beim Marktaustritt nicht zu Marktbedingungen
anderen Verwendungszwecken zugeführt werden können, vermag demnach nicht zu überzeugen.
Ein Konkurrent müsste bei der Entwicklung und dem Aufbau erhebliche Sunk Costs in Kauf nehmen.
9.2.2.26 Weiter
machen die Beschwerdeführerinnen geltend, ihren Kunden würde bei einem Wechsel der verwendeten
Medikamenteninformationsdatenbank keine erhebliche wettbewerbsrelevante Switching Costs oder andere Lock-In-Effekte
entstehen.
9.2.2.27 Mit
dem Begriff Wechselkosten (engl. switching costs) werden die Transaktionskosten bezeichnet, die einem
Nachfrager durch den Wechsel auf ein anderes, funktional identisches Produkt (bzw. auf eine andere, funktional
identische Dienstleistung) des bisherigen oder eines anderen Anbieters entstehen (Paul
Klemperer, Competition when Consumers Have Switching Costs: An Overview with Applications to Industrial
Organization, Macroeconomics, and International Trade, Review of Economic Studies, 62 (4) [1995], S.
515-539). Wechselkosten müssen nicht zwingend monetärer Natur sein. Sie können ebenso
im administrativen Aufwand, der mit einem Wechsel verbunden ist, oder in den spezifischen Lernkosten,
die für die Nutzung eines neuen Produkts bzw. einer neuen Dienstleistung zu erbringen sind, begründet
sein. Im Bereich der Informations- und Kommunikationstechnologie (ICT) führt vor allem das Erfordernis
der durchgehenden Kompatibilität der eingesetzten ICT-Komponenten zu Wechselkosten. Wechselkosten
bilden sodann die Basis für den sogenannten Lock-In-Effekt. Dieser beschreibt das Phänomen,
dass ein Kunde neue Produkte bzw. Dienstleistungen von seinem angestammten Anbieter bevorzugt, obwohl
auf dem Markt bereits günstigere Alternativen vorhanden und auch erprobt sind - und diese
Alternativen technisch allenfalls auch überlegen wären. Der Grund für dieses Phänomen
ist die Tatsache, dass ein Anbieterwechsel für einen Kunden nur dann sinnvoll ist, wenn der durch
den Wechsel entstehende Nutzenzuwachs grösser oder zumindest gleich gross ist, wie die durch den
Wechsel verursachten Kosten.
9.2.2.28 HCI
lässt die von ihr veredelten Medikamenteninformationen als maschinenlesbare Codes in die Informatiksysteme
ihrer Kunden einfliessen. Hierzu nutzt sie einen proprietären Standard, der von anderen Unternehmen
nicht mitverwendet werden könnte. Das hat zur Folge, dass ein Anbieter von einer konkurrierenden
Medikamenteninformationsdatenbank seine Daten nicht einfach so anstelle von HCI in die bei den Kunden
bereits vorhandene Softwareapplikationen einspeisen könnte. Um eine Alternative zu den INDEX-Produkten
zu nutzen, wäre kundenseitig vielmehr eine Anpassung der verwendeten, möglicherweise aber auch
die Anschaffung einer neuen Software nötig. Ein Softwarewechsel führt neben den monetären
Anpassungs- bzw. Neuanschaffungskosten zu weiteren Wechselkosten. Bei Neueinführung einer Software
entstehen einem Unternehmen unter anderem Kosten für die Schulung der Mitarbeiter sowie für
die technische und organisatorische Integration in den bestehenden Geschäftsprozess. Ist die Software
eine bestimmte Zeit lang genutzt worden, haben Systemtechniker die Software in der Regel auf Hardware,
Netzwerke, Datenbanken etc. abgestimmt. Für die Nutzung der Software sind allenfalls auch eigene
Hilfsprogramme erstellt worden. Auf jeden Fall werden sich die Anwender bestimmt "Tricks" im
Umgang mit der Software angeeignet und sich an die neuen Benutzerschnittstellen gewöhnt haben. Da
all diese Aufwendungen systemspezifisch sind, müssten sie bei einem Wechsel zu einem konkurrierenden
Softwareprodukt erneut erbracht werden. Demnach besteht vorliegend eine Wechselkostenproblematik.
9.2.2.29 Sodann
räumen die Beschwerdeführerinnen in ihrer Beschwerde selber ein, dass in sogenannten ICT-Märkten
in einem gewissen Ausmass immer solche Schranken bestehen. Falls die Beschwerdeführerinnen mit diesem
Hinweis auf eine angebliche "Wechselkosten-Normalität" auf ICT-Märkten zum Ausdruck
bringen möchte, dass die Wechselkosten vorliegend produkt- bzw. dienstleistungsimmanent seien und
deshalb bei der Beurteilung der Marktstellung keine Berücksichtigung finden dürfen, geht sie
jedoch fehl. Denn für die Verhaltenskontrolle nach Art. 7 KG ist es unerheblich, aus welchem
Grund, ein ins Recht zu fassendes Unternehmen als marktbeherrschend qualifiziert wird. Insbesondere braucht
es keinen Nachweis, dass das Unternehmen durch ein aktives Zutun zur Entstehung seiner marktbeherrschenden
Stellung beigetragen hat (vgl. oben E. 9.1.4
m.H.).
9.2.2.30 Soweit
die Beschwerdeführerinnen in diesem Zusammenhang schliesslich Bezug auf das Gutachten "Grundlagenanalyse
Stammdaten" von S._______ (vgl. Vorinstanz, act. 1070, Beilage 14) nehmen, ist festzuhalten,
dass dieses nicht das Vorhandensein von potentiellem Wettbewerb untersucht, sondern die beiden Stammdatenprovider
e-mediat mit "hospINDEX advanced" und ouwerkerk mit "med-drugs xml basic" mittels
einer quantitativen Inhaltsanalyse vergleicht und sie auf ihre Substitutionsfähigkeit hin untersucht.
Dem Gutachten liegt folgende Fragestellung zu Grunde: "Welche Auswirkungen kann ein Strategiewechsel
der Pharmafirmen auf Schweizer Spitäler, hinsichtlich der Verfügbarkeit von Pharmazeutischen
Stammdaten haben, wenn aufgrund des Entscheides des Bundesverwaltungsgerichts vom Juni 2011, die Zusammenarbeit
mit e-mediat nicht weiter verfolgt wird". Aus dem blossen Vergleich der zwei Datenbanken kann somit
nicht auf das Fehlen von Switching Costs geschlossen werden.
9.2.2.31 Weiter
bringen die Beschwerdeführerinnen vor, die Generierung der hier interessierenden Datenbanken erfolge
vor allem aufgrund des Vollständigkeitserfordernisses unter den Bedingungen eines angreifbaren natürlichen
Monopols. Daraus leiten die Beschwerdeführerinnen ab, ihr als Anbieterin von veredelten Daten könne
deshalb bereits aus modelltheoretischen Gründen keine marktbeherrschende Stellung zu kommen.
9.2.2.32 Ein
natürliches Monopol liegt vor, wenn ein einzelnes Unternehmen einen Markt zu niedrigeren Kosten
mit Gütern oder Dienstleistungen versorgen kann, als dies zwei getrennten Unternehmen, mit dem gleichen
Wissensstand und unter Verwendung von derselben Technologie, möglich wäre (Mankiw,
a.a.O., S. 306 f.).
9.2.2.33 In
der Regel sind für die Entwicklung digitaler Güter sehr hohe Anfangsinvestitionen notwendig,
währendem die Vervielfältigung günstig bzw. zum Teil nahezu kostenlos ist. Deshalb werden
die Durchschnittskosten immer geringer, je öfter digitale Güter verkauft werden. Da sich die
hohen Fixkosten auf immer mehr Einheiten verteilen, kann ein einzelner Anbieter einen ICT-Software-Markt
zu geringeren Kosten mit demselben digitalen Gut versorgen als dies mehrere parallele Anbieter tun könnten.
Diese Produktionsbedingungen begünstigen das Entstehen natürlicher Monopole (vgl. Reiner
Clement/Dirk Schreiber/Paul Bossauer/Christina Pakusch, Internet-Ökonomie: Grundlagen und
Fallbeispiele der digitalen und vernetzten Wirtschaft, 4. Aufl., 2019, S. 63 ff. und 240).
9.2.2.34 Der
abgegrenzte relevante Markt für veredelte maschinenlesbare Daten betreffend Medikamenteninformationen
weist Merkmale eines natürlichen Monopols auf. So ist davon auszugehen, dass die fixen Kosten für
die Entwicklung und Bereitstellung der INDEX-Datenbanken im Vergleich zu den variablen Kosten hoch sind.
Sowohl der (originäre) Aufwand für die Erstellung der Datenbankstruktur, als auch der (wiederkehrende)
Aufwand für das Erfassen und die Pflege der Medikamenteninformationen sind von der effektiven Nutzerzahl
der Daten unabhängig. Aufgrund der Datenbereitstellung via Webservices dürften auch keine nennenswerte
variable Reproduktions- oder Vertriebskosten entstehen. HCI profitiert somit von einer stark ausgeprägten
Stückkostendegression, d.h. die Durchschnittskosten sinken mit jedem zusätzlichen Nutzer des
gleichen INDEX-Produkts. Nebst diesen Grössenvorteilen (Economies of Scale) dürfte HCI auch
von erheblichen Verbundsvorteilen (Economies of Scope) profitieren. Da die verschiedenen INDEX-Produkte
auf dieselbe Metadatenbank zurückgreifen, führt ein Nutzerzuwachs bei einem INDEX-Produkt immer
auch zu tieferen Durchschnittskosten bei allen anderen INDEX-Produkten. Im Ergebnis kann HCI den Markt
für veredelte, maschinenlesbare Daten betreffend Medikamenteninformationen wohl zu viel niedrigeren
Kosten mit benutzergruppenspezifischen Medikamenteninformationsdatenangeboten versorgen, als dies mehreren
parallelen Anbietern möglich wäre. Dies spricht für das Vorliegen eines natürlichen
Monopols.
9.2.2.35 Ob
ein natürliches Monopol angreifbar ist oder nicht, hängt entscheidend davon ab, in welchem
Ausmass es durch Marktzutritts- und Marktaustrittsschranken geschützt ist und wie rasch das etablierte
Unternehmen auf potenziell neue Marktzutritte reagieren könnte. Die Bestreitbarkeit eines natürlichen
Monopols lässt sich anhand der Theorie der bestreitbaren Märkte beurteilen. Diese besagt, dass
nicht nur ein tatsächlich vollzogener Marktzutritt Marktmacht verhindern kann, sondern dass unter
bestimmte Bedingungen die Drohung eines potentiellen Marktzutritts durch andere Unternehmen ausreichend
ist, um selbst einen Monopolisten dazu zu zwingen, sich so zu verhalten wie ein Unternehmen bei vollkommenem
Wettbewerb (William J. Baumol/John C. Panzar/Robert D. Willig,
Contestable Markets and the Theory of Industry Structure, 1982; Michael
Spence, Contestable Markets and the Theory of Industry Structure; Journal of Economic Literature,
21 [1983], S. 981-990; William J. Baumol/Robert
D. Willig, Contestability: Developments since the Book, Oxford Economic Papers, 38 [1986], S.
9-36). Die Theorie der bestreitbaren Märkte beruht jedoch auf einer Reihe von restriktiven Annahmen.
So müssen insbesondere alle Unternehmen, die etablierten und die neu eintretenden, Zugang zur gleichen
Technologie haben und es dürfen keine versunkenen Kosten auftreten. Neue Wettbewerber müssen
zudem jederzeit und ohne Zeitverzögerung in den Markt eintreten, jede technisch mögliche Menge
herstellen und den Markt, wann immer gewünscht, auch ohne Kosten sofort wieder verlassen können.
Schliesslich muss die Reaktionszeit der etablierten Unternehmen hinreichend lang sein, sodass ein Neueinsteiger
in den Markt eintreten und die von ihm vor dem Eintritt beobachteten Profite auch tatsächlich realisieren
kann. Nur soweit diese Bedingungen kumulativ erfüllt sind, vermag sich potenzielle Konkurrenz auch
disziplinierend auf den Markt auszuwirken (Ulrich Schwalbe/Daniel
Zimmer, Kartellrecht und Ökonomie: Moderne ökonomische Ansätze in der europäischen
und deutschen Zusammenschlusskontrolle, 2. Aufl., 2011, S. 190).
9.2.2.36 Mithin
muss also das Zeitintervall zwischen dem Bekanntwerden eines neuen Marktzutritts und der Möglichkeit,
die Güter oder Dienstleistungen des Neueinsteigers zu beziehen, kürzer sein, als die transaktionsbedingte
Zeitverzögerung für die Reaktion des im Markt bereits etablierten Unternehmens. Wäre,
dem nicht so, könnte ein etabliertes Unternehmen beispielsweise unmittelbar auf einen niedrigeren
Preis des Neueinsteigers regieren, worauf dieser gar nie einen positiven Gewinn realisieren und deshalb
- trotz beobachtbarer supranormaler Gewinne - von vornherein gar nicht in den Markt eintreten
würde (Ulrich Schwalbe/Daniel Zimmer, a.a.O., S. 191).
9.2.2.37 Vorliegend
ist nicht anzunehmen, dass ein konkurrierender Datenveredler eine alternative Medikamenteninformationsdatenbank
in kürzerer Zeit entwickeln und auf den Markt bringen kann, als HCI zur Durchführung einer
abwehrenden Wettbewerbsreaktion benötigen würde. Die Lancierung eines erfolgreichen Konkurrenzproduktes
liesse sich kaum "über Nacht" und unbeobachtet von HCI bewerkstelligen. Zumal auch die
Beschwerdeführerinnen einräumen, dass dies erst nach dem Aufbau einer spezifischen Fachredaktion,
bestehend aus Ärzten, Apothekern, Pharmaassistenten, etc. durch eine Konkurrentin möglich wäre.
Zudem ist davon auszugehen, dass HCI einen bevorstehenden Marktzutritt nicht nur frühzeitig erkennen
würde, sondern auch zeitnah zu einer entsprechenden Abwehrreaktion in der Lage wäre. Denn unter
den möglichen Abwehrreaktionen finden sich zahlreiche Verhaltensanpassungen, die sich zugunsten
von ihren Kunden auswirken würden. Neben einer allgemeinen Preissenkung wäre beispielsweise
auch eine Mengenausdehnung möglich, indem den Datenkunden zusätzlich Informationen zugänglich
gemacht würden, die bei HCI bereits vorhanden sind, aber bislang noch nicht Teil des abonnierten
INDEX-Produkts waren. Solche Verhaltensanpassungen liessen sich relativ rasch und widerstandslos umsetzen.
9.2.2.38 Weitergehend
wurde bereits unter E. 9.2.2.20
bis 9.2.2.28
dargelegt, dass im zu beurteilenden Markt eine Wechselkostenproblematik besteht und potentielle Wettbewerber
bei der Entwicklung und dem Aufbau einer Datenbank mit erheblichen Sunk Costs konfrontiert wären.
9.2.2.39 Somit
ist vorliegend kein angreifbares natürliches Monopol gegeben und auf dem relevanten Markt findet
keine Marktdisziplinierung im Sinne der Theorie der bestreitbaren Märkte statt. Es besteht kaum
Raum für das Entstehen von (wirksamen) "Wettbewerb im Markt". Das Entstehen von (wirksamen)
"Wettbewerb um den Markt" wäre theoretisch zwar möglich, ist im vorliegenden Fall
aus den vorerwähnten Gründen aber sehr unwahrscheinlich.
9.2.2.40 Die
Vorinstanz kam im Übrigen in der Vernehmlassung letztlich zum gleichen Schluss und hielt fest, dass
selbst wenn man der Argumentation der Beschwerdeführerinnen folgen würde und von einem "Wettbewerb
um den Markt" ausginge, eine marktbeherrschende Position vorliegen würde, da weder ein aktueller
Konkurrent ersichtlich sei, der in der Lage wäre, HCI den Markt streitig zu machen, noch irgendwelche
konkreten Anzeichen vorhanden seien, dass potenzielle Konkurrenz entstehen könnte, die einen disziplinierenden
Einfluss auf die Verhaltensweise von HCI haben könnte. Zutreffend erwog die Vorinstanz im Übrigen
bereits in der Verfügung, dass der Wettbewerb auf dem Markt für veredelte, maschinenlesbare
Daten betreffend Medikamenteninformationen, wenn, dann in Form von Innovationswettbewerb spielen müsste,
wie es im elektronischen Bereich üblicherweise der Fall ist.
9.2.2.41 Im
Ergebnis ist somit festzuhalten, dass die angesichts des aktuellen Wettbewerbs bestehende marktbeherrschende
Stellung der ehemaligen Galenica-Gruppe mittels HCI durch den potentiellen Wettbewerb im massgeblichen
Zeitraum nicht aufgehoben wurde.
9.3 Markt
für die Aufnahme und den Erhalt in elektronischen Datensätzen betreffend Medikamenteninformationen
9.3.1
Aktueller
Wettbewerb
im relevanten Zeitraum
9.3.1.1 Die
Vorinstanz erwog, die Leistungserbringerinnen und -erbringer, Vertriebsunternehmen und Kostenträger
würden im Zusammenhang mit den von ihnen verwendeten Programmen den Zugang zu den Medikamenteninformationen
in der von HCI zur Verfügung gestellten Form nachfragen. Gleichzeitig würde HCI die Schnittstelle
zu den Softwarehäusern kontrollieren. Den Zugang zu dieser Datenbank für die Zulassungsinhaberinnen
könne nur HCI gewährleisten. HCI habe deshalb für Zulassungsinhaberinnen, die den Leistungserbringerinnen
und -erbringern, Vertriebsunternehmen und Kostenträgern Zugriff auf ihre veredelten, maschinenlesbaren
Daten gewährleisten möchten, einen Marktanteil von 100%, womit die Marktbeherrschung gegeben
sei.
9.3.1.2 Die
Beschwerdeführerinnen bringen vor, Unternehmen wie ywesee würden HCI konkurrieren. Ihr Marktanteil
betrage nicht 100%.
9.3.1.3 Es
stellt sich die Frage, ob ywesee auf dem Markt für die Aufnahme und den Erhalt in elektronischen
Datensätzen betreffend Medikamenteninformationen überhaupt eine Konkurrentin von HCI darstellt.
Die Datenbank von ywesee enthält zwar die Daten von [...]
Arzneimittel und [...] von der Krankenkasse bezahlten Non-Pharma Artikeln. Die Zulassungsinhaberinnen
stehen jedoch betreffend die Aufnahme und den Erhalt in diese Datenbank in keinem Vertragsverhältnis
mit ywesee. Die Aufnahme und der Erhalt der Arzneimittelinformationen in die Datenbank von ywesee erfolgt
für die Zulassungsinhaberinnen kostenlos. Ihre Arzneimittelinformationen werden auch dann in die
Datenbank aufgenommen, wenn dies von den Zulassungsinhaberinnen gar nicht nachgefragt bzw. gewünscht
wird.
9.3.1.4 Stellt
man bei der Berechnung der Marktanteile auf den Umsatz ab, resultiert somit ein Marktanteil von 0% von
ywesee. Ein Abstellen auf die Anzahl der Kunden von ywesee ist nicht möglich, da nicht bekannt ist,
wie viele Zulassungsinhaberinnen die Aufnahme in diese Datenbank effektiv nachfragen. Die Datenbank von
ywesee wird "nur" von rund [...] Ärztinnen und
Ärzten benutzt, nicht jedoch von anderen Leistungserbringerinnen und -erbringern, Vertriebsunternehmen,
Kostenträgern und Softwarehäusern. Es muss folglich davon ausgegangen werden, dass die Aufnahme
und der Erhalt in der Datenbank von ywesee den Erwartungen der Mehrheit der Zulassungsinhaberinnen nicht
genügt.
9.3.1.5 Neben
dem Angebot von ywesee sind keine anderen aktuellen Konkurrenzangebote ersichtlich, was im Übrigen
von den Beschwerdeführerinnen auch nicht geltend gemacht wird. Damit ergibt sich, dass selbst wenn
ywesee als aktuelle Konkurrentin angesehen würde, auf dem Markt für die Aufnahme und den Erhalt
in elektronische Datensätze betreffend Medikamenteninformationen, wenn dann nur sehr eingeschränkter
aktueller Wettbewerb vorhanden ist.
9.3.2
Potentieller Wettbewerb
9.3.2.1 Potentieller
Wettbewerb ist gemäss den Erwägungen der Vorinstanz nicht vorhanden und zwar solange nicht,
als Galenica mittels HCI auf dem Markt für veredelte, maschinenlesbare Daten betreffend Medikamenteninformationen
eine marktbeherrschende Stellung habe und die Schnittstelle zu den Softwarehäusern nicht offengelegt
werde. Die Marktzutrittsschranken seien zu hoch.
9.3.2.2 Die
Beschwerdeführerinnen sind demgegenüber der Ansicht, potentieller Wettbewerb sei vorhanden
und ein Markteintritt möglich, was insbesondere das kostenlose Angebot MEDIupdate XML zeige. Daher
sei es wahrscheinlich, dass innert der nächsten zwei bis drei Jahre Marktzutritte in hinreichender
Grösse stattfinden würden. Auch auf diesem Markt würden sich die regulatorischen Veränderungen
positiv auf den potentiellen Wettbewerb auswirken und die Internationalisierung der Daten würde
einen Markteintritt ausländischer Anbieter fördern. Die Vorinstanz habe nicht begründet,
weshalb kein Konkurrenzangebot kurzfristig möglich sein solle.
9.3.2.3 Nach
Ansicht der Beschwerdeführerinnen soll das Angebot MEDIupdate XML von ywesee zeigen, dass Markteintritte
möglich sind. Von ywesee geht aber - sofern sie überhaupt eine Konkurrentin auf diesem
Markt darstellt - wie oben unter E. 9.3.1.3
dargelegt, keine hinreichende Konkurrenzwirkung aus. Die Möglichkeit eines Markteintritts von Konkurrenten
kann aber nur dann eine disziplinierende Wirkung auf ein Unternehmen ausüben, wenn von ihnen eine
hinreichende Konkurrenzwirkung ausgeht. Entsprechend kann aus dem Beispiel MEDIupdate XML von ywesee
gerade nicht geschlossen werden, dass Markteintritte mit hinreichender Konkurrenzwirkung in einem absehbaren
Zeitraum möglich sind.
9.3.2.4 Ebenfalls
nicht zu überzeugen vermag das Vorbringen, potentieller Wettbewerb bestehe aufgrund der Änderung
der gesetzlichen Rahmenbedingungen. Wie unter E. 9.2.2.16
dargelegt, lässt sich aus diesem Umstand gerade nicht ableiten, dass ein Markteintritt in einem
absehbaren Zeitraum wahrscheinlich ist. Dies wäre jedoch Voraussetzung für die Berücksichtigung
der Möglichkeit eines Markteintrittes.
9.3.2.5 Entgegen
dem Vorbringen der Beschwerdeführerinnen kann der Vorinstanz auch nicht vorgeworfen werden, sie
begründe nicht, weshalb ein Konkurrenzangebot kurzfristig nicht möglich sein sollte. So führte
die Vorinstanz mit Verweis auf ihre Erwägungen zum potentiellen Wettbewerb im Markt für veredelte,
maschinenlesbare Daten betreffend Medikamenteninformationen, wo sie verschiedene Hindernisse für
potenziellen Wettbewerb erwähnt, aus, dass die Marktzutrittsschranken zu hoch seien.
9.3.2.6 Weitere
Hinweise auf potentiellen Wettbewerb sind weder ersichtlich, noch werden solche geltend gemacht. Damit
ist nicht zu beanstanden, wenn die Vorinstanz zum Schluss gekommen ist, dass potentieller Wettbewerb
solange nicht vorhanden sei, als die Galenica mittels HCI auf dem Markt für veredelte, maschinenlesbare
Daten betreffend Medikamenteninformationen eine marktbeherrschende Stellung habe und die Schnittstelle
zu den Softwarehäusern nicht offengelegt werde, da die Marktzutrittsschranken zu hoch seien.
9.3.3
Stellung der Marktgegenseite
9.3.3.1 Der
Aspekt der Stellung der Marktgegenseite erfordert eine Abklärung, ob aufgrund spezifischer Faktoren
den Nachfragern des jeweiligen Produkts eine besondere Verhandlungsmacht zukommt, aufgrund der sie einen
ausreichenden Wettbewerbsdruck gegenüber dem untersuchten Unternehmen ausüben können,
so dass sich dieses nicht unabhängig verhalten kann (Urteile 2C_113/2017, Hallenstadion,
E. 5.5.2; B-3618/2013, Hallenstadion, E. 218).
9.3.3.2 Die
Vorinstanz stellte fest, HCI habe es sich trotz des Vollständigkeitserfordnisses erlauben können,
den Zulassungsinhaberinnen die Streichung aus den Datensätzen in Aussicht zu stellen. Zudem würden
die Beschwerdeführerinnen selbst den Standpunkt vertreten, dass ohne ihre Produkte ein sicherer
und effizienter Vertrieb nicht möglich sei. Darin sähen die Beschwerdeführerinnen den
grossen Nutzen einer Präsenz in den INDEX-Daten für die Zulassungsinhaberinnen. Aus der Stellung
der Marktgegenseite könne somit nicht geschlossen werden, dass sich HCI nicht unabhängig verhalten
könne.
9.3.3.3 Demgegenüber
vertreten die Beschwerdeführerinnen die Auffassung, dass die Zulassungsinhaberinnen über eine
sehr starke Stellung verfügten, was bereits aus der Grösse und den erzielten Umsätzen
dieser Unternehmen zu schliessen sei. Im Vergleich zu den multinationalen Pharmakonzernen sei HCI, die
im Geschäftsbereich Medikamenteninformationen einen jährlichen Umsatz von ca. [...] erziele,
ein kleines Unternehmen. Die Annahme, HCI könne die Zulassungsinhaberinnen unter Druck setzen, sei
nicht plausibel. Zwanzig Zulassungsinhaberinnen hätten an ouwerkerk eine Anschubfinanzierung von
je ca. Fr. [...] für das Produkt Just-Medical geleistet. Diese Unternehmen würden problemlos
die nötigen Mittel bereitstellen können, um ernsthaft in den Markt einzutreten.
9.3.3.4 Weiter
bringen die Beschwerdeführerinnen vor, die Marktgegenseite verfüge überdies über
eine beachtliche Marktstärke, [...]. HCI könne ihre Geschäftstätigkeit nur fortführen,
wenn ihre Datenbanken einigermassen vollständig, von guter Qualität und aktuell, ihre Daten
maschinenlesbar und ihre Produkte stets innovativ seien. Diese [...] steige mit der Grösse der
entsprechenden Zulassungsinhaberinnen. Organisationsgrad, Sachkunde und Professionalität der oftmals
multinationalen Pharmaunternehmen seien ebenfalls erheblich. Einige Zulassungsinhaberinnen hätten
zwischenzeitlich keine Verträge mit HCI abgeschlossen, womit HCI die Informationen auf eigene Kosten
habe einpflegen müssen. Auch deshalb sei HCI nicht in der Lage sich von den anderen Marktteilnehmern
unabhängig zu verhalten. Daran ändere auch der Nutzen, den die Zulassungsinhaberinnen durch
die Aufnahme in die INDEX-Datenbanken erhielten, nichts.
9.3.3.5 Für
die Beurteilung der Stellung der Marktgegenseite können alle Aspekte, aus denen sich eine besondere
Verhandlungsposition der Nachfrager mit ausreichendem Wettbewerbsdruck ergibt, herangezogen werden (Urteil
B-3618/2013, Hallenstadion, E. 219). Entsprechende Faktoren bilden
dabei insbesondere (i) die wirtschaftliche Stärke der Nachfrager, (ii) die Bedeutung der Nachfrager
für das untersuchte Unternehmen, (iii) die Anzahl der Nachfrager, (iv) der Organisationsgrad der
Nachfrager, sowie (v) die Sachkunde und Professionalität der Nachfrager (Urteil
B-3618/2013,
Hallenstadion, E. 219; Reinert/Wälchli,
BSK-KG, Art. 4 Abs. 2 N 306 ff.; Stäuble/Schraner,
DIKE-KG, Art. 4 Abs. 2 N 246). Mass-gebend für die Beurteilung
der Stellung der Marktgegenseite ist eine Wertung aller relevanten Aspekte im Rahmen einer Gesamtanalyse,
ohne dass einem der Aspekte ein absoluter Vorrang aufgrund von allgemeinen Umständen zukommt (Urteil
B-3618/2013, Hallenstadion, E. 220; Stäuble/Schraner,
DIKE-KG, Art. 4 Abs. 2 N 247).
9.3.3.6 Damit
die Marktgegenseite eine disziplinierende Wirkung auf das marktbeherrschende Unternehmen zu Gunsten aller
Marktteilnehmer des relevanten Marktes ausüben kann, müsste die Marktgegenseite allerdings
einen derartigen Wettbewerbsdruck aufbauen können, dass sowohl die Wettbewerber des potentiell marktbeherrschenden
Unternehmens als auch die übrigen Unternehmen der Marktgegenseite von dessen fehlender Möglichkeit
zu einem unabhängigen Verhalten profitieren würden. Nicht ausreichend für eine Beeinflussung
im Rahmen einer Beurteilung der marktbeherrschenden Stellung ist hingegen, dass lediglich einzelne Unternehmen
der Marktgegenseite über solch eine wirtschaftliche Stärke verfügen, die sie jeweils in
die Lage versetzen, ihre Verhandlungsposition gegenüber dem marktbeherrschenden Unternehmen durchzusetzen
(Urteil B-831/2011, SIX, E. 488).
9.3.3.7 Einige
Zulassungsinhaberinnen verfügen aufgrund ihrer Grösse und ihrer Umsätze über wirtschaftliche
Stärke. Auch kann diesen Zulassungsinhaberinnen Sachkunde und Professionalität nicht abgesprochen
werden. Aber HCI stehen mit insgesamt rund 300 Zulassungsinhaberinnen eine grosse Anzahl Nachfragerinnen
gegenüber. Darunter befinden sich auch zahlreiche kleinere und mittlere Unternehmen mit beschränkter
wirtschaftlicher Stärke. Dazu kommt, dass die ehemalige Galenica-Gruppe, zu welcher HCI gehörte,
aufgrund ihrer Grösse und ihren Umsätzen ebenfalls über wirtschaftliche Stärke verfügte.
9.3.3.8 Weiter
kann aus dem geltend gemachten Umstand, zwanzig Zulassungsinhaberinnen hätten an ouwerkerk eine
Anschubfinanzierung von je ca. Fr. [...] für das Produkt Just-Medical geleistet, nicht auf einen
hohen Organisationsgrad der Marktgegenseite geschlossen werden. Denn einerseits handelt es sich bei zwanzig
Zulassungsinhaberinnen nur um einen kleinen Teil der Nachfragerinnen. Andererseits kann aufgrund des
fehlenden Erfolges dieses Projektes nicht gesagt werden, sie hätten sich in der Vergangenheit bereits
"erfolgreich" zusammengeschlossen.
9.3.3.9 Weitere
Aspekte, die für einen hohen Organisationsgrad sprechen würden, werden nicht vorgebracht.
9.3.3.10 Die
Feststellung der Vorinstanz, HCI habe es sich trotz des Vollständigkeitserfordnisses erlauben können,
den Zulassungsinhaberinnen die Streichung aus den Datensätzen in Aussicht zu stellen, ist nicht
zu beanstanden. Denn auch aus dem geltend gemachten Umstand, dass einige Zulassungsinhaberinnen zwischenzeitlich
keine Verträge mit HCI abgeschlossen hätten, lässt sich nicht auf einen beachtenswerten
Wettbewerbsdruck der Marktgegenseite schliessen. Denn zum einen wird nur geltend gemacht, dass die Zulassungsinhaberinnen
"zwischenzeitlich" keine Verträge abgeschlossen haben. Daraus ist zu schliessen, dass
sie davon wieder abgerückt sind. Zum anderen hat dieser Wettbewerbsdruck nicht dazu geführt,
dass alle Zulassungsinhaberinnen ihre Position gegenüber HCI haben durchsetzen können bzw.
von einer fehlenden Möglichkeit von HCI zu einem unabhängigen Verhalten haben profitieren können.
9.3.3.11 Die
Zulassungsinhaberinnen übten im massgeblichen Zeitraum auf HCI keinen beachtenswerten Wettbewerbsdruck
aus, der die Möglichkeit zum unabhängigen Verhalten gegenüber allen Unternehmen der Marktgegenseite
ausgeschlossen hätte.
9.4 Zweiseitiger
Markt
9.4.1 Die
Vorinstanz prüfte sodann, ob die beiden definierten Märkte als jeweils "normale"
Märkte zu definieren sind oder ob ein sogenannter zweiseitiger Markt vorliegt.
9.4.2 Eine
zentrale Eigenschaft zweiseitiger Märkte ist, dass der Nutzen einer Gruppe von Kunden, die eine
bestimmte Plattform nutzen, von der Grösse der anderen Gruppe von Kunden auf dieser Plattform abhängt
"indirekte Netzwerkeffekte"). Um festzustellen, ob ein zweiseitiger Markt vorliegt, können
folgende Bedingungen geprüft werden: (i) die Plattform bietet zwei Arten von Gütern oder Dienstleistungen
an; (ii) es liegen zwei unterschiedliche Nachfragergruppen vor, die unterschiedliche Güter oder
Dienstleistungen erwerben; (iii) es liegen indirekte Netzwerkeffekte bei mindestens einer Gruppe vor,
welche die Nachfragen der beiden Gruppen miteinander verbinden; (iv) der Markt ist so aufgebaut, dass
keine direkten Verhandlungen zwischen den beiden Nachfragergruppen stattfinden können (kein «pass-through»)
(Marc Blatter, Digitalisierung - Herausforderungen
für die Wettbewerbspolitik, sic! 2016 S. 378 ff., 379 m.H. auf P. Belelfamme/M.
Peitz, Industrial Organization, Cambridge 2010, 628 und L.
Filistrucchi/D. Gerardin/E. van Damme, Identifying two-sided markets: A progress report, World
Competition 2013, 33-59).
9.4.3 Die
Vorinstanz erwog, dass spezifische Charakteristika vorlägen, die grundsätzlich für eine
Betrachtung als zweiseitigen Markt sprächen. Der zweiseitige Charakter sei aber für die weiteren
Analysen von untergeordneter Bedeutung, da es vorliegend an einer Internalisierung der indirekten Netzwerkeffekte
fehle. Zudem sei der Umstand, dass beide Marktgegenseiten die Produkte und Dienstleistungen von HCI nutzten,
nicht kausal auf die Gestaltung der Preisstruktur zurückzuführen, was für zweiseitige
Märkte typisch wäre. Weiter würden sich die Produkte und Dienstleistungen, die HCI gegenüber
den beiden Marktgegenseiten erbringe, in sachlicher Hinsicht grundlegend unterscheiden. Ebenso fehle
es an einer messbaren, durch HCI vermittelten Transaktion zwischen den beiden Marktgegenseiten.
9.4.4 Die
Beschwerdeführerinnen bringen keine Einwände gegen diese Erwägungen und Beurteilung vor.
Das Bundesverwaltungsgericht kann sich den zutreffenden Erwägungen der Vorinstanz anschliessen.
Es liegen zwar zahlreiche Charakteristika vor, die für einen zweiseitigen Markt sprechen. Da die
Verhältnisse auf der anderen Marktseite aber konstant blieben, ist der zweiseitige Charakter von
untergeordneter Bedeutung und die Analyse kann sich auf eine Marktseite beschränken.
9.4.5 Soweit
die Vorinstanz im Rahmen der Analyse der Preisstruktur erwog, es läge prima Vista keine Veränderung
der Preisstruktur vor, sondern eine Erhöhung des aggregierten Preisniveaus, ist lediglich ergänzend
festzuhalten, dass jedoch betreffend Umfang des Angebotes eine Erhöhung stattfand.
10. Isolierte
Feststellung der marktbeherrschenden Stellung
10.1 Die
Vorinstanz hat im Dispositiv (Ziff. 1) festgestellt, dass Galenica mittels ihrer Tochtergesellschaft
HCI seit dem 1. Januar 2013 auf den beiden abgegrenzten Märkten über eine marktbeherrschende
Stellung gemäss Art. 4 Abs. 2 KG verfüge.
10.2 Sie
erwog hierzu, das Bundesverwaltungsgericht habe im Urteil
B-7633/2009 vom 14. September
2015 in Sachen ADSL II zwar die isolierte Feststellung der Marktbeherrschung
abgelehnt. Dabei habe es sich hauptsächlich auf BGE 137 II 199, Terminierung
Mobilfunk, E. 6.5 f. gestützt, wobei das Bundesgericht aber keine derart strikte Haltung
vertreten habe wie das Bundesverwaltungsgericht im Urteil B-7633/2009. Nach der bundesgerichtlichen Rechtsprechung
könnten reine Feststellungen nicht auf Art. 30 KG gestützt werden und zur Anwendung von Art.
25 VwVG sei es erforderlich, dass einerseits ein schutzwürdiges (öffentliches) Feststellungsinteresse
vorliege und andererseits dieses Interesse nicht ebenso gut mit einer rechtsgestaltenden Verfügung
gewährt werden könne. Im konkreten Fall von BGE 137 II 199 sei das strittige Sanktionsverfahren
ausdrücklich auf einen festen in der Vergangenheit liegenden Zeitraum begrenzt gewesen, die Marktverhältnisse
hätten sich verändert und für die kartellrechtliche Überprüfung der späteren
Sachverhalte hätten neue Untersuchungen mit Ermittlung der Marktstellung durchgeführt werden
müssen. Das Bundesgericht habe aber mit Verweis auf den Entscheid der Rekurskommission für
Wettbewerbsfragen (REKO/WEF) vom 9. Juni 2005 in Sachen Telekurs Multiplay,
E. 6.2.6 (veröffentlicht in: RPW 2005/3 S. 530 ff., 555 f.) explizit festgehalten, dass im zu beurteilenden
Entscheid keine Meldepflicht nach Art. 9 Abs. 4 KG in Frage gestanden habe. Im verwiesenen Entscheid
habe die REKO/WEF erwogen, unter dem Gesichtspunkt eines legitimen Feststellungsinteresses erscheine
ein die kartellrechtliche Rechtslage lediglich feststellendes Dispositiv zulässig, wenn die Vorinstanz
eine Untersuchung einzustellen beabsichtige, weil sich ein marktbeherrschendes Unternehmen zwar zulässig
verhalten habe, aber der fusionsrechtlichen Meldepflicht nach Art. 9 Abs. 4 KG unterstellt werden solle.
10.3 Nach
Ansicht der Vorinstanz ist es unerheblich, ob sich das marktbeherrschende Unternehmen, welches der Meldepflicht
nach Art. 9 Abs. 4 KG unterstellt werden soll, im Sinne von Art. 7 KG unzulässig verhalten hat oder
nicht. Die separate Feststellung könne auch gerade im Hinblick auf Beschwerdeverfahren notwendig
sein. Denn das Bundesverwaltungsgericht könne anders als die WEKO eine missbräuchliche Verhaltensweise
verneinen, aber die Marktbeherrschung stützen, welche andauere und deshalb für künftige
Zusammenschlusskontrollverfahren in Zusammenhang mit Art. 9 Abs. 4 KG relevant sei. Da das Bundesverwaltungsgericht
in der Regel die Verfügung lediglich aufhebe, würde dies dazu führen, dass die WEKO ihre
Prüfungsbefugnisse in der Zusammenschlusskontrolle in diesen Fällen nicht ausüben könne.
Mit Blick auf den Sinn und Zweck von Art. 9 Abs. 4 KG bestehe vorliegend ein schutzwürdiges öffentliches
Interesse an der Feststellung der marktbeherrschenden Stellung der Galenica auf den beiden abgegrenzten
Märkten. Es bestehe die Gefahr, dass Galenica (potentielle) Wettbewerber übernehmen könne,
welche einen Umsatz unter 100 Mio. Fr. aufweisen würden, um damit ihre Marktstellung zu zementieren,
zumal Galenica auch in benachbarten Märkten stark positioniert sei.
10.4 Die
Beschwerdeführerinnen machen einerseits geltend, sie würden nicht mehr demselben Konzern angehören.
Die Beschwerdeführerin 1 sei die Muttergesellschaft der Vifor Pharma Gruppe und die Beschwerdeführerin
2 gehöre zur heutigen neuen Galenica-Gruppe (zunächst Galenica Santé-Gruppe). Bereits
im Zeitpunkt der Eröffnung der Verfügung sei HCI keine Tochtergesellschaft der Beschwerdeführerin
1 mehr gewesen, womit Ziffer 1 der angefochtenen Verfügung aufzuheben sei.
10.5 Andererseits
machen die Beschwerdeführerinnen geltend, es sei nach der neueren bundesgerichtlichen Rechtsprechung
(BGE 137 II 199, Terminierung Mobilfunk,
E. 6) und dem Urteil des Bundesverwaltungsgericht B-7633/2009 vom 14. September 2015 in Sachen ADSL
II im Rahmen einer Sanktionsverfügung nach Art. 49a KG weder erforderlich noch zulässig,
im Dispositiv die Feststellung einer marktbeherrschenden Stellung gesondert vorzunehmen. Dabei verweisen
die Beschwerdeführerinnen im Wesentlichen auf E. 385 des Urteils des Bundesverwaltungsgericht
B-7633/2009
vom 14. September 2015 in Sachen ADSL II. Das Bundesverwaltungsgericht
habe in diesem Entscheid das Vorbringen des öffentlichen Interesses aufgrund von Art. 9 Abs. 4 KG
berücksichtigt und sei zum Schluss gekommen, dass die Feststellung der Marktbeherrschung keine verbindliche
Wirkung für einen späteren Zeitraum aufweisen könne. Die Fälle seien gleich gelagert.
An dieser Rechtsprechung sei festzuhalten.
10.6 Die
Vorinstanz hält in ihrer Vernehmlassung fest, HCI sei im Zeitpunkt der Eröffnung der Verfügung
nach wie vor eine Tochtergesellschaft der Beschwerdeführerin 1 gewesen. In der Duplik führt
sie zudem aus, die Feststellung der Marktbeherrschung entfalte auf einem Markt grundsätzlich Wirkung
für die ganze Unternehmensgruppe. Meldepflichtig seien somit unverändert die Galenica AG und
die Beschwerdeführerin 2.
10.7
Wie von der Vorinstanz und den Beschwerdeführerinnen dargelegt, hat sich das Bundesgericht
in BGE 137 II 199 in Sachen Terminierung Mobilfunk und das Bundesverwaltungsgericht
im Urteil B-7633/2009 in Sachen ADSL II mit der Frage der Zulässigkeit
einer isolierten Feststellung der marktbeherrschenden Stellung im Dispositiv auseinandergesetzt. In beiden
Entscheiden wurde festgehalten, das Entscheiderkenntnis habe sich auf die Rechtsfolge zu beschränken.
Im Dispositiv seien keine Ausführungen im Hinblick auf das Vorliegen einzelner Tatbestandsmerkmale
vorzunehmen, denn diese würden ausschliesslich Bestandteil der Begründung des Entscheides bilden.
Entsprechend ist im Erkenntnis grundsätzlich weder festzuhalten, ob eine marktbeherrschende Stellung
vorliegt, noch ob eine solche allenfalls missbraucht wurde (BGE 137 II 199, Terminierung
Mobilfunk, E. 6.2; Urteil B-7633/2009, ADSL
II, E. 382). Reine Feststellungen können
nicht auf Art. 30 KG gestützt werden (BGE 137 II 199, Terminierung
Mobilfunk, E. 6.3; Urteil B-7633/2009, ADSL
II, E. 383).
10.8 Gemäss
Art. 39 KG finden die Bestimmungen des Verwaltungsverfahrensgesetzes Anwendung, soweit das Kartellgesetz
nicht hiervon abweicht. Nach Art. 25 VwVG kann eine in der Sache zuständige Behörde von Amtes
wegen oder auf Gesuch hin eine Feststellungverfügung erlassen. Die Anwendbarkeit von Art. 25 VwVG
setzt bei beiden Varianten voraus, dass ein entsprechendes schutzwürdiges Feststellungsinteresse
vorliegt, welches nicht abstrakte, theoretische Rechtsfragen, sondern konkrete Rechte oder Pflichten
zum Gegenstand hat. Überdies muss ausgeschlossen sein, dass das schutzwürdige Interesse ebenso
gut mit einer rechtsgestaltenden Verfügung gewahrt werden kann (BGE 137 II 199, Terminierung
Mobilfunk, E. 6.4 ff. und Urteil B-7633/2009, ADSL
II, E. 384; beide
m.H. auf BGE 126 II 300 E. 2c; Rhinow/Koller/Kiss/Thurnherr/Brühl-Moser,
a.a.O., Rz. 1279 ff.; Häner,
Praxiskommentar VwVG, Art. 25 N 14 und 20).
10.9 In
BGE 137 II 199 kam das Bundesgericht zum Schluss, dass im konkret zu beurteilenden Fall kein schutzwürdiges
öffentliches Feststellungsinteresse ersichtlich sei. Denn das strittige Sanktionsverfahren sei ausdrücklich
beschränkt auf den Zeitraum von 1. April 2004 bis 31. Mai 2005. Schon deshalb könne eine allfällige
Feststellung der Marktbeherrschung keine verbindliche Vorwirkung für den späteren Zeitraum
zeitigen, für den die Untersuchung unter veränderten tatsächlichen Verhältnissen
weiterlaufe. Vielmehr sei die Marktbeherrschung ohnehin neu abzuklären. Hinzukomme, dass auch eine
andere Rechtswirkung kartellrechtlicher Natur nicht ersichtlich sei. Es stehe keine Meldepflicht nach
Art. 9 Abs. 4 KG in Frage. Ohnehin würde sich die Marktbeherrschung für den hier fraglichen
Zeitraum nicht ohne weiteres auf spätere Unternehmenszusammenschlüsse auswirken. Entsprechend
könne auch offengelassen werden, wieweit insofern überhaupt ein selbständiger Feststellungsentscheid
zulässig wäre (BGE 137 II 199, Terminierung Mobilfunk,
E. 6.5.1 f.).
10.10 Diese
Rechtsprechung hat das Bundesgericht im Urteil 2C_484/2010 vom 29. Juni 2012 in Sachen Publigroupe
bestätigt (Urteil 2C_484/2010, Publigroupe, E. 14 [nicht
publizierte Erwägung in BGE 139 I 72]).
10.11 Das
Bundesverwaltungsgericht hat unter Hinweis auf BGE 137 II 199 im Urteil B-7633/2009 vom 14. September
2015 in Sachen ADSL II erwogen, die Feststellung der Marktbeherrschung
könne für eine bestimmte Periode grundsätzlich keine verbindliche Wirkung für einen
späteren Zeitraum aufweisen. Entsprechend sei es ausgeschlossen, für spätere Zeiträume
ohne weitere Prüfung der Umstände eine Marktbeherrschung anzunehmen. Vielmehr müsse das
Tatbestandsmerkmal der Marktbeherrschung für jedes Verfahren neu abgeklärt werden; auch wenn
dabei unter Berücksichtigung der prozessualen Rechte der Verfahrensbeteiligten auf bereits vorgenommene
Untersuchungshandlungen oder Beweismassnahmen zurückgegriffen werden könne. Aus denselben Gründen
bedürfe es auch im Hinblick auf Art. 9 Abs. 4 KG nicht einer vorgängigen Feststellung einer
Marktbeherrschung.
10.12 Derweil
hat das Bundesgericht in einem neueren Entscheid zu Wettbewerbsabreden nach Art. 5 KG die Möglichkeit
zur Feststellung der Wettbewerbswidrigkeit eines bestimmten wirtschaftlichen Verhaltens im Dispositiv
anerkannt (Urteil des BGer 2C_101/2016 vom 18. Mai 2018, Altimum,
E. 17 [nicht publizierte Erwägung in BGE 144 II 246]).
10.13 Das
Bundesverwaltungsgericht stellte im Urteil B-831/2011 vom 18. Dezember 2018 in Sachen SIX
daraufhin fest, die Möglichkeit einer Feststellung des wettbewerbswidrigen Verhaltens sei auch bei
der Beurteilung einer Sanktionsverfügung in Bezug auf Art. 7 KG sachgerecht (Urteil B-831/2011,
SIX, E. 419). Weiter erwog das Bundesverwaltungsgericht aber auch,
es bedürfe selbst bei Anerkennung der Feststellung eines marktmissbräuchlichen Verhaltens im
Dispositiv unter Berücksichtigung von Art. 9 Abs. 4 KG im Regelfall keiner zusätzlichen Feststellung
der marktbeherrschenden Stellung des betreffenden Unternehmens. Denn durch die Feststellung eines marktmissbräuchlichen
Verhaltens gemäss Art. 7 KG werde implizit das Vorliegen einer marktbeherrschenden Stellung bejaht.
Zudem werde dadurch die Anwendung von Art. 9 Abs. 4 KG nicht verhindert, weil mit der Feststellung
eines wettbewerbswidrigen Verhaltens keine Aussage darüber verbunden sei, dass die marktbeherrschende
Stellung nach dem der Feststellung jeweils zu Grunde liegenden relevanten Zeitraum nicht mehr vorliege
(Urteil B-831/2011, SIX, E. 420). Die Dispositiv-Ziffer mit der
isolierten Feststellung der marktbeherrschenden Stellung wurde aufgehoben (Urteil B-831/2011, SIX,
Ziff. 2 des Dispositiv und E. 421).
10.14 An
dieser noch jungen Rechtsprechung ist festzuhalten, zumal die von der Vorinstanz dagegen vorgebrachten
Argumente nicht zu überzeugen vermögen. Denn zum einen lässt sich aus dem Hinweis des
Bundesgerichts in BGE 137 II 199, Terminierung Mobilfunk, E. 6.5.2
auf den Entscheid der REKO/WEF vom 9. Juni 2005 in Sachen Telekurs Multiplay,
E. 6.2.6 (veröffentlicht in: RPW 2005/3 S. 530 ff., 555 f.) nicht ableiten, das Bundesgericht
habe damit die Zulässigkeit der isolierten Feststellung der marktbeherrschenden Stellung bejaht.
Vielmehr hat das Bundesgericht im Urteil 2C_484/2010 vom 29. Juni 2012 in Sachen Publigroupe
seine Rechtsprechung explizit bestätigt.
10.15 Zum
anderen lässt sich auch nicht mit Blick auf den Sinn und Zweck von Art. 9 Abs. 4 KG das Vorliegen
eines schutzwürdigen öffentlichen Interesses ableiten. Denn Art. 9 Abs. 4 KG strebt nicht die
Wirkungen an, wie sie eine Feststellungsverfügung äussert. Die Bestimmung zielt auf eine Erweiterung
der Meldepflicht für besonders starke Unternehmen und will sich dabei an einem für die Unternehmen
leichter und klarer feststellbaren Kriterium orientieren, als es deren Marktanteile wären. Es ist
aber nicht Ziel der Norm, verfahrensrechtliche Fragen wie die präjudizielle Verbindlichkeit von
Feststellungen zu regeln. Im Gegensatz dazu zielen die typischen eine Feststellungsverfügung anordnenden
Normen wie beispielsweise Art. 10 des Bundesgesetzes über den Wald vom 4. Oktober 1991 (Waldgesetz,
WaG, SR 921.0) oder Art. 18 Messmittelverordnung vom 15. Februar 2006 (MessMV, SR 941.210) genau darauf
ab, eine Vorfrage zur Hauptfrage eines gesonderten Entscheids zu machen und die Frage für künftige,
andere Verfahren verbindlich zu regeln. Art. 9 Abs. 4 KG bezweckt eine solche verbindliche Feststellung
der Marktbeherrschung nicht (Samuel Indermühle, Die
umsatzunabhängige Meldepflicht von Unternehmenszusammenschlüssen im Schweizer Kartellgesetz,
2013, Rz. 13.19).
10.16 Der
Vollständigkeit halber ist zudem festzuhalten, dass der Verzicht auf die isolierte Feststellung
der marktbeherrschenden Stellung auch nicht zur Folge haben muss, dass die WEKO ihre Prüfungsbefugnis
nach Art. 9 Abs. 4 KG nicht mehr ausüben kann. Denn zwar weist der Wortlaut des deutschen Gesetzestextes
von Art. 9 Abs. 4 KG darauf hin, dass für das Auslösen der umsatzunabhängigen Meldepflicht
eine rechtskräftige Feststellungsverfügung über das Vorliegen einer marktbeherrschenden
Stellung notwendig ist. So besteht nach dem deutschsprachigen Wortlaut die Meldepflicht, wenn am Zusammenschlussvorhaben
ein Unternehmen beteiligt ist, "für welches in einem Verfahren nach diesem Gesetz rechtskräftig
festgestellt worden ist, dass es in der Schweiz auf einem bestimmten Markt eine beherrschende Stellung
hat". Demgegenüber deuten die französisch- und italienischsprachigen Fassungen von Art.
9 Abs. 4 KG daraufhin, dass die Marktbeherrschung im Rahmen der Erwägungen einer Verfügung,
die in Bestandskraft erwachsen ist, festgestellt worden sein müsse. Denn der französische Text
postuliert die erweiterte Meldepflicht, wenn "une décision passé en force établit
qu'une entreprise participante occupe en Suisse une position dominante sur un marché"
und der italienische Text, wenn "se risulta da una procedura fondata sulla presente legge e passata
in giudicato che un'impresa participante alla concentrazione occupa in Svizzera una posizione dominante
sul mercato". Im Gegensatz zu den in Art. 9 Abs. 4 KG verwendeten Ausdrücke "établir"
und "risultare" werden für den Ausdruck "feststellen" im Sinne einer Feststellungsverfügung
in Art. 25 VwVG die Ausrücke "constater" und "accertare" vewendet (Indermühle,
a.a.O, Rz. 14.7 ff.).
10.17 Ziffer
1 des Dispositivs der angefochtenen Verfügung ist somit aufzuheben.
11. Unzulässige
Verhaltensweisen
11.1 Eine
unzulässige Verhaltensweise gemäss Art. 7 Abs. 1 KG liegt vor, wenn ein marktbeherrschendes
Unternehmen durch den Missbrauch seiner Stellung auf dem relevanten Markt andere Unternehmen in der Aufnahme
oder Ausübung des Wettbewerbs behindert oder die Marktgegenseite benachteiligt. Das Kartellrecht
verbietet eine marktbeherrschende Stellung nicht, und eine solche ist für sich allein auch nicht
missbräuchlich, besteht doch der Sinn des Wettbewerbs gerade darin, durch Markterfolg und internes
Wachstum eine dominierende Stellung zu erreichen. Marktbeherrschung wird allerdings dann problematisch,
wenn - wie Art. 7 Abs. 1 KG festhält - als qualifizierendes Element eine unzulässige
Verhaltensweise hinzutritt. Solche Verhaltensweisen setzen einen Missbrauch voraus: Missbraucht wird
danach die marktbeherrschende Stellung, welche es einem Unternehmen erlaubt, sich unabhängig von
anderen Marktteilnehmern zu verhalten. Das missbräuchliche Verhalten richtet sich entweder gegen
andere Unternehmen oder gegen die Marktgegenseite (d.h. Lieferanten oder Abnehmer des behindernden Unternehmens;
BGE 139 I 72, Publigroupe, E. 10.1.1; Urteile des BGer 2C_113/2017,
Hallenstadion, E. 6.1; 2C_985/2015 vom 9. Dezember 2019,
ADSL II, E. 4.1;).
11.2 Ein
missbräuchliches Verhalten gemäss Art. 7 KG umfasst alle denkbaren Verhaltensweisen von marktbeherrschenden
Unternehmen, welche volkswirtschaftlich schädliche Effekte aufweisen oder die wirtschaftliche Freiheit
von anderen Unternehmen behindern. Solche Verhaltensweisen richten sich überwiegend als sog. Behinderungsmissbrauch
gegen andere Wettbewerber oder als sog. Ausbeutungsmissbrauch gegen die jeweilige Marktgegenseite, d.h.
Abnehmer bzw. Lieferanten des marktbeherrschenden Unternehmens (BGE 139 I 72, Publigroupe,
E. 10.1.1 f.; Urteile 2C_985/2015, ADSL II, E. 4.1; B-831/2011,
SIX, E. 510; B-7633/2009,
ADSL II, E. 388).
Charakteristisch für den sog. Ausbeutungsmissbrauch ist das Streben des marktbeherrschenden Unternehmens
nach ökonomischen Vorteilen durch eine Beeinträchtigung der Interessen von Handelspartnern
und Verbrauchern unter Ausnutzung seiner marktbeherrschenden Stellung. Behinderungsmissbrauch umfasst
dagegen sämtliche Massnahmen beherrschender Unternehmen ausserhalb eines fairen Leistungswettbewerbs,
die sich unmittelbar gegen aktuelle und potentielle Wettbewerber (Konkurrenten und Handelspartner) richten
und diese in ihren Handlungsmöglichkeiten auf dem beherrschten oder den benachbarten Märkten
einschränken (BGE 139 I 72, Publigroupe, E. 10.1.1; Urteile
2C_113/2017, Hallenstadion, E. 6.1; 2C_985/2015, ADSL
II, E. 4.1).
11.3
Der Schutz des Wettbewerbs gemäss Art. 7 KG ist somit nicht nur darauf ausgerichtet, Endverbraucher
vor einem unmittelbaren Schaden durch ein missbräuchliches Verhalten zu bewahren, sondern er umfasst
angesichts der dominanten Stellung des marktbeherrschenden Unternehmens auch allgemein die Sicherstellung
von sachgerechten Wettbewerbsbedingungen zur Aufrechterhaltung oder Ausbildung eines ausreichenden Wettbewerbs
auf allen durch das jeweilige Verhalten beeinflussten Märkten (Urteile B-831/2011,
SIX, E. 510; B-7633/2009,
ADSL II, E. 388).
11.4 Einem
marktbeherrschenden Unternehmen kommt deshalb eine besondere Verantwortung zu, durch sein Verhalten am
Markt einen wirksamen und unverfälschten Wettbewerb nicht zu beeinträchtigen. Daher hat es
auf die Anwendung von Praktiken zu verzichten, die nicht den Mitteln eines Leistungswettbewerbs entsprechen,
und die zu einer Verdrängung anderer Wettbewerber führen können (Botschaft zu einem Bundesgesetz
über Kartelle und andere Wettbewerbsbeschränkungen [Kartellgesetz, KG] vom 23. November 1994
[BBl 1995 I 468, 569]; BGE 139 I 72, Publigroupe,
E. 10.1.1; Urteile B-831/2011, SIX, E. 510 und 1119; B-7633/2009,
ADSL II, E. 388; Amstutz/Carron,
BSK-KG, Art. 7 N 72 f.; Urteil des EuGH vom 6. September 2017 C-413/14 P Intel
Corporation Inc./Kommission, EU:C:2017:632 Rn. 135). Daraus folgt zum einen, dass Unternehmen
in beherrschender Stellung unter besonderen Umständen das Recht zu bestimmten Verhaltensweisen oder
Massnahmen abzusprechen ist, die für sich genommen nicht missbräuchlich sind und die sogar
nicht zu beanstanden wären, wenn sie von nicht beherrschenden Unternehmen an den Tag gelegt oder
vorgenommen würden (Urteile B-831/2011, SIX, E. 510 und 1120;
B-7633/2009, ADSL II, E. 388; Amstutz/Carron,
BSK-KG, Art. 7 N 72 f.; Clerc/Këllezi, CR-Concurrence,
Art. 7 I N 65). Zum anderen folgt daraus, dass einem marktbeherrschenden Unternehmen die Verpflichtung
zukommt, alle praktizierenden Verhaltensweisen auf ihre Vereinbarkeit mit Art. 7 KG zu überprüfen
(Urteil B-831/2011, SIX, E. 1121; Amstutz/Carron,
BSK-KG, Art. 7 N 73).
11.5 Verdeutlicht
werden die Behinderung und Benachteiligung nach Art. 7 Abs. 1 KG durch die nicht abschliessende Liste
von Verhaltensweisen in Art. 7 Abs. 2 KG. Ob die darin aufgeführten Verhaltensweisen missbräuchlich
sind, ist allerdings immer an den Anforderungen von Art. 7 Abs. 1 KG zu beurteilen (BGE 139 I 72, Publigroupe,
E. 10.1.2; Urteile 2C_113/2017, Hallenstadion, E. 6.1; 2C_985/2015,
ADSL II, E. 4.2).
11.6 Für
die Auslegung von Art.7 KG kann auf die Literatur und Praxis zu Art. 102 des Vertrages über die
Arbeitsweise der Europäischen Union (AEUV; Abl. C 115747 vom 9. Mai 2008) gegriffen werden, da die
unzulässigen Verhaltensweisen marktbeherrschender Unternehmen nach Art. 7 KG im Wesentlichen parallel
zu Art. 102 AEUV geregelt sind. Liegen also gleiche Sachlagen vor, so kann primär davon ausgegangen
werden, dass sie gleich beurteilt werden sollen. Davon geht implizit auch das Abkommen vom 17. Mai 2013
zwischen der Schweizerischen Eidgenossenschaft und der europäischen Union über die Zusammenarbeit
bei der Anwendung ihres Wettbewerbsrechts (SR 0.251.268.1) im dritten Erwägungsgrund aus, da "die
Systeme der Schweiz und der [Europäischen] Union für die Durchsetzung des Wettbewerbsrechts
auf denselben Grundsätzen beruhen und vergleichbare Vorschriften enthalten" (BGE 139 I 73,
Publigroupe, E. 8.2.3; Urteil 2C_985/2015, ADSL
II, E. 4.3).
12. Einschränkung
der Erzeugung, des Absatzes oder der technischen Entwicklung i.S.v. Art. 7 Abs. 2 Bst. e KG
12.1 Sachverhalt
12.1.1 In
einem Vertrag zwischen e-mediat und einem Softwarehaus D._______ wurde die Klausel A verwendet, die wie
folgt lautet:
"Soweit es [...] zur
Herstellung oder Weiterentwicklung von Vertragsprodukten als sinnvoll erachtet, den Produktanwendern
zusätzlich den Zugriff auf für sie nützliche Partner- und Produkte-Stamm-Daten (d.h. auf
andere als auf HOSPINDEX- und CIS-Daten) zu ermöglichen, ist sie verpflichtet, dieselben bei e-mediat
zu beschaffen. Soweit e-mediat zu deren Bereitstellung nicht bereit oder dazu nicht innert einer der
Problemstellung angemessenen nützlichen Frist in der Lage ist, ist [...] berechtigt, diese Komponenten
anderweitig zu beziehen."
In einer Zusatzvereinbarung wurde zudem vereinbart, dass die D._______ an Arztpraxen
keine weiteren
Medikamentendaten vertreibe ausser medINDEX.
12.1.2 Eine
(zur Klausel A) weitgehend identische Klausel findet sich in einem weiteren Vertrag zwischen e-mediat
und einem Softwarehaus. Dieser Vertrag wurde von den Parteien zwar unterzeichnet, jedoch nicht datiert.
HCI hat am 29. November 2016 einen neuen Vertrag mit diesem Softwarehaus eingereicht, datiert auf [...],
mit Bezugnahme auf den alten Vertrag, wobei angegeben wird, dieser habe vom [...] datiert. Der neue
Vertrag enthält die oben erwähnte Klausel nicht.
12.1.3 Klausel
B lautet wie folgt und wurde in 83 Verträgen mit Softwarehäusern verwendet, wobei 75 dieser
Verträge aus den Jahren 2012 bis 2014 stammen:
"Ohne vorgängige schriftliche Zustimmung von e-mediat ist
das SWH [Softwarehaus] nicht berechtigt, Daten Dritter in die XML-Strukturen von e-mediat zu implementieren
und/oder Daten in seine SW-Programme einzuspeisen, die nicht von e-mediat stammen und die gleich oder
im Wesentlichen gleich wie Daten von e-mediat strukturiert sind."
12.1.4 Ab
2015 hat HCI eine neue Formulierung gewählt, die in 21 von 23 der seit 2015 abgeschlossenen Verträge
verwendet wurde:
"Kundenindividuelle Daten oder Daten von Dritten dürfen
in der Softwarelösung zu den bestehenden INDEX-Daten hinzugefügt werden, sofern deren Datenquelle
klar ersichtlich ist. Die Datenquelle sowie jegliche Veränderung muss für den Kunden sichtbar
angezeigt werden."
12.1.5 Zu
diesen neuen Verträgen wurden dem Sekretariat keine Vorgängerversionen mit den jeweiligen Softwarehäusern
eingereicht, was den Schluss nahelegt, dass die Mehrheit dieser Softwarehäuser erstmals einen Vertrag
mit HCI abgeschlossen hat.
12.1.6 Die
Vorinstanz kam in der angefochtenen Verfügung zum Schluss, mit den Klauseln A und B läge eine
Alleinbezugspflicht der Softwarehäuser für zusätzliche Partner- und Produkte-Stamm-Daten
sowie eine Untersagung der anderweitigen Verwendung der Strukturen der Softwarehäuser vor. Dadurch
sei der Absatz der Konkurrenten in missbräuchlicher Art und Weise i.S.v. Art. 7 Abs. 1 i.V.m. Abs.
2 Bst. e KG eingeschränkt worden.
12.2 Grundlagen
12.2.1 Art.
7 Abs. 2 Bst. e KG erfasst grundsätzlich alle Formen von Behinderungs- und Verdrängungspraktiken
eines marktbeherrschenden Unternehmens gegenüber Konkurrenten und stellt damit insofern gegenüber
den anderen in Art. 7 Abs. 2 KG genannten Verhaltensweisen einen Auffangtatbestand dar (Rz. 454 der Verfügung
der Vorinstanz vom 19. Oktober 2015 in Sachen Online Buchungsplattformen
für Hotels [veröffentlicht in: RPW 2016/1 S. 67 ff., 125]; Amstutz/Carron,
BSK-KG, Art. 7 N 625; Clerc/Këllezi, CR-Concurrence,
Art. 7 II N 234 f.; Stäuble/Schraner, DIKE-KG, Art.
7 N 458).
12.2.2 Der
Tatbestand will verhindern, dass es durch die Einschränkung der Erzeugung, des Absatzes oder der
technischen Entwicklung zu einer künstlichen Verknappung kommt. Eine Verknappung ist dann künstlich,
wenn sie nicht durch Marktveränderungen ausgelöst wird, sondern durch das Bestreben des Marktbeherrschers
die Preise in die Höhe zu treiben oder sie hoch zu halten (Botschaft KG, BBl 1995 I 468, 574; Weber/Volz,
a.a.O., Rz. 2.721 und 2.723).
12.2.3 Der
Tatbestand der Einschränkung der Erzeugung, des Absatzes
oder der technischen
Entwicklung i.S.v. Art. 7 Abs. 1 i.V.m. Abs. 2 Bst. e KG wird als erfüllt betrachtet, wenn kumulativ
folgende Merkmale vorliegen:
- (i)
Es liegt ein marktbeherrschendes Unternehmen vor, welches
- (ii)
eine Verhaltensweise praktiziert, die zu einer Einschränkung der Erzeugung, des Absatzes oder der
technischen Entwicklung führt;
- (iii)
durch die Verhaltensweise kommt es zu einer künstlichen Verknappung;
- (iv)
die durch die Verhaltensweise bewirkte Einschränkung der Erzeugung, des Absatzes oder der technischen
Entwicklung ist nicht durch objektive Rechtfertigungsgründe gerechtfertigt.
12.3 Marktbeherrschende
Stellung
Die ehemalige Galenica-Gruppe verfügte mittels HCI auf dem Markt für veredelte, maschinenlesbare
Daten betreffend Medikamenteninformationen über eine marktbeherrschende Stellung (s. oben E. 9.2).
12.4 Einschränkung
des Absatzes
12.4.1 Unter
"Einschränkung des Absatzes" im Sinne von Art. 7 Abs. 2 Bst. e KG fallen insbesondere
Verhaltensweisen eines marktbeherrschenden Unternehmens, welche darauf abzielen, das Marketingspektrum
der Konkurrenz zu verringern und dadurch deren Marktzugang künstlich zu beschränken, ohne dass
dies eine Folge der normalen Marktentwicklung bzw. des normalen Leistungswettbewerbs wäre (RPW 2016/1
S. 67 Rz. 455, Online Buchungsplattformen für Hotels; Amstutz/Carron,
BSK-KG, Art. 7 N 662; Clerc/Këllezi, CR-Concurrence,
Art. 7 II N 235; Stäuble/Schraner, DIKE-KG, Art. 7
N 464).
12.4.2 Der
Begriff der Einschränkung erfasst dabei nur Verhaltensweisen, die Produkte oder Dienstleistungen
von Konkurrenten des Marktbeherrschers entweder weniger attraktiv oder weniger absetzbar machen. Verhaltensweisen,
welche die Produkte oder Dienstleistungen des beherrschenden Unternehmens zweckmässiger oder besser
verfügbar machen oder die Behinderung von Konkurrenten, die auf höherwertige Leistungen des
marktbeherrschenden Unternehmens zurückzuführen sind, fallen demgegenüber nicht unter
die Bestimmung, selbst wenn dabei zwangsläufig eine Einschränkung im Sinne des Gesetzeswortlautes
vorliegt (RPW 2016/1 S. 125 Rz. 455, Online Buchungsplattformen für
Hotels; Stäuble/Schraner, DIKE-KG, Art. 7 N
466 f.; vgl. Amstutz/Carron, BSK-KG, Art. 7 N 631 f.).
12.4.3 Einschränkende
Verhaltenswesen ergeben sich nicht nur aus Verboten, durch welche die Marktgegenseite beispielsweise
daran gehindert wird, an andere Wettbewerber zu liefern oder von ihnen gewisse Produkte oder Dienstleistungen
zu beziehen, sondern auch aus der Setzung von Anreizen, welche derartiges Verhalten fördern (Weber/Volz,
a.a.O., Rz. 2.746).
12.4.4 Einerseits
kann die Einschränkung des Absatzes unilateralen Handlungen des marktbeherrschenden Unternehmens
entspringen, indem dieses sich etwa weigert, gewisse Käufer zu beliefern oder seine Geschäftspartner
mit einer Beschränkung des geographischen Marktes oder des Kundenkreises belegt (Amstutz/Carron,
BSK-KG, Art. 7 N 663). Als Beispiel kann unter Bezugnahme auf die europäische Rechtsprechung das
Verhalten eines marktbeherrschenden Unternehmens angeführt werden, dem ein Ausschliesslichkeitsrecht
zusteht, von dem nur mit seiner Zustimmung Abweichungen möglich sind, und das im konkreten Fall
die strikte Einhaltung dieses Rechts verlangt, mit dem Ziel seinen einzigen Konkurrenten vom Markt zu
verdrängen (Urteile des EuG vom 8. Oktober 1996 Rs. T-24, 25, 26 und 28/93 Compagnie
Maritime Belge Transports SA und Compagnie maritime belge SA/Kommission, Slg. 1996 II-1201 ff.
Rn. 108 f.). Andererseits kann ein marktbeherrschendes Unternehmen den Absatz durch bilaterale Handlungen
einschränken, meistens in Verträgen mit Handelspartnern oder Dritten. Darunter fallen insbesondere
Ausschliesslichkeitsbindungen, die als Alleinbezugsbindungen oder als Rabatte in Erscheinung treten (Amstutz/Carron,
BSK-KG, Art. 7 N 664; Stäuble/Schraner, DIKE-KG, Art.
7 N 458). Alleinbezugsbindungen sind dadurch gekennzeichnet, dass der Abnehmer verpflichtet ist, die
Vertragsgegenstände nur von seinem Vertragspartner, d.h. Lieferanten, zu beziehen. Zur Durchsetzung
solcher ausschliesslichen Bezugsbindungen können wirtschaftliche Vor- oder Nachteile wie Erteilung
oder Entzug von Treuerabatten, Auferlegung einer Vertragsstrafe, Lieferungsbruch, etc. vereinbart werden
(Yi-Tien Lin, Die sog. "englische Klausel" in
Bezugsbindungsverträgen und ihre Behandlung im europäischen und deutschen Kartellrecht, 2006,
S. 34 f.).
12.4.5 Zur
Frage, ob Alleinbezugsbindungen absatzeinschränkende Wirkung haben (können), ist kurz auf die
Haltung der Ökonomie einzugehen. Gemäss der Chigago School erreicht ein Produzent, der mit
einem Zwischenhändler eine Alleinbezugsbindung eingehen will, dessen Zustimmung, indem er ihm einen
vorteilhafteren Preis anbietet. Der Verkaufspreis des Zwischenhändlers wiederum sei durch die Kaufbereitschaft
des Konsumenten begrenzt. Daher werde ein rationaler Produzent bzw. Zwischenhändler nur dann an
einer Alleinbezugsbindung interessiert sein, wenn sie Effizienz verspreche. Vertreter der Post Chigago
Economics haben in jüngerer Zeit jedoch gezeigt, dass sich die Chigago School in allzu einseitiger
Weise auf sehr strikte Hypothesen gestützt hatte, namentlich darauf, dass: (1) die Unternehmen eine
nicht-lineare Preisgestaltung verwenden, (2) alle wirtschaftlichen Akteure an der Aushandlung der Alleinbezugsbindungen
beteiligt sind, und (3) ein Unternehmen, das einen Vertrag mit Alleinbezugsbindung abgeschlossen hat,
die Käufer für die dadurch erlittenen Nachteile entschädigen muss. Würden diese Hypothesen
allerdings modifiziert, veränderten sich die Ergebnisse der ökonomischen Analyse. Die Verfechter
der Post Chicago Economics führten in diesem Zusammenhang folgende Überlegungen an: Wenn ein
potenzieller Konkurrent hohe Fixkosten aufwenden müsse, um in einen neuen Markt einzutreten, könne
ein bereits im Markt aktives Unternehmen dessen Markteintritt verhindern, ohne mit allen Käufern
Exklusivverträge eingegangen haben zu müssen; es reiche in diesem Fall aus, wenn das Unternehmen
nur mit einigen wenigen Käufern Exklusivverträge abgeschlossen habe, um zu verhindern, dass
der Konkurrent die für das wirtschaftliche Überleben erforderliche Grösse erreiche. Damit
hat die moderne Theorie nachgewiesen, dass Alleinbezugsbindungen durchaus zu wettbewerbsfeindlichen Zwecken
missbraucht werden können (siehe zum Ganzen Amstutz/Carron, in: Amstutz/Reinert
[Hrsg.], Basler Kommentar zum Kartellgesetz, 1. Aufl., 2010, Art. 7 N 445 [nachfolgend zit.: {Autor},
BSK-KG 2010], nicht mehr diskutiert in der 2. Aufl. 2021).
12.4.6 Dieser
Standpunkt wird heute auch in der Schweizerischen Wettbewerbspraxis vertreten. Danach behindern Alleinbezugsbindungen
aktuelle oder potenzielle Konkurrenten in der Aufnahme des Wettbewerbs, sofern dadurch der Zugang zu
Vertriebskanälen oder zum Endabnehmer eingeschränkt wird (Rz. 64 ff. der Verfügung der
Vorinstanz vom 1. März 1999 in Sachen Beschaffung, Verteilung und
Lagerung von Stiersamen zur künstlichen Besamung von Rindern [veröffentlicht in: RPW
1999/1 S. 75 ff., 88 ff.]; Rz. 29 des Schlussberichts des Sekretariats der WEKO vom 11. Februar
1999 in Sachen Vorabklärung gemäss Art. 26 KG betreffend Distribution
von Feldschlösschen-Hürlimann Bieren [veröffentlicht in: RPW 1999/1 S. 57 ff.,
62 f.]; Weber/Volz, a.a.O., Rz. 2.734). Alleinbezugsvereinbarungen
sind als kartellrechtlich zulässig zu betrachten, wenn sie im gegenseitigen Interesse der Vertragspartner
liegen und in einer normalen, durch Wettbewerb gekennzeichneten Marktsituation getroffen werden. Dies
gilt jedoch nicht für einen Markt, in dem der Wettbewerb wegen der marktbeherrschenden Stellung
eines Geschäftspartners bereits eingeschränkt ist (Stäuble/Schraner,
DIKE-KG, Art. 7 N 469).
12.4.7 Die
Vorinstanz kam zum Schluss, dass durch die Klauseln A und B der Absatz aktueller und potentieller Konkurrenten
eingeschränkt wurde. Die Beschwerdeführerinnen bringen hingegen vor, es handle sich bei den
Klauseln A und B nur um Zustimmungsvorbehalte, welche weder den eigenen Absatz von HCI noch den Absatz
der Konkurrenten eingeschränkt hätten. Die Vorinstanz habe sich auf eine formale Betrachtung
beschränkt und die tatsächliche Einschränkung des Absatzes durch die beiden Klauseln nicht
nachgewiesen. Der mangelnde Erfolg der Konkurrenten liege in den Qualitätsunterschieden der Daten.
12.4.8 Nachfolgend
ist deshalb in einem ersten Schritt zu klären, wie die Klauseln A und B zu qualifizieren sind, d.h.
ob es sich um Alleinbezugsverpflichtungen, Zustimmungsvorbehalte oder Weiteres handelt. In einem nächsten
Schritt ist sodann auf die Frage der Auswirkungen einzugehen.
12.4.9 Die
Vorinstanz erwog zur Klausel A, es sei den Softwarehäusern durch diese Klausel untersagt gewesen,
zusätzliche Partner- und Produkt-Stamm-Daten auf dem Markt zu beschaffen, da sie e-mediat exklusiv
ein Vorrecht gewähren mussten, diese Nachfrage zu befriedigen. Nur falls
e-mediat
diese Daten nicht habe anbieten wollen oder nicht habe anbieten können, sei es den Softwarehäusern
gestattet gewesen, bei anderen Datenveredlern diese Daten zu beschaffen bzw. diese Daten selbst aus Primärquellen
zu beziehen und zu veredeln. Klausel A stelle somit eine Alleinbezugspflicht für neu nachgefragte
Daten zugunsten von e-mediat dar.
12.4.10 Die
Beschwerdeführerinnen rügen, die Klausel A beziehe sich nur auf Daten, die von HCI nicht angeboten
würden, womit der Bezug von Konkurrenzdaten nicht ausgeschlossen werde. Zudem enthalte die Klausel
A kein Verbot zur Zusammenarbeit mit einem Drittanbieter, sondern nur einen Zustimmungsvorbehalt.
12.4.11 Die
Vorinstanz hält dem wiederum entgegen, bei der Klausel A spreche bereits deren Wortlaut gegen ein
reines Zustimmungserfordernis zwecks Verhinderung von Leistungsstörungen.
12.4.12 Die
Vorbringen der Beschwerdeführerinnen gegen die Qualifikation der Klausel A als Alleinbezugsverpflichtung
überzeugen nicht. So kann einerseits dem Argument, die Klausel betreffe nur Daten, die nicht von
HCI angeboten werden, nicht gefolgt werden. Denn gemäss Wortlaut der Klausel sind alle anderen Daten
als jene im HOSPINDEX bzw. in den CIS-Daten enthaltenen betroffen. Damit kann es sich durchaus um Daten
handeln, die HCI anderen Kunden bereits anbietet oder in Zukunft anbieten möchte. Zudem ist als
Ausgangspunkt der gesamte relevante Markt, d.h. der Markt für veredelte, maschinenlesbare Daten
betreffend Medikamenteninformationen und nicht nur der Markt für jene veredelten, maschinenlesbaren
Daten betreffend Medikamenteninformationen, die HCI aktuell der D._______ anbot, zu betrachten. Insofern
ist die Vorinstanz zutreffend zum Schluss gekommen, dass es sich um Konkurrenzdaten handelt.
12.4.13 Auch
das Argument, es handle sich nicht um ein Verbot, sondern lediglich um einen Zustimmungsvorbehalt, vermag
nicht zu überzeugen. Wie die Vorinstanz zutreffend festhielt, spricht bereits der Wortlaut der Klausel
A gegen eine solche Auslegung. Gemäss Wortlaut handelt es sich um ein Verbot zusätzliche Daten
von Konkurrenten zu beziehen, wenn HCI diese selbst anbieten will und kann.
12.4.14 Zudem
blieb in der angefochtenen Verfügung unberücksichtigt, dass HCI mit D._______ in der Zusatzvereinbarung
vom 6. bzw. 13. September 2012 zusätzlich vereinbart hat, dass die D._______ an Arztpraxen keine
weiteren Medikamentendaten vertreibe ausser medINDEX ([...]). Bei dieser Zusatzvereinbarung, welche
abgeschlossen wurde, nachdem das Bundesverwaltungsgericht 2011 die Publikationspflicht im Compendium
aufgehoben hatte und bevor Anfang 2013 AIPS in Betrieb genommen wurde, liegt ein Verbot vor, veredelte,
maschinenlesbare Daten betreffend Medikamenteninformationen von Konkurrenten zu beziehen; und zwar sämtliche
und nicht nur solche, die HCI D._______ aktuell mit medINDEX bereits anbot. Die D._______ wurde also
verpflichtet, ihren gesamten Bedarf betreffend veredelte, maschinenlesbare Daten betreffend Medikamenteninformationen
bei HCI zu decken.
12.4.15 Zusammenfassend
ergibt sich, dass die Vorinstanz die Klausel A zu Recht als Alleinbezugsverpflichtung beurteilt hat.
Die Alleinbezugspflicht wird zudem durch die Zusatzvereinbarung vom 6. bzw. 13. September 2012 unterstrichen.
12.4.16 Zur
Klausel B erwog die Vorinstanz, sie untersage es den Softwarehäusern, die vorhandenen Strukturen
für Produkte anderer Datenveredlern bzw. für eigene Datenbanken zu verwenden, wenn die Softwarehäuser
selbst die Daten veredeln wollten. So werde sichergestellt, dass e-mediat weiterhin die Daten in
komplettem Umfang liefern könne und es den Softwarehäusern nicht möglich sei, beispielsweise
die Medikamenteninformationen von einem Konkurrenten zu beziehen oder die Arzneimittelinformationen direkt
aus AIPS zu laden und selbst zu veredeln, während e-mediat die Non-Pharma Daten liefere. Während
der kritischen Periode (2012-2014) sei die Klausel systematisch bei der Erneuerung von Verträgen
oder mittels Abschluss von Zusätzen zu bestehenden Verträgen eingebaut worden. Da HCI am 29.
November 2016 von den meisten dieser Verträge keine neue Version eingereicht habe, sei davon auszugehen,
dass diese Klauseln in diesen Verträgen noch gültig seien.
12.4.17 Dagegen
bringen die Beschwerdeführerinnen vor, es handle sich auch bei der Klausel B nur um einen Zustimmungsvorbehalt
und damit um kein Verbot und keine Alleinbezugsverpflichtung. Die Klausel B wäre nur dann zur Anwendung
gekommen, wenn ein Softwarehaus Drittdaten direkt in die XML-Strukturen der HCI implementieren würde
oder wenn Drittanbieter die Datenbankstrukturen der HCI nachahmen würden. Wenn aber die Konkurrenzdaten
nicht in die Datenbankstrukturen der HCI eingepflegt würden bzw. wenn die Datenbankstruktur nicht
"abgekupfert" würde, sei keine Erlaubnis von HCI erforderlich gewesen.
12.4.18 Gemäss
Wortlaut der Klausel B war eine schriftliche Zustimmung von HCI notwendig, wenn die Konkurrenzdaten in
die Datenbankstrukturen der HCI eingepflegt werden oder wenn die Konkurrenzdaten im Wesentlichen gleich
strukturiert waren. Ohne Zustimmung von HCI lag somit in diesem Fällen ein Verbot vor. Eine Zustimmung
von HCI war nur dann nicht erforderlich, wenn die Konkurrenzdaten nicht in die Datenbankstruktur von
HCI eingepflegt werden wollten und auch nicht gleich oder
im Wesentlichen gleich strukturiert waren.
12.4.19 Durch
das Zustimmungserfordernis lag keine reine Alleinbezugspflicht vor. Allerdings weist dieses Zustimmungserfordernis
Ähnlichkeiten mit der sogenannten "englischen Klausel"
auf. Die englische Klausel verpflichtet den Abnehmer dazu, dem Lieferanten ein besseres bzw. günstigeres
Angebot eines konkurrierenden Lieferanten zu melden und nur darauf einzugehen, wenn der Lieferant ihm
kein entsprechendes günstiges Angebot unterbreitet (Reinert,
BSK-KG, Art. 4 Abs. 1 N 742; Weber/Volz, a.a.O., Rz. 2.642;
Urs Egli, Die Bedeutung des Kartellrechts in der Vertragspraxis
[2. Teil], recht 2014, S. 67 ff., S. 73). Sowohl die englische Klausel als auch die vorliegende Klausel
enthält eine Offenlegungspflicht des Abnehmers. Wenn der Abnehmer von der Klausel Gebrauch macht,
muss er den Lieferanten über das konkurrierende Angebot bzw. die konkurrierenden Konditionen unterrichten.
Ohne eine Mitteilung über die Existenz eines Konkurrenzangebots kann der Abnehmer nicht von seiner
Abnahmepflicht befreit werden (Yi-Tien Lin, a.a.O., S. 54;
vgl. auch Amstutz/Car-ron, BSK-KG, Art. 7 N 429; Weber/Volz,
a.a.O., Rz. 2.642). Sowohl die englischen Klauseln als auch die vorliegende Klausel mit dem Zustimmungsvorbehalt
erlauben es in den Besitz von Informationen über die Marktlage sowie über die Möglichkeiten
und das Vorgehen der Wettbewerber zu gelangen, die für die Marktstrategie ausserordentlich wertvoll
sind. Der Lieferant gewinnt einen Einblick in Konkurrenzangebote und die Marktstrategie des konkurrierenden
Lieferanten, die er sonst unter normalem Marktverfahren nicht erhalten hätte. Beide Klauseln können
insbesondere dazu dienen, Marktinformationen und Einzelheiten über die Konkurrenzangebote zu sammeln,
um Preis- bzw. Angebotsanpassungen vorzunehmen; was die Konkurrenten darin behindert, Marktanteile zu
gewinnen.
12.4.20 Deshalb
können Alleinbezugsverpflichtungen selbst wenn sie mit einer englischen Klausel verbunden werden,
wettbewerbsschädliche Wirkungen haben. Zudem kann auch die Vereinbarung einer englischen Klausel
für sich allein betrachtet zu einer missbräuchlichen Wettbewerbsbeschränkung führen
(Weber/Volz, a.a.O., Rz. 2.737). Teilweise wird in
der Lehre davon ausgegangen, dass englische Klauseln von marktmächtigen Unternehmen per se nicht
vereinbart werden dürfen (Egli, a.a.O., S. 73; Wirtz,
in: Mäger, Europäisches Kartellrecht, 5. Aufl. 2012, Kap. 6 Rz. 76). Teilweise geht die Lehre
davon aus, dass es von den konkreten Faktoren des Marktes abhängig sei, ob eine englische Klausel
Verdrängungswirkungen entfalte (Weber/Volz, a.a.O.,
Rz. 2.643, 2.645 und 2.737, Amstutz/Carron, BSK-KG, Art.
7 N 429; vgl. Reinert, BSK-KG, Art. 4 Abs. 1 N 752).
12.4.21 Im
Urteil vom 12. Februar 1979 85/76 Hoffmann-La Roche & Co. AG
gg. Kommission hielt der EuGH gar fest, dass eine englische Klausel auch unter günstigsten
Umständen keine merkliche Milderung der Wettbewerbsverzerrung bewirke, welche die ausschliesslichen
Bezugsverpflichtungen [und Treuerabatte] auf einem Markt schaffen, der bereits eine geschwächte
Wettbewerbsstruktur aufweist, weil auf ihm ein Unternehmen in beherrschender Stellung tätig ist;
vielmehr verstärke diese sogar den missbräuchlichen Charakter der Ausnutzung der beherrschenden
Stellung (Urteil des EuGH vom 12. Februar 1979 85/76 Hoffmann-La
Roche & Co. AG/Kommission, Slg. 1979 -00461 Rn. 107). Im Fall BP-Kemi
- DDSF sah die Kommission in der Verwendung einer englischen Klausel in der Alleinbezugsvereinbarung
eine Wettbewerbsbeschränkung i.S.v. Art. 81 Abs. 1 des Vertrages zur Gründung der Europäischen
Gemeinschaft (EG-Vertrag, EGV; ABl. EG Nr. L 157/11). Aufgrund der Ermittlung des konkurrierenden Marktverhaltens
und der Abschreckung des Wettbewerbers wurde die englische Klausel allein als wettbewerbsbeschränkend
beurteilt. Darüber hinaus leitete die Kommission auch den wettbewerbsbeschränkenden Charakter
der englischen Klausel aus der Gesamtbetrachtung in Verbindung mit der durch die englische Klausel ergänzten
ausschliesslichen Bezugsbindung und der langfristigen Bezugsbeziehung ab (sechsjährige Bezugsbindung;
Entscheidung 79/934/EWG der Kommission vom 5. September 1979 in einem Verfahren nach Art. 85 EWG-Vertrag,
COMP/IV/29.021 BP Kemi - DDSF, Abl. L 286/32; vgl. Yi-Tien
Lin, a.a.O., S. 103). Im Fall Natriumkarbonat - Solvay
stellte die Kommission ähnlich fest, dass die englische Klausel den wettbewerbsfeindlichen Effekt
der langfristigen Liefervereinbarungen oder Treuerabatte nicht mildere, sondern die Bindung des Abnehmers
an den Lieferanten verstärke. Denn durch die englische Klausel erhalte der Lieferant Kenntnis über
die Absichten seiner Wettbewerber und der Vorteil des Lieferanten gegenüber seinen Wettbewerbern
werde dadurch festgeschrieben (Entscheidung 91/297/EWG der Kommission vom 19. Dezember 1990 in einem
Verfahren nach Art. 85 EWG-Vertrag, COMP/IV/33.133-A Soda - Solvay,
Abl. L 152/1 Rz. 35, 37 und 60; Entscheidung 2003/6/EG der Kommission vom 13. Dezember 2000 in einem
Verfahren nach Art. 82 EG-Vertrag, COMP/33.133-C Natriumkarbonat - Solvay,
Abl. L 10/10 Rz. 111, 122 und 177 ff.). Im Fall Industriegase
befand die Kommission schliesslich ebenfalls, dass die englische Klausel zu streichen sei, liess jedoch
eine Ausnahme zu. Die englische Klausel könne dann weiterhin verwendet werden, wenn der Abnehmer
(aber nicht der Lieferant) die Einbeziehung einer englischen Klausel in den Vertrag fordere und wenn
die notwendige Vorsorgemassnahme ergriffen werde, die gewährleiste, dass der Lieferant nicht den
günstiger anbietenden Wettbewerber identifizieren könne (Kommission, 19. Bericht über
die Wettbewerbspolitik, 1989, Rz. 62 Industriegase; Pressemitteilung
der Kommission IP/89/426 vom 7. Juni 1989 Air Liquide etc., Ziff.
5 [abrufbar unter: https://europa.eu/rapid/press-release_IP-89-426_en.htm {abgerufen am 18.08.2020}];
Yi-Tien Lin, a.a.O., S. 107 f.).
12.4.22
Die Klausel B mit ihrem Zustimmungsvorbehalt war somit aufgrund der möglichen Ermittlung
des konkurrierenden Marktverhaltens und der Abschreckung der Wettbewerber geeignet, aktuellen und potentiellen
Konkurrenten den Zugang zu Vertriebskanälen und zu Endabnehmern einzuschränken. Darüber
hinaus ergibt sich dies auch aus einer Gesamtbetrachtung der Klausel B mit der in den Verträgen
in der Regel auf 36 Monate festgelegten Mindestbezugsdauer (vgl. Vorinstanz, act. 1120, i.d.R. Ziff.
19 des Vertrages) sowie der regelmässig zu findenden Vereinbarung einer Konventionalstrafe von Fr.
[...] bei Vertragsverletzung durch das Softwarehaus (vgl. Vorinstanz, act. 1120, i.d.R. Ziff. 5 der
Beilage 7).
12.4.23
An diesem Ergebnis vermag auch die Rüge der Beschwerdeführerinnen, die Vorinstanz habe
nicht zwischen den angeblichen Wirkungen der Klausel A und Klausel B unterschieden, nichts zu ändern.
Zwar sind die beiden Klauseln nicht identisch. Es handelt sich wie oben ausgeführt bei Klausel A
um eine Alleinbezugsverpflichtung im eigentlichen Sinne und bei Klausel B "lediglich" um eine
Klausel, die ähnliche Wirkung entfaltet. Da ihre Wirkung jedoch ähnlich ist und sie auch den
gleichen Bereich betreffen, ist die Vorinstanz darin zu stützen, wenn sie davon ausgeht, dass eine
isolierte Betrachtung der einzelnen Klauseln zu kurz greift.
12.4.24 Die
Beschwerdeführerinnen bringen vor, die Klausel A sei nur in einem Vertrag bzw. in 0.57% aller Verträge
vorgesehen gewesen. Demzufolge könne ihr keine nennenswerte den Absatz einschränkende Wirkung
zugesprochen werden. Die Klausel B sei nur in 83 Verträgen bzw. in 47% aller Verträge gewesen,
womit die überwiegende Mehrheit der Softwarehäuser nicht an eine solche Klausel gebunden gewesen
sei. Deshalb könnten die beiden Klauseln nicht am mangelnden Erfolg von ywesee und ouwerkerk schuld
gewesen sein.
12.4.25 Auch
dieses Vorbringen ist nicht stichhaltig. Wenn ein potenzieller Konkurrent hohe Fixkosten aufwenden muss,
um in einen neuen Markt einzutreten, kann ein bereits im Markt aktives Unternehmen dessen Markteintritt
verhindern, ohne mit allen Käufern Exklusivverträge eingegangen zu sein. Es reicht in diesem
Fall aus, wenn das Unternehmen nur mit einigen wenigen Käufern Exklusivverträge abgeschlossen
hat, um zu verhindern, dass der Konkurrent die für das wirtschaftliche Überleben erforderliche
Grösse erreicht. Die WEKO hat im Fall Beschaffung, Verteilung und
Lagerung von Stiersamen zur künstlichen Besamung von Rindern beispielsweise festgehalten,
dass die abgeschlossenen Exklusivverträge im Ergebnis nur 18% der Stierbesamungen auf dem Gesamtmarkt
auf sich vereinigten, dass dieses Verteilnetz aber einen flächendeckenden Besamungsdienst in Platz
setze, der es dem SVKB ermögliche, "die Etablierung von konkurrenzierenden KB-Unternehmen zu
erschweren" (RPW 1999/1 S. 75 ff. Rz. 66, Beschaffung, Verteilung
und Lagerung von Stiersamen zur künstlichen Besamung von Rindern).
12.4.26 In
casu wurden die beiden fraglichen Klauseln (bzw. vorwiegend Klausel B) in knapp der Hälfte und in
der Periode von 2012 und 2014, als sich der Markt aufgrund der Einführung von AIPS hätte öffnen
können, in knapp Dreiviertel aller abgeschlossenen Verträge mit den Softwarehäusern verwendet.
Angesichts dessen kann vorliegend aus der Anzahl Verträgen mit den fraglichen Klauseln nicht geschlossen
werden, diese hätten keine absatzeinschränkende Wirkung.
12.4.27 Im
Übrigen ist die Vorgehensweise der Vorinstanz im Zusammenhang mit der Klausel A, indem sie zwar
erwähnt, dass in einem weiteren Vertrag mit einem Softwarehaus eine mit der Klausel A vergleichbare
Klausel zu finden sei, diesen aufgrund der fehlenden Datierung und des neuen Vertrages vom September
2015 im Ergebnis aber nicht berücksichtigt, nicht zu beanstanden.
12.4.28 Gemäss
den Beschwerdeführerinnen habe HCI nie eine Anfrage um Erlaubnis für die Zusammenarbeit mit
einer Drittfirma verweigert. Die Vorinstanz führe auch kein Beispiel an, bei dem die Klausel den
Absatz tatsächlich beschränkt habe. Vielmehr habe HCI E._______ eine Zusammenarbeit mit ywesee
erlaubt. Weiter habe HCI auch [...] Softwarehäusern erlaubt, die Daten der Datenbank [...] von
F._______ mit Informationen zur sicheren Handhabung der Medikamentenabgabe zu verwenden. Diese Daten
habe sie diesen neun Softwarehäusern sogar über ihren Server zur Verfügung gestellt. Auch
die Klausel A sei während der Zusammenarbeit mit der D._______ nie von Relevanz gewesen und die
D._______ habe sich nie darauf berufen. Vielmehr habe die D._______ die Klausel als bedeutungslos qualifiziert.
Die Klauseln A und B hätten sich entsprechend gar nicht ausgewirkt.
12.4.29 Die
Vorinstanz entgegnet dem jedoch, aus dem Umstand, dass die Beschwerdeführerinnen selbst mit keiner
Anfrage konfrontiert worden sei, könne nicht gefolgert werden, dass die Klauseln sich nicht ausgewirkt
hätten. Denn insbesondere vor dem Hintergrund der übrigen Umstände könne bereits
die vertragliche Festlegung verschliessende Wirkung zeitigen. Die Marktzutrittsschranken seien für
allfällige Drittanbieter bereits ohne die Klauseln sehr hoch gewesen. Bei der Klausel A sei zudem
zu berücksichtigen, dass Ärztinnen und Ärzte erst allmählich auf umfassende Praxisadministrationssoftware
und elektronische Patientendossiers umsteigen würden und dass mit D._______ (und einem weiteren
Softwarehaus) zwei Keyplayer in diesem Segment gebunden worden seien, welche potentiell der Zugang zu
einer erforderlichen kritischen Masse und Kenntnis deren Bedürfnisse zukommen würde. Zudem
sei die Klausel A gerade im Segment der Ärztinnen und Ärzte verwendet worden, wo ywesee heute
nur als Nischenanbieterin tätig sei.
12.4.30 Die
Beschwerdeführerinnen erachten es hingegen als ungenügend, festzuhalten, die Klauseln hätten
möglicherweise Wirkungen gehabt. Die Argumentation der Vorinstanz lasse vielmehr darauf schliessen,
dass die Auswirkungen nicht klar seien. Die Beschwerdeführerinnen sind der Auffassung, die Vorinstanz
hätte die Wirkungen nachweisen müssen.
12.4.31 Zunächst
ist darauf hinzuweisen, dass die Klauseln selbst in Fällen, in denen HCI eine Zusammenarbeit mit
einer Drittfirma erlaubt haben will, nicht per se unproblematisch erscheinen. Denn auch dann kommt die
Offenlegungspflicht des Softwarehauses, mit der HCI über das konkurrierende Angebot unterrichtet
werden muss, zum Zug. Dadurch gelangt HCI auch in diesen Fällen in den Besitz von Informationen
über die Marktlage sowie über die Möglichkeiten und das Vorgehen der Wettbewerber. HCI
gewinnt so einen Einblick in Konkurrenzangebote und die Marktstrategie des konkurrierenden Lieferanten,
den sie sonst unter normalen Marktverfahren womöglich nicht erhalten würde (s. oben E. 12.4.19).
12.4.32 Darüber
hinaus ist mit der Vorinstanz davon auszugehen, dass bereits die vertragliche Festlegung Absatz einschränkende
Wirkungen zeitigen kann, insbesondere auch vor den von der Vorinstanz erwähnten Umständen.
Die Beschwerdeführerinnen gehen fehl, wenn sie rügen, die Vorinstanz hätte die Wirkungen
weitergehend nachweisen müssen. Denn eine solche Auslegung würde auch der unten in den Erwägungen
12.5.5
- 12.5.9
ausführlich darzulegenden Rechtsprechung widersprechen, wonach bereits die Möglichkeit eines
Eintritts nachteiliger Einwirkungen auf den Wettbewerb als ausreichend zu qualifizieren ist und nicht
tatsächlich verifizierbare Schädigungen des Wettbewerbs eintreten müssen.
12.4.33 Weiter
bringen die Beschwerdeführerinnen vor, die Softwarehäuser im April 2017 darüber informiert
zu haben, dass sie nicht mehr länger an die Klausel B gebunden seien. Die Aufhebung der Klausel
habe zu keinen Veränderungen in den Wettbewerbsverhältnissen geführt, was die fehlende
Wirkung der Klausel beweise.
12.4.34 Wie
die Vorinstanz zutreffend festhält, können aus einem späteren Verlauf unter anderen tatsächlichen
Gegebenheiten - insbesondere bei komplexen Märkten und in Zusammenhang mit Innovationswettbewerb
- keine aussagekräftigen Schlüsse für frühere Perioden gezogen werden. Die
heutige Wettbewerbssituation unterscheidet sich von der damaligen Wettbewerbssituation. Damals bestanden
andere regulatorische Bedingungen als heute und die Wettbewerbsverhältnisse haben sich in den vergangenen
Jahren gefestigt. Insofern ist auch dieses Vorbringen der Beschwerdeführerinnen nicht stichhaltig.
12.4.35 Im
Weiteren wollen die Beschwerdeführerinnen berücksichtigt wissen, dass die Softwarehäuser
im Regelfall nur Vermittler seien. Die Leistungserbringerinnen und -erbringer seien als effektive Nutzer
und Kunden der HCI in keiner Weise verpflichtet, in eine ausschliessliche Bezugsverpflichtung mit HCI
zu treten. Entsprechend seien die Kunden der HCI frei, mit alternativen Datenanbietern Verträge
abzuschliessen.
12.4.36 Aus
diesem Argument lässt sich jedoch nichts zugunsten der Beschwerdeführerinnen ableiten. Denn
eine Vorgehensweise nach der Argumentation der Beschwerdeführerinnen hätte zur Folge, dass
die Leistungserbringerinnen und -erbringer mit der bestehenden Software gewisse Funktionen nutzen und
für die veredelten Medikamenteninformationen eine andere Software nutzen müssten. Offensichtlich
würde es dabei an den für die unterschiedlichen Funktionen nötigen Schnittstellen fehlen.
Eine solche Lösung erscheint für die Leistungserbringerinnen und -erbringer keine gangbare
Alternative darzustellen. Es erscheint offensichtlich, dass die Leistungserbringerinnen und -erbringer
nach Möglichkeit eine Software nachfragen, die möglichst alle Bereiche abdeckt. Hinzukommt,
dass die meisten existierenden Softwarehäuser mit HCI einen Vertrag abgeschlossen haben, somit kaum
Ausweichmöglichkeiten vorhanden sind.
12.4.37 Schliesslich
bringen die Beschwerdeführerinnen unter Hinweis auf die Qualität ihrer Datenbanken sinngemäss
vor, die INDEX-Datenbanken seien dank der Klauseln A und B zweckmässiger, da sie im Interesse der
Kunden und der öffentlichen Gesundheit gegen redundante, überflüssige und unübersichtliche
zusätzliche Daten von Drittanbietern geschützt seien. Wie bereits erwähnt fallen Verhaltensweisen,
welche die Produkte oder Dienstleistungen des marktbeherrschenden Unternehmens zweckmässiger machen,
nicht unter Art. 7 Abs. 2 Bst. e KG, selbst wenn dabei zwangsläufig eine Einschränkung im Sinne
des Gesetzeswortlauts vorliegt (s. E. 12.4.2).
12.4.38 Die
Beschwerdeführerinnen stellen sich sinngemäss auf den Standpunkt, die Qualität der Datenbanken
und der Begriff "Zweckmässigkeit" bemesse sich insbesondere an den Faktoren Validierung,
Vollständigkeit und Umfang der Daten. Daneben würden aber auch Eigenschaften wie Mehrsprachigkeit,
einheitliche Abfolge und Darstellung, Einschlägigkeit, Kürze und Präzision sowie zusätzliche
Inhalte und Angaben ins Gewicht fallen.
12.4.39 Die
Qualität von Daten beurteilt sich anhand von vielen Aspekten (z.B. Vollständigkeit, Konsistenz,
Plausibilität, Genauigkeit, Konformität; Alexander Thamm/Michael
Gramlich/Alexander Borek, The Ultimate Data and Ai Guide, 2020, S. 37 f.). Generell gilt: Je konsistenter,
genauer und vollständiger die Daten sind, desto besser. Ab welchem Punkt eine schlechte Datenqualität
die Projektimplementierung oder die Funktionalität eines künstlichen Intelligenzsystems gefährdet,
ist jedoch vom jeweiligen Produkt abhängig (Thamm/Gramlich/Borek,
a.a.O., S. 39). Es kann grundsätzlich davon ausgegangen werden, dass "smart data", d.h.
aus big data-Datenbeständen ermittelte nutzbringende, abgesicherte und hochwertige Daten, in der
Regel qualitativ besser sind als big data, d.h. riesige unstrukturierte Datenmengen, die mit den bisherigen
Methoden nicht analysiert oder verarbeitet werden können (vgl. James
A. George/James A. Rodger, Smart Data: Enterprise Performance Optimization Stategy, Hoboken 2010).
Nicht nur beim ärztlichen Einsatz gegenüber Patienten, sondern generell sind mehrsprachig,
einheitlich, präzis und knapp gehaltene Daten gegenüber unformatiert redundanten Datenmengen
nützlicher, zuverlässiger und zeitsparender (vgl. Michael
Nonnemacher/Daniel Nasseh/Jürgen Stausberg, Datenqualität in der medizinischen Forschung,
Leitlinie zum adaptiven Management von Datenqualität in Kohortenstudien und Registern, 2. Aufl.,
2014).
12.4.40 Die
Daten zu den einzelnen Arzneimitteln in den INDEX-Datenbanken erscheinen im Vergleich mit den Einträgen
in anderen Datenbanken (z.B. MEDIupdate XML von ywesee oder AIPS)
übersichtlich strukturiert und präzis. Zudem enthalten sie weitere ergänzende Angaben
wie beispielsweise Clinical Decision Support, Kurzinformation, Foto des Präparats, Krankenkassen-Rückerstattungsinformationen,
Link zu Packungsbeilage, Preis, Abgabekategorie, was offensichtlich zur Qualität ihrer Datenbank
beiträgt (vgl. Vorinstanz act. 1093).
12.4.41 Für
die vorliegend zu prüfende Frage der Zweckmässigkeit des Verhaltens ist jedoch nicht entscheidend,
ob die Qualität der Datenbank an sich zweckmässig ist, sondern ob die Klauseln A und B für
die Qualitätssicherung zweckmässig waren, was mit den vorerwähnten Feststellungen noch
nicht beantwortet ist. Die Beschwerdeführerinnen betonen die Wichtigkeit der Qualität der INDEX-Datenbanken
sowie die Wirkungslosigkeit der Klauseln. Sie unterlassen es aber darzulegen, inwiefern die Qualität
ihrer Datenbanken durch die Gewährung des Zugriffs auf Daten von Drittanbietern bzw. durch die Verwendung
ihrer XML-Strukturen für (im Wesentlichen) gleich strukturierten Daten von Drittanbietern konkret
beeinträchtigt würde.
12.4.42 Wenn
durch einen Datenbankimport beispielsweise Daten aus med-drugs von ouwerkerk oder aus MEDIupdate XML
von ywesee neben den Daten der INDEX-Datenbanken in die Softwareprogramme eingespeist würden, dürfte
ein Benutzer in der Regel rasch eine Wiederholung erkennen und bemerken, dass es sich um eine abweichende
Datenquelle mit allenfalls weniger vollständig oder sprachlich limitierten Angaben zum selben Arzneimittel
handelt. Zwar ist es durchaus denkbar, dass diesfalls einzelne Angaben aus der Datenquelle des Drittanbieters
mit jenen in den INDEX-Datenbanken im Kontrast oder Widerspruch stünden. Die Beschwerdeführerin
weist insofern zurecht darauf hin, dass ein Eintrag deshalb insgesamt widersprüchlich wirken könne.
Dessen Ursache muss jedoch nicht zwangsläufig in fehlerhaften Angaben liegen. Denn es ist auch denkbar,
dass ein Kontrast oder Widerspruch auf abweichende Auffassungen der Fachwelt oder revidierte Erkenntnisse
der Behörden zurückzuführen ist, so dass der Datenbankbenutzer durch die Angaben aus zusätzlichen
Datenquellen auf heikle Fragen oder einen Meinungsstreit hingewiesen wird. Zudem wurde mit den Klauseln
A und B auch die Einspeisung von Daten mit neuen ausländischen Erkenntnissen verhindert, was sich
negativ auf die Qualität der Daten auswirken kann. Insgesamt ergibt sich, dass die Zweckmässigkeit
der Klauseln A und B für die Qualitätssicherung nicht grundsätzlich bejaht werden kann.
12.4.43 Das
Tatbestandsmerkmal, dass das marktbeherrschende Unternehmen eine Verhaltensweise praktiziert, die zu
einer Einschränkung des Absatzes führt, ist demzufolge gegeben.
12.5 Künstliche
Verknappung
12.5.1 Im
Fokus von Art. 7 Abs. 2 Bst. e KG stehen Behinderungs- bzw. Verdrängungspraktiken des marktbeherrschenden
Unternehmens gegenüber Konkurrenten. Erfasst werden Verhaltensweisen, die den Marktzugang von aktuellen
oder potenziellen Konkurrenten beschränken, ohne dass dies Folge der normalen Marktentwicklung bzw.
des normalen Leistungswettbewerbs ist (Rz. 134 der Verfügung der Vorinstanz vom 14. Juli 2014 in
Sachen Preispolitik und andere Verhaltensweisen der SDA [veröffentlicht
in: RPW 2014/4 S. 670 ff., 688]; Clerc/Këllezi, CR-Concurrence,
Art. 7 II N 235).
12.5.2 Nach
den Materialien ist für das Vorliegen eines Missbrauchs i.S.v. Art. 7 Abs. 2 Bst. e KG nicht nur
ein Einschränkungssachverhalt, sondern auch eine "künstliche Verknappung" erforderlich.
Eine Verknappung ist dann künstlich, wenn sie nicht durch Marktveränderungen ausgelöst
wird, sondern durch das Bestreben des Marktbeherrschers die Preise in die Höhe zu treiben oder sie
hoch zu halten (Botschaft KG, BBl 1995 I 468, 574).
12.5.3 Der
Begriff der künstlichen Verknappung nähert sich damit dem Konzept der Wettbewerbsschädigung
an. Gemäss dem Urteil des Bundesverwaltungsgerichts B-2798/2018 vom 16. Februar 2021 i.S. Naxoo
muss eine Wettbewerbsbeeinträchtigung in Gestalt einer Marktzugangsbeschränkung von
aktuellen oder potenziellen Konkurrenten vorliegen, ohne dass dies Folge einer normalen Marktentwicklung
ist (Urteil des BVGer
B-2798/2018 vom 16. Februar 2021, Naxoo,
E. 11.4.4; vgl. Amstutz/Carron, BSK-KG, Art. 7 N 669). Ein
Teil der Lehre ist der Auffassung, die Einschränkung von Erzeugung, Absatz und technischer Entwicklung
sei bereits dann missbräuchlich, wenn die Wettbewerbsfähigkeit der Mitbewerber betroffen ist
(Clerc/Këllezi, CR-Concurrence, Art. 7 II N 246) bzw.
verlangt nicht explizit das Vorliegen einer wettbewerbsschädlichen Wirkung (Borer,
a.a.O., Art. 7 N 26; Dähler/Krauskopf/Strebel, in:
Geiser/Krauskopf/Münch, Schweizerisches und europäisches Wettbewerbsrecht, 2005, Rz. 8.93 ff.;
von Büren/Marbach/Ducrey, Immaterialgüter- und
Wettbewerbsrecht, 3. Aufl. 2008, N 1550). Demgegenüber vertreten Amstutz/Carron
die Auffassung, der Schluss von einer Wettbewerb-Behinderung auf eine Wettbewerbs-Schädigung
sei unzulässig. Es müsse nebst der Rivalenbehinderung gesondert dargetan werden, dass ein von
Bst. e erfasstes Verhalten eine Wettbewerbsschädigung erzeuge (Amstutz/Carron,
BSK-KG, Art. 7 N 670). Und auch nach Weber/Volz muss neben
der Einschränkung der Produktion, des Absatzes oder der technischen Entwicklung eine Wettbewerbsbeschränkung
vorliegen (Weber/Volz, a.a.O., Rz. 2.746). Das Vorliegen
einer Wettbewerbsbehinderung wird auch von Stäuble/Schraner
vorausgesetzt. Die Verhaltensweise, die zu einer Einschränkung führe, müsse andere Unternehmen
in der Aufnahme oder Ausübung des Wettbewerbs behindern oder die Marktgegenseite benachteiligen
(Stäuble/Schraner, DIKE-KG, Art. 7 N 473 f.).
12.5.4 Nach
europäischem Wettbewerbsrecht führen Exklusivitätsvereinbarungen, an denen marktbeherrschende
Unternehmen beteiligt sind, praktisch immer zu einer nicht hinnehmbaren Beeinträchtigung des Marktzuganges,
weil sie die Konkurrenten des marktbeherrschenden Unternehmens am Absatz ihrer Produkte an die exklusiv
gebundenen Kunden hindern. Sie werden daher als missbräuchlich beurteilt (Wirtz,
a.a.O., Kap. 6 Rz. 76; Mestmäcker/Schweitzer, Europäisches
Wettbewerbsrecht, 3. Aufl. 2014, § 18 Rz. 45 ff.).
12.5.5 Das
Bundesverwaltungsgericht hat im Urteil B-831/2011 vom 18. Dezember 2018 in Sachen SIX
zu verschiedenen Einzelfragen hinsichtlich der Wettbewerbsbehinderung in allgemeiner Weise Stellung genommen.
So ist das Bundesverwaltungsgericht unter Auslegung von Art. 7 KG und unter Berücksichtigung des
Schutzzwecks zum Schluss gelangt, dass Art. 7 KG kein Erheblichkeitsmerkmal im Sinne einer Geringfügigkeitsschwelle
aufweise. Dieses Ergebnis entspricht der Beurteilung von Erheblichkeitseinwänden durch die EU-Wettbewerbspraxis,
wonach weder eine de minimis-Schwelle vorgesehen ist noch ein spürbarer Einfluss auf den Wettbewerb
verlangt wird. Für die Verwirklichung einer Wettbewerbsverfälschung
nach Art. 7 KG ist es demnach nicht erforderlich, dass die nachteiligen Einwirkungen auf den Wettbewerb
durch das missbräuchliche Verhalten eine bestimmte Erheblichkeitsschwelle überschreiten (Urteil
B-831/2011, SIX, E. 1132 ff., insb. E. 1144-1146).
12.5.6 Ebenso
untersuchte das Bundesverwaltungsgericht in diesem Entscheid, wie für ein marktmissbräuchliches
Verhalten der Nachweis über das Vorliegen einer Wettbewerbsverfälschung zu führen ist
bzw. es ging der Frage nach, ob im Sinne eines Gefährdungsdelikts bereits die Möglichkeit eines
Eintritts nachteiliger Einwirkungen für die Marktteilnehmer als ausreichend zu qualifizieren ist
oder ob im Sinne eines Erfolgsdelikts tatsächlich verifizierbare Auswirkungen auf Seiten der Marktteilnehmer
eingetreten sein müssen. Das Bundesverwaltungsgericht stellte dabei zunächst fest, dass diese
Frage in der schweizerischen Literatur unterschiedlich beurteilt wird, in der EU-Wettbewerbspraxis die
Missbrauchsvorschrift des Art. 102 AEUV grundsätzlich im Sinne eines Gefährdungstatbestands
qualifiziert und angewendet werde (Urteil B-831/2011, SIX, E.
1198 ff.) und verwies dazu auf die nachfolgende EU-Wettbwerbspraxis (Urteil
B-831/2011,
SIX, E. 1202 ff.):
"1202. Hierbei ist massgebend, ob das fragliche Verhalten
geeignet ist, eine Beeinträchtigung des Wettbewerbs oder allenfalls auch eine Beseitigung des Wettbewerbs
herbeizuführen (vgl. EuGH, EU:C:1979:36, Hoffman-La Roche, Ziff. 127; EuG, EU:T:2009:317, Clearstream,
Ziff. 148).
1203. Die notwendige Grundlage hierfür bildet die Möglichkeit
einer nachteiligen Einwirkung auf den Wettbewerb. Ist eine nachteilige Einwirkung nicht darstellbar,
scheidet die Verwirklichung einer Wettbewerbsverfälschung aus (vgl. EuGH, 14.10.2010, C-280/08P,
Deutsche Telekom AG gg. EU-Kom, EU:C:2010:603, zit. Deutsche Telekom, Ziff. 254; EuGH, EU:C:2011:83,
zit. TeliaSonera, Ziff. 61; EuGH, 6.6.2012, C-457/10, Astra Zeneca AB u.a. gg. EU-Kom, EU:C:2012:770,
zit. AstraZeneca, Ziff. 112). Die nachteilige Einwirkung auf den Wettbewerb darf zudem auch nicht
nur rein hypothetischer Natur sein (vgl. EuGH, EU:C:2015:615, Post Danmark II, Ziff. 65).
1204. Allerdings ist es andererseits nicht erforderlich, dass auch tatsächlich
ein Erfolg oder ein bestimmter Schaden eintritt (vgl. EuGH, EU:C:2010:603, Deutsche Telekom, Ziff. 254).
Vielmehr ist es bereits ausreichend, dass eine potenziell nachteilige Einwirkung nachgewiesen wird (vgl.
EuGH, EU:C:2011:83, TeliaSonera, Ziff. 64 f.; EuGH, EU:C:2012:770, AstraZeneca, Ziff. 112; EuGH, EU:C:2012:221,
Tomra, Ziff. 79; EuGH, EU:C:2015:615, Post Danmark II, Ziff. 66, 67).
1205. Für die Feststellung einer potenziell nachteiligen Einwirkung
wurde es verschiedentlich bereits für ausreichend erachtet, auf den Zweck der Massnahme zu verweisen
(vgl. EuG, EU:T:2003:250, Michelin II, Ziff. 240; EuG, EU:T:2009:317, Clearstream, Ziff. 144). Soweit
ein Unternehmen unter Anführung von Beweisen die Möglichkeit einer nachteiligen Einwirkung
bestreitet, bedarf es allerdings einer Auseinandersetzung mit dessen Einwänden (vgl. EuGH, EU:C:2017:632,
Intel, Ziff. 138 ff.).
1206. [...]
1207. Im Ergebnis folgt aus den vorstehenden Prämissen jedenfalls,
dass für die Erfüllung des Tatbestandsmerkmals der Wettbewerbsverfälschung keine tatsächlichen
Auswirkungen nachgewiesen werden müssen (vgl. DE BRONETT, W-HdKR, § 22 Rn. 48; FUCHS/MÖSCHEL,
IM-EUWBR, Art. 102 Rn. 143 ff.; BULST, LB-EUKR, Art. 102 Rn. 131; EU-KOM, Prioritätenmitteilung,
Ziff. 19 f., massgeblich ist die Wahrscheinlichkeit einer Schädigung und nicht der Nachweis einer
tatsächlich eingetretenen Schädigung)."
12.5.7 Das
Bundesverwaltungsgericht kam zum Schluss, dass eine der EU-Wettbewerbspraxis entsprechende Qualifizierung
von Art. 7 KG im Sinne eines Gefährdungstatbestands sachgerecht ist. Denn die Wettbewerbsbehörde
muss zum Schutz des Wettbewerbs bereits zu einem Zeitpunkt einschreiten können, in dem sie Kenntnis
von einem wirtschaftlichen Verhalten erhält, mit dem eine nachteilige Einwirkung auf den Markt einhergeht.
Ansonsten würden die nachteiligen Einwirkungen auf den Wettbewerb länger andauern und damit
sowohl die Beschränkung der anderen Wettbewerber als auch die Stellung des marktbeherrschenden Unternehmens
verstärkt werden. Zudem schlägt sich eine nachteilige Einwirkung auf den Wettbewerb nicht zwingend
in einer eindeutig quantifizierbaren und durch die Wettbewerbsbehörden verifizierbaren Schädigung
der anderen Wettbewerber nieder. Denn die anderen Wettbewerbsteilnehmer reagieren auf eine unangemessene
Verhaltensweise des marktbeherrschenden Unternehmens in der Regel nicht mit einem sofortigen Marktaustritt,
sondern sie versuchen durch sonstige wirtschaftliche Massnahmen die durch die unangemessene Verhaltensweise
auftretenden Einschränkungen und den sich daraus ergebenden geschäftlichen Druck zu umgehen
oder zumindest abzufedern (Urteil B-831/2011, SIX, E. 1209 ff.).
12.5.8 Die
Beurteilung einer Wettbewerbsverfälschung erfolgt aufgrund einer Betrachtung aus der Sicht eines
objektiven Dritten. Massgebend hierfür ist allein das Handeln des marktbeherrschenden Unternehmens.
Subjektive Beweggründe einer Zuwiderhandlung auf Seiten
des marktbeherrschenden Unternehmens sind für die Beurteilung nicht massgeblich. Sie weisen allenfalls
indikative Bedeutung auf, bilden aber keine konstitutive Voraussetzung für die Feststellung einer
Wettbewerbsverfälschung (Urteil B-831/2011, SIX, E. 1194
m.w.H.).
12.5.9 Diese
allgemeinen Grundsätze gelten auch vorliegend. Das fragliche Verhalten muss somit geeignet sein,
den Wettbewerb zu beeinträchtigen.
12.5.10 Die
Vorinstanz kam zum Schluss, dass es aktuellen und potentiellen Konkurrenten durch das Vorrecht von e-mediat
unmöglich sei, die Softwarehäuser mit neu nachgefragten Daten zu beliefern. Entsprechend würden
sie vom Markt für veredelte, maschinenlesbare Daten gedrängt werden respektive Marktzutrittsschranken
aufgebaut werden. Ein Vertragsschluss betreffend Lieferung neuer Daten käme zwischen dem Softwarehaus
und HCI allein aufgrund der Alleinbezugspflicht der Softwarehäuser zustande und nicht aufgrund besserer
Vertragskonditionen. Die Klausel bewirke, dass die marktbeherrschende Stellung zukünftig zementiert
werde. Für einen Markteintritt müssten aufgrund dieser Klausel potentielle Konkurrenten einen
vollständigen Datensatz anbieten, die Spezialisierung auf neue Nachfragen oder ähnliches sei
nicht möglich. Zudem sei zur Durchsetzung des Vertrages und damit auch zur Durchsetzung der Alleinbezugspflicht
eine Konventionalstrafe vereinbart worden, die bei einem Verstoss fällig würde.
12.5.11 Weiter
erwog die Vorinstanz, das Verbot der Verwendung der Strukturen für andere Programme verschliesse
den Markt für veredelte, maschinenlesbare Daten betreffend Medikamenteninformationen für potentielle
Konkurrenzangebote. Die Implementierung von Teildatensätzen anderer Datenveredler werde untersagt.
Die Marktzutrittsschranken für potentielle Konkurrenten, beispielsweise Softwarehäuser selber,
würden erhöht, da sie einen umfassenden Datensatz anbieten und eine komplett neue Software
aufbauen müssten, um ein allfälliges Konkurrenzangebot zu implementieren. Schliesslich zeige
die systematische Anwendung der Klausel ab 2012, dass die Strategie von HCI gegen allfällige Konkurrenten
gerichtet gewesen sei. Denn in dieser Zeitperiode hätten das Urteil des Bundesverwaltungsgerichts
und die Einführung von AIPS anderen Anbietern die Möglichkeit eröffnet, auf dem Markt
Fuss zu fassen.
12.5.12 Die
Beschwerdeführerinnen rügen, die Schädigung des Wettbewerbs werde weder darlegt noch nachgewiesen.
12.5.13 Da
bereits die Möglichkeit eines Eintritts nachteiliger Einwirkungen auf den Wettbewerb als ausreichend
zu qualifizieren ist und nicht tatsächlich verifizierbare Schädigungen des Wettbewerbs eintreten
müssen, lässt sich entgegen der Ansicht der Beschwerdeführerinnen mit dem Verweis auf
eine mangelnde Darlegung und Abklärung von tatsächlich eingetretenen Umständen die Unrechtmässigkeit
einer kartellrechtlichen Verfügung wegen des Fehlens einer Wettbewerbsbehinderung nicht begründen.
12.5.14 Die
Vorinstanz erwog, ywesee und ouwerkerk sei es nicht gelungen mit ähnlichen Produkten auf dem Markt
zu kommen. Ywesee sei der Ansicht, die Klauseln hätten ihr massiv geschadet.
12.5.15 Die
Beschwerdeführerinnen erachten den Hinweis der Vorinstanz auf die Aussagen von ywesee und ouwerkerk
dagegen als nicht überzeugend. Ywesee behaupte zwar, die Softwarehäuser hätten sie in
Bezug auf die Apotheken ausgebremst. Es sei jedoch nicht belegt, dass die fraglichen Klauseln dafür
verantwortlich gewesen seien. Auch die Behauptung von ywesee, T._______ würde aufgrund eines Knebelvertrages
mit HCI nicht mit ihr zusammenarbeiten, sei unzutreffend. Gemäss Beilage 1 der Anhörung von
M._______ habe sich T._______ aus anderen Gründen für eine Zusammenarbeit mit HCI entschlossen.
Ouwerkerk mache für den mangelnden Erfolg technische Gründe geltend und bestätige, dass
für die Leistungserbringerinnen und -erbringer die Qualität der Daten sehr wichtig sei. Die
D._______ habe die Klausel A selbst als bedeutungslos bezeichnet. Es habe in der untersuchten Zeitperiode
in qualitativer Hinsicht keine vergleichbare Datenbank in der Schweiz gegeben. Deshalb sei davon auszugehen,
dass der Erfolg von HCI auf der Qualität ihrer Leistungen und nicht auf den fraglichen Klauseln
beruhe. Jedenfalls bestehe eine glaubwürdige Alternativerklärung, aus welchem Grund ywesee
und ouwerkerk nicht mit dem gewünschten Erfolg in den Markt eingetreten seien.
12.5.16 Es
ist davon auszugehen, dass ein wesentlicher Grund, weshalb es ywesee und ouwerkerk nicht gelungen ist,
in den Markt oder stärker in den Markt einzutreten, am geringeren Datenumfang und der möglicherweise
geringeren Qualität ihres Angebotes lag (vgl. auch E. 12.4.39).
Dies lässt bzw. liess jedoch einen Markteintritt nicht vollständig verhindern, wie der kleine
Marktanteil von ywesee im Ärztesektor zeigt. Es erscheint durchaus naheliegend, dass neben den Angebotsunterschieden
auch die Klauseln A und B zu einer Behinderung von Markteintritten von Konkurrenten führten. Letztlich
kann diese Frage jedoch offengelassen werden. Denn wie erwähnt genügt im Sinne eines Gefährdungsdelikts
bereits die Möglichkeit eines Eintritts nachteiliger Einwirkungen für die Marktteilnehmer.
Tatsächlich verifizierbare Schädigungen des Wettbewerbs durch die Klauseln A und B müssen
nicht eingetreten sein.
12.5.17 Aus
diesem Grund vermag auch das Vorbringen der Beschwerdeführerinnen, sie seien bereit gewesen,
Kooperationen mit anderen Datenveredlern zuzulassen, nicht zu überzeugen. Bereits oben wurde festgehalten,
dass die Klauseln aufgrund der Offenlegungspflicht selbst in Fällen, wo HCI eine Zusammenarbeit
mit einer Drittfirma erlaubt haben will, nicht per se unproblematisch erscheinen. Die Klauseln waren
auch dann geeignet, Marktinformationen und Einzelheiten über die Konkurrenzangebote zu sammeln,
um Preis- bzw. Angebotsanpassung vorzunehmen, was die Konkurrenten darin behindern kann, Marktanteile
zu gewinnen. Hinzukommt, dass es vom Willen und der Entscheidung von HCI abhängig war, ob Kooperationen
mit Drittanbietern zugelassen wurden oder nicht.
12.5.18 Die
Klauseln A und B waren offensichtlich geeignet, den Markt für veredelte, maschinenlesbare Daten
betreffend Medikamenteninformationen für potentielle Konkurrenzangebote zu verschliessen. Die Klauseln
waren ebenso geeignet, zu verhindern, dass potentielle Konkurrenten nur Teildatensätze anbieten
konnten und dass die Nachfragerinnen und Nachfrager unter den Angeboten verschiedener Wettbewerber das
günstigste (für verschiedene Teildatensätze) auswählen und ohne spürbaren wirtschaftlichen
Nachteil wechseln konnten.
12.5.19 Weiter
bringen die Beschwerdeführerinnen vor, die Klauseln seien nicht systematisch eingeführt worden.
Auch wenn die Klausel B für eine gewisse Zeitperiode in der Vertragsvorlage enthalten gewesen sei,
sei damit weder die Verfolgung einer systematischen Abschottungsstrategie noch eine Verdrängungswirkung
nachgewiesen.
12.5.20 Die
Beurteilung einer Wettbewerbsbeeinträchtigung erfolgt aus der Sicht eines objektiven Dritten. Subjektive
Beweggründe einer Zuwiderhandlung auf Seiten des marktbeherrschenden Unternehmens sind nicht massgeblich
(s. oben E. 12.5.8).
Das Verhalten eines Unternehmens in beherrschender Stellung kann auch ohne jedes Verschulden als missbräuchlich
betrachtet werden. Ob das fragliche Unternehmen wettbewerbsfeindliche
Ziele verfolgt hat, ist für die rechtliche Bewertung der Tatsachen unerheblich. Der Nachweis, dass
das fragliche Unternehmen wettbewerbsfeindliche Ziele verfolgt hat, kann die Feststellung des Missbrauchs
einer beherrschenden Stellung zwar untermauern, er ist aber keine Bedingung für diese Feststellung
(vgl. Urteil EuG EU:T:2009:317, Clearstream, Rn. 141 f.).
Entsprechend ist es nicht erforderlich, dass nachgewiesen wird, dass HCI mit den Klauseln A und B eine
systematische Abschottungsstrategie verfolgt hat. In diesem Zusammenhang ebenso unbeachtlich ist die
Rüge der Beschwerdeführerinnen, die Vorinstanz habe sich nicht mit ihren Argumenten betreffend
Sinn und Zweck der beanstandeten Klauseln auseinandergesetzt.
12.6 Sachliche
Rechtfertigungsgründe
12.6.1 Rechtfertigung
des Verhaltens ist aufgrund sachlicher Gründe zulässig, auch wenn im Gegensatz zu Art. 5 Art.
7 keine ausdrückliche textliche Regelung kennt. Sachliche Gründe sind objektive Gründe.
Dies bedeutet, dass es sich beim Verhalten des marktbeherrschenden Unternehmens um ein solches handeln
muss, das sich als fairer Leistungswettbewerb beschreiben lässt (Urteil 2C_985/2015, ADSL
II, E. 5.9).
12.6.2 Die
missbräuchliche Einschränkung der Erzeugung, des Absatzes oder der technischen Entwicklung
kann durch legitimate business reasons gerechtfertigt werden. Die inkriminierte Praktik kann ein objektiv
notwendiges Verhalten sein. Die in Art. 7 Abs. 2 lit. e KG genannten Verhaltensweisen können insbesondere
sachlich gerechtfertigt sein: (1) aus Sicherheits- und Umweltschutzgründen; (2) durch Kapazitätsengpässe,
die eine Aufrechterhaltung des bisherigen Produktions- oder Vertriebsumfangs verunmöglichen; (2)
als Reaktion auf eine Nachfrageänderung; (4) durch entsprechende Rationaliserungsprozesse; (5) wenn
die Entstehungskosten eines Produkts nicht durch den zu erzielenden Gewinn gedeckt werden können
und die Einschränkung somit auf Kosteneinsparungen beruht (Jacqueline
Sievers, Legitimate business reasons beim Missbrauch einer marktbeherrschenden Stellung gemäss
Art 7 KG, Diss. 2014, S. 190 ff; Stäuble/Schranker,
DIKE-KG, Art 7 N 476). Als objektive Gründe für eine Alleinbezugsklausel werden beispielsweise
die Übertragung von sensiblem Know-How oder eine allfällige Gegenleistung für die Exklusivität
(z.B. Stabilität der Bezugsquelle für den Käufer, damit dieser wiederum seinen eigenen
Kunden stets Qualität, Quantität oder gleichbleibende Preise garantieren kann) erwähnt
(Rz. 68 ff. der Verfügung der Vorinstanz vom 1. Dezember 2003 in Sachen TicketCorner
[veröffentlicht in: RPW 2004/3 S. 778 ff., 798 ff.]; Amstutz/Carron,
BSK-KG 2010, Art. 7 N 464, in 2. Aufl. 2021 nicht mehr diskutiert). Ausserdem darf das marktbeherrschende
Unternehmen, das spezifische Investitionen tätigen musste, um einen Klienten zu beliefern, legitimerweise
fordern, dass der betroffene Klient wenigstens eine gewisse Menge an gelieferter Ware bezieht, so dass
die getätigten Investitionen amortisiert werden können (Amstutz/Carron,
BSK-KG 2010, Art. 7 N 464, in 2. Aufl. 2021 nicht mehr diskutiert).
12.6.3 Eine
Rechtfertigung durch legitimate business reasons kommt allerdings nur dann in Betracht, wenn der Grundsatz
der Verhältnismässigkeit eingehalten ist. Dies setzt voraus, dass die vom marktbeherrschenden
Unternehmen ausgeübte Verhaltensweise geeignet ist, das anvisierte Ziel, d.h. den sachlichen Grund
zu erreichen, und dem marktbeherrschenden Unternehmen keine alternativen Verhaltensweisen zur Verfügung
stehen, die sich weniger wettbewerbsverfälschend auswirken (Gebot der Unerlässlichkeit; Amstutz/Carron,
BSK-KG, Art. 7 N 180; Stäuble/Schraner, DIKE-KG, Art.
7 N 130 f.; Weber/Volz, a.a.O., Rz. 2.567; vgl. Urteil
2C_985/2015, ADSL II, E. 5.9).
12.6.4 Die
Beschwerdeführerinnen machten sowohl vor der Vorinstanz als auch im Beschwerdeverfahren geltend,
HCI habe insbesondere aufgrund folgender voneinander unabhängige und für sich alleine ausreichende
sachliche Gründe die Klauseln in die Verträge aufgenommen:
- HCI
verpflichte sich in den Lizenzverträgen mit den Leistungserbringerinnen und -erbringern, die lizenzierten
Arzneimitteldaten vertragsgemäss zugänglich zu machen. Wegen der indirekten Übermittlung
der Daten über die Softwarehäuser müsse HCI in den Verträgen mit den Softwarehäusern
dafür sorgen, dass die Übertragung integral und unter Wahrung der Datenintegrität erfolge.
Die Klauseln hätten sichergestellt, dass eine allfällige Beeinträchtigung der Datenintegrität
durch die Verwendung von Drittdaten nicht ohne Rücksprache mit HCI erfolgen könne. Entsprechend
hätten die Klauseln zur Verhinderung von Leistungsstörungen in den Lizenzverträgen zwischen
HCI und den Leistungserbringerinnen und -erbringern gedient.
- Eine
Vermischung der Daten durch die Softwarehäuser führe für HCI zu Haftungs- und Reputationsrisiken,
da für die Leistungserbringerinnen und -erbringer unter Umständen nicht ersichtlich wäre,
welche Daten von HCI und welche Daten von Drittanbietern stammen würden. Mit dem Zustimmungserfordernis
habe HCI darauf vertrauen können, dass die Softwarehäuser die entsprechenden Modalitäten
zuerst mit HCI hätten klären müssen, bevor Drittdaten an die Kunden von HCI geliefert
worden wären. So hätten Haftungs- und Reputationsrisiken verhindert werden können.
12.6.5 Die
Vorinstanz prüfte die Frage, ob die Softwarehäuser für das Funktionieren der Software
auf Daten aus einer einheitlichen Quelle, d.h. von einem Datenveredler, angewiesen seien. Die Befragung
der Softwarehäuser habe ergeben, dass technisch der Einbezug anderer Daten oder auch der Einbezug
unterschiedlicher Datenstämme für Medikamenteninformationen und Daten von Non-Pharma Produkten
in die Software möglich wäre. Der Aufwand für eine solche Bezugsänderung sei jedoch
sehr unterschiedlich eingeschätzt worden. Zudem hätten viele Softwarehäuser den Umfang
und die Qualität der Daten von alternativen Anbieter in Frage gestellt. Auch das Gespräch mit
einem grösseren Softwarehaus habe bestätigt, dass technisch eine Integration von Daten aus
verschiedenen Quellen in die Software möglich wäre.
12.6.6 Weiter
erwog die Vorinstanz, die Frage des Umfanges und der Qualität der Daten sei unabhängig von
der Frage der technischen Voraussetzungen an die Daten. Qualität und Umfang seien gewöhnliche
Wettbewerbsvariablen und im Wettbewerb seien durchaus qualitativ oder umfangmässig verschiedene
Angebote denkbar.
12.6.7 Die
Beschwerdeführerinnen weisen zutreffend daraufhin, dass die von der Vorinstanz geprüfte Frage
der technischen Möglichkeit der Integration von Daten aus verschiedenen Quellen nur einen Teil der
vorgebrachten Rechtfertigungsgründe abdeckt. Die Vorinstanz hätte auch auf die anderen von
den Beschwerdeführerinnen vorgebrachten Rechtfertigungsgründe eingehen müssen. Für
die von den Beschwerdeführerinnen vorgebrachten Rechtfertigungsgründe der Verhinderung von
Leistungsstörungen und von Haftungs- und Reputationsrisiken ergibt sich jedoch, dass mildere Mittel
zur Verfügung standen. Mit der Vorinstanz und wie die geänderten Vertragsbestimmungen von HCI
zeigen, ist davon auszugehen, dass diese beiden Ziele auch mit einer Vertragsbestimmung zu erreichen
gewesen wären, wonach Daten von Dritten und Veränderungen der Datenquelle als solche sichtbar
hätten gekennzeichnet werden müssen.
12.6.8 Vor
welchem Hintergrund im Laufe der Untersuchung die Vertragsklausel B durch eine Kennzeichnungspflicht
ersetzt wurde, ist in diesem Zusammenhang unerheblich. Insofern ist das Vorbringen der Beschwerdeführerinnen,
sie hätten die Klausel B im Mustervertrag ausschliesslich vor dem Hintergrund, dass das Sekretariat
während des Untersuchungsverfahrens die These vertreten habe, die Klausel B könnte eine missbräuchliche
Verhaltensweise darstellen, durch eine andere Klausel ersetzt, nicht stichhaltig.
12.6.9 Soweit
sich die Beschwerdeführerinnen auf die Lehrmeinung von David/Jacobs
berufen, wonach ein Verhalten erst unzulässig sei, wenn es offensichtlich missbräuchlich und
damit meist geradezu willkürlich sei und nicht bereits dann, wenn ein anderes Verhalten sachgerechter,
sinnvoller
oder besser gewesen wäre (David/Jacobs,
a.a.O., Rz. 755), ist festzuhalten, dass dieser Auffassung nicht gefolgt werden kann. Zum einen widerspricht
sie der unter E. 12.6.3
dargestellten herrschenden Lehre und Praxis im Zusammenhang mit dem Verhältnismässigkeitsprinzip.
Alles, was über das zur Interessenwahrung Notwendige hinausgeht, fällt nicht mehr in den Anwendungsbereich
des Rechtfertigungsgrundes (Sievers, a.a.O., S. 88). Stehen
alternative Strategien zur Verfügung, die wie das vom Marktbeherrscher gewählte Verhalten die
angestrebten Ziele hätten erreichen können, sich aber weniger wettbewerbsverfälschend
auswirken, kann nicht davon gesprochen werden, dass das marktbeherrschende Unternehmen nur zur Verwirklichung
höherwertiger externer Interessen, zum Schutz seiner geschäftlichen Belange oder zur Erzeugung
ökonomischer Effizienzen gehandelt hat (Amstutz/Carron,
BSK-KG, Art. 7 N 180). Zwar sind nicht jegliche hypothetische oder theoretische Alternativen zu erwägen.
Wenn wie im vorliegenden Fall ein anderes naheliegendes Verhalten, sachgerechter und weniger wettbewerbsverfälschend
ist um das anvisierte Ziel zu erreichen, scheidet eine Rechtfertigung durch legitimate business reasons
aber per se aus.
12.6.10 Zudem
ist eine solche Auffassung auch nicht mit dem Grundgedanken zu vereinen, wonach einem marktbeherrschenden
Unternehmen eine besondere Verantwortung zukommt, durch sein Verhalten am Markt einen wirksamen und unverfälschten
Wettbewerb nicht (weiter) zu beeinträchtigen. Daher hat es auf die Anwendung von Praktiken zu verzichten,
die nicht den Mitteln eines Leistungswettbewerbs entsprechen, und die zu einer Verdrängung anderer
Wettbewerber führen können (s. oben E. 11.4).
12.6.11 Da
die Verhältnismässigkeit nicht gewahrt ist, erübrigt sich eine weitere Prüfung dieser
beiden vorgebrachten Rechtfertigungsgründe.
12.6.12 Weiter
bringen die Beschwerdeführerinnen vor, es liege mit der Verhinderung von UWG-Verletzungen durch
Anbieter von Drittdaten ein weiterer sachlicher Rechtfertigungsgrund vor. Die Datenbankstruktur sei von
HCI selbständig entwickelt worden und aufgrund der Möglichkeit der verschiedenen Verknüpfungen
von Produkten äusserst komplex. Bei unveränderter Übernahme dieser Strukturierung durch
ein Konkurrenzunternehmen würde das kommerzielle Anbieten der Arzneimittelinformationen in der von
HCI entwickelten XML-Datenbankstruktur gegen Art. 5 Bst. c UWG verstossen. Klausel B habe es HCI
ermöglicht, allfällige Verstösse gegen das UWG frühzeitig zu erkennen bzw. darauf
Einfluss zu nehmen, dass die Datenbankstruktur nicht tel quel übernommen werde.
12.6.13 Die
Vorinstanz weist daraufhin, dass es sich hierbei um ein neues Argument handle. Mit den zivil- und/oder
strafrechtlichen Mitteln würden zum Schutz gegen einen Verstoss gegen das UWG mildere Mittel zur
Verfügung stehen. Da dieser Grund erst in der Beschwerde erwähnt werde, scheine er ferner auch
nicht dem ursprünglichen Zweck der Klausel zu entsprechen. Entsprechend falle dieses Argument als
Rechtfertigung für den Verstoss gegen das Kartellgesetz ausser Betracht.
12.6.14 Gemäss
den Beschwerdeführerinnen hindern die zivilrechtliche Klagemöglichkeiten und Straftatbestände
im UWG die Unternehmen nicht, zusätzliche Vorkehren zu treffen, um Rechtsverletzungen zu verhindern.
Präventivmassnamen seien wirkungsvoller, als nachträglich zeit- und kostenintensive Prozesse
zu führen. Im Übrigen seien die Befürchtungen betreffend UWG-Verletzungen nicht nachgeschoben,
bereits 2012 hätten sie sich mit Schutzmöglichkeiten vor UWG-Verletzungen befasst, was das
Memorandum "Schutzstrategie Index-Produkte" vom 30. Mai 2012 belege. Zudem würde
die Anfertigung einer Kopie der Strukturen der INDEX-Produkte sowie das Erstellen eines Konkurrenzprodukts
mit derselben XML-Schnittstelle auch das Urheberrecht der Beschwerdeführerin 2 verletzen.
12.6.15 Für
die Vorinstanz zeigt das Memorandum "Schutzstrategie Index-Produkte" jedoch, dass die Beschwerdeführerinnen
unter dem Vorwand des Schutzes der Strukturen die Daten monopolisieren würden. An den Daten kämen
ihnen eben keine exklusiven Rechte zu. Für eine funktionierende Datenübertragung müssten
die Softwarehäuser über Schnittstellen verfügen. Sobald sie die Daten über die Schnittstelle
bezogen und die darin enthaltenen Daten in ihre eigene softwarespezifische Struktur überführt
hätten, habe sich der Schutz erschöpft, da die ursprüngliche Struktur des XML-Dokuments
für die weitere Datennutzung nicht mehr benötigt werde. Aus welcher Quelle Daten stammen würden,
könne ausserdem von den Softwarehäusern abgebildet werden. Die von den Beschwerdeführerinnen
verwendeten Klauseln würden somit, sicher nicht das mildeste Mittel zur Erreichung der vorgegebenen
Zwecke darstellen.
12.6.16 Die
Beschwerdeführerinnen halten diese Ausführungen der Vorinstanz zur Erschöpfung des Schutzes
schliesslich aus immaterialgüterrechtlicher Perspektive und aus UWG-Sicht als nicht nachvollziehbar.
Auch marktbeherrschende Unternehmen dürften sich auf das UWG und die Immaterialgüterrechte
berufen. Es sei zwar möglich, dass marktbeherrschende Unternehmen einem Kontrahierungszwang unterliegen
und Zwangslizenzen gewähren müssten. Aber auch bei dieser Konstellation sei der Schutz der
Rechte nicht vollständig aufgehoben.
12.6.17 Vorliegend
ist unbestritten, dass an den Daten kein Schutz durch Immaterialgüterrechte besteht (s. oben E.
2.2.2.4).
Einzig die XML-Strukturen der INDEX-Produkte geniessen urheberrechtlichen Schutz. Darunter fallen das
Kopieren der XML-Strukturen und das Anbieten eines Konkurrenzproduktes mit derselben XML-Schnittstelle.
12.6.18 Im
Wettbewerbsrecht hat sich die Ansicht durchgesetzt, dass Nachahmungen grundsätzlich zulässig
sein müssen, weil sie die Verbreitung von Innovationen fördern und zu sinkenden Preisen führen.
Diese Ansicht findet Ausdruck im heute allgemein anerkannten Grundsatz der Nachahmungsfreiheit. Danach
steht es jedermann frei, die Erzeugnisse eines Konkurrenten nachzuahmen und ebenfalls anzubieten, sofern
kein Schutz durch Immaterialgüterrechte besteht (Florent Thouvenin,
Art. 5 lit. c UWG - reloaded, sic! 2018, S. 595 ff., S. 595 f., m.w.H.).
12.6.19 Eine
Nachahmung liegt vor, wenn ein Erzeugnis nach einer bestimmten Vorlage mehr oder minder detailgetreu
nachgebildet wird, ohne dass diese Vorlage in das Reproduktionsverfahren einbezogen worden ist. Die Nachahmung
basiert auf einem gedanklichen Vorgang, bei dem das nachzuahmende Erzeugnis vom Nachahmer analysiert
wird, um mithilfe der so gewonnen Erkenntnisse ein identisches oder ähnliches Erzeugnis zu schaffen.
Dadurch grenzt sich die Nachahmung von der unmittelbaren Übernahme ab, bei welcher das Erzeugnis
eines Dritten gegenständlich ins Reproduktionsverfahren einbezogen wird. Mit der Übernahme
befasst sich Art. 5 lit. c UWG (Florent Thouvenin, a.a.O.,
S. 596, m.w.H.). Der Tatbestand besagt, dass unlauter handelt, wer das marktreife Arbeitsergebnis eines
anderen ohne angemessenen eigenen Aufwand durch technisches Reproduktionsverfahren als solches übernimmt
und verwertet. Art. 5 lit. c UWG ist aufgrund der oben erwähnten Nachahmungsfreiheit sehr eng
formuliert (Simone Brauchbar Birkhäuser, in: Peter
Jung/Philippe Spitz, Bundesgesetz gegen den unlauteren Wettbewerb [UWG], 2. Aufl. 2016, Art. 5 N
37). Einschränkend wirken insbesondere die Voraussetzung des technischen Reproduktionsverfahrens
und die restriktive Auslegung des Tatbestandsmerkmals des angemessenen eigenen Aufwands (vgl. Florent
Thouvenin, a.a.O., S. 597 und 602 m.w.H.).
12.6.20 Die
Klausel B erfasst nicht nur das Kopieren der XML-Strukturen der HCI und das Anbieten eines Konkurrenzproduktes
mit derselben XML-Schnittstelle und auch nicht nur die Übernahme der Daten ohne angemessenen eigenen
Aufwand durch technisches Reproduktionsverfahren, sondern sie erfasst eben auch durch das UWG nicht geschützte
Nachahmungen. Darüber hinaus betrifft sie sogar Daten, die HCI selber gar nicht anbot. Angesichts
dessen und unter besonderer Berücksichtigung des Grundsatzes der Nachahmungsfreiheit erscheint die
Klausel B bzw. eine Rechtfertigung durch legitimate bussiness reasons wegen Verhinderung von UWG-Verletzungen
nicht verhältnismässig. Die Vorinstanz hat zutreffend darauf hingewiesen, dass mit den zivil-
und/oder strafrechtlichen Mitteln des UWG (Art. 9 und 23 UWG) mildere Mittel gegen einen Verstoss gegen
das UWG zur Verfügung stehen. Soweit die Beschwerdeführerinnen diesbezüglich vorbringen,
Präventivmassnahmen seien wirkungsvoller um Rechtsverletzungen zu verhindern, ist festzuhalten,
dass es ihnen unbenommen gewesen wäre, zusätzlich eine engere Vertragsbestimmung zu verwenden,
die effektiv nur auf die möglichen Urheberrechts- und UWG-Verletzungen abgezielt hätte. Die
vorliegende Klausel geht jedoch weit darüber hinaus. Eine Rechtfertigung durch legitimate bussiness
reasons wegen Verhinderung von UWG-Verletzungen kommt somit aufgrund der fehlenden Einhaltung des Grundsatzes
der Verhältnismässigkeit nicht in Betracht.
12.7 Fazit
Als Ergebnis der Prüfung
im Beschwerdeverfahren ist festzustellen, dass die Verwendung der Klauseln A und B durch HCI in den Verträgen
mit den Softwarehäusern ein wettbewerbswidriges Verhalten in der Missbrauchsform einer Einschränkung
des Absatzes gemäss Art. 7 Abs. 1 i.V.m. Abs. 2 Bst. e KG darstellt.
13. Koppelung
von Leistungen i.S.v. Art. 7 Abs. 2 Bst. f KG
13.1 Sachverhalt
13.1.1 Documed
bzw. HCI bot gemäss den abgeschlossenen Verträgen und dem Leistungskatalog für das Jahr
2013 den Zulassungsinhaberinnen mit dem Basismodul D1 die Publikation der Fach- und Patienteninformationen
im Compendium (auf www.compendium.ch, in der entsprechenden App sowie im E-Book) und mit dem Basismodul
E1 die Aufnahme der Medikamenteninformationen in die INDEX-Produkte (sowie Clinical Decision Support
bei RX-Produkten) an. Beide Dienstleistungen konnten nur mit den Basisdienstleistungen der Module D1+E1
bezogen werden, welche insbesondere redaktionelle und technische Qualitätssicherungs- und Aufbereitungsarbeiten
enthielten (sowie das Auftragsmanagement via compendiumPORTAL2).
13.1.2 Der
Upload auf AIPS war gemäss Leistungskatalog nicht in den Modulen enthalten. Documed bzw. HCI nahm
jedoch bei entsprechender Beauftragung durch den Kunden gemäss Ziffer 2 der "Vereinbarung zur
Publikation von Informationen im Arzneimittel-Kompendium der Schweiz® und in den INDEX-Produkten"
auch die Publikation der Kundentexte in AIPS gemäss den Swissmedic-Anforderungen vor. Hierfür
wurde den Zulassungsinhaberinnen kein zusätzliches Entgelt verrechnet.
13.1.3 Die
Vorinstanz kam in der angefochtenen Verfügung zum Schluss, Galenica habe mittels HCI durch dieses
Modulbundling den Tatbestand der an den Abschluss von Verträgen gekoppelten Bedingung i.S.v. Art.
7 Abs. 1 i.V.m. Abs. 2 Bst. f KG erfüllt.
13.2 Grundlagen
13.2.1 Ein
Koppelungsgeschäft gemäss Art. 7 Abs. 2 Bst. f KG liegt vor, wenn an den Abschluss von Verträgen
die Bedingung gekoppelt wird, dass ein Geschäftspartner zusätzliche Leistungen in Form von
Waren oder Dienstleistungen anzunehmen oder zu erbringen hat, die keinen sachlichen Zusammenhang zum
Grundgeschäft aufweisen (Urteil 2C_113/2017, Hallenstadion,
E. 6.2.1; Stäuble/Schraner, DIKE-KG, Art. 7 N 489;
Zäch, a.a.O., Rz. 700; Weber/Volz,
a.a.O., N 2.752). Der Anbieter des koppelnden Gutes macht dessen Lieferung abhängig von der Abnahme
einer zusätzlichen Leistung. Der Abnehmer ist in der Wahl der zusätzlichen Leistung nicht frei,
hat also keine andere Wahl, als auch das gekoppelte Gut zu erwerben (Urteil 2C_113/2017, Hallenstadion,
E. 6.2.2).
13.2.2 Es
gibt verschiedene Koppelungstechniken, wie die Bündelung ("pure bundling"), das Verbundgeschäft
("tying") und das Anreizgeschäft ("mixed bundling"),
welche durch direkte oder indirekte Koppelung erreicht wird. Die Bündelung umfasst den ausschliesslich
gemeinsamen Absatz von Haupt- und Zusatzprodukt. Die beiden Güter werden stets nur in einem Koppelungsverhältnis
angeboten. Das Verbundgeschäft umfasst den ausschliesslichen Absatz des Hauptprodukts zusammen mit
dem Zusatzprodukt aufgrund einer einseitigen Kombination des Hauptprodukts mit dem Zusatzprodukt, weshalb
das Zusatzprodukt auch alleine verfügbar bleibt. Das Anreizgeschäft umfasst die Sachverhalte,
bei denen eine unabhängige Abnahme von Haupt- und Zusatzprodukt aufgrund einer bloss fakultativen
Kombination zwar theoretisch möglich bleibt, die gleichzeitige Nachfrage aufgrund spezifischer ökonomischer
Anreize - wie die Ausgestaltung von Gesamtpreisen oder die Gewährung von Rabatten und sonstigen
Vergünstigungen bei Abnahme von Haupt- und Zusatzprodukt - aber bei realistischer Betrachtung
ganz offensichtlich vorzuziehen ist (Urteile 2C_113/2017, Hallenstadion,
E. 6.2.2; B-831/2011, SIX, E. 1266;
B-3618/2013,
Hallenstadion, E. 250 m.w.H; Amstutz/Carron,
BSK-KG, Art. 7 N 683 ff.; Stäuble/Schraner, DIKE-KG,
Art. 7 N 497; Weber/Volz, a.a.O., Rz. 2.763). Hinsichtlich
Koppelungsgrund wird zwischen vertraglicher und faktischer Koppelung unterschieden (Urteil B-831/2011,
SIX, E. 1267).
13.2.3 Koppelungsgeschäfte
sind kartellrechtlich relevant, wenn daraus eine Wettbewerbsbeschränkung resultiert. Das ist insbesondere
der Fall, wenn das marktbeherrschende Unternehmen seine Stellung ausnutzt, um seine Lieferanten oder
Abnehmer zur Belieferung bzw. Abnahme eines Gutes zu bewegen, das sie entweder gar nicht oder zumindest
nicht zu den vom marktbeherrschenden Unternehmen vorgegebenen Geschäftsbedingungen absetzen bzw.
erwerben möchten, oder um seine Marktmacht auf den Markt des gekoppelten Gutes, auf dem es bislang
nicht marktbeherrschend ist, zu übertragen (Urteil 2C_113/2017, Hallenstadion,
E. 6.2.2; Stäuble/Schraner, DIKE-KG, Art. 7 N 502;
Clerc/Këllezi, CR-Concurrence, Art. 7 II N 279
f.).
13.2.4 Der
Absatz des Zusatzprodukts beruht in solchen Fällen nicht auf dessen eigenen Leistungsfaktoren, sondern
knüpft an den von den jeweiligen Nachfragern bzw. Anbietern angestrebten Absatz des Hauptprodukts
an. Die Wettbewerbsverfälschung kann somit bestehen in:
(i)
einer Benachteiligung der Marktgegenseite des marktbeherrschenden Unternehmens durch die Aufhebung
seiner Handlungsfreiheit infolge der Notwendigkeit zur Abnahme oder Leistung eines Produkts, welches
gar nicht oder jedenfalls nicht unter Anwendung der jeweiligen Modalitäten abgenommen oder geleistet
worden wäre; und/oder
(ii)
(ii) einer Behinderung von Konkurrenten durch deren Verdrängung, indem diesen die Nachfrager
bzw. Anbieter auf dem Markt des Zusatzprodukts entzogen werden.
Durch eine Koppelung kann die Stellung des marktbeherrschenden Unternehmens auf
dem Markt des Hauptprodukts
oder auf dem Markt des Zusatzprodukts oder auch auf beiden Märkten gestützt oder verstärkt
werden (Urteile B-831/2011, SIX, E. 1265; B-3618/2013, Hallenstadion,
E. 249; Clerc/Këllezi, CR-Concurrence, Art. 7
II N 263 f.; Stäuble/Schraner, DIKE-KG, Art. 7 N 491;
Weber/Volz, a.a.O., Rz. 2.753).
13.2.5 Der
Tatbestand der unzulässigen Koppelung von Leistungen i.S.v. Art. 7 Abs. 1 i.V.m. Abs. 2 Bst. f KG
wird als erfüllt betrachtet, wenn kumulativ folgende Merkmale vorliegen (Urteile 2C_113/2017, Hallenstadion,
E. 6.2.1; B-831/2011, SIX, E. 1268; B-3618/2013, Hallenstadion,
E. 253):
- (i)
marktbeherrschende Stellung eines Unternehmens auf dem Markt des Hauptprodukts;
- (ii)
Vorliegen separater Produkte, d.h. das koppelnde und das gekoppelte Gut sind getrennte Güter;
- (iii)
Kombination bzw. Verknüpfung von Haupt- und Zusatzprodukt durch das marktbeherrschende Unternehmen;
- (iv)
wettbewerbsbeschränkender Effekt;
- (v)
Fehlen von Rechtfertigungsgründen.
Im Urteil B-831/2011 i.S. SIX
wird als zusätzliches Merkmal das Vorliegen von "Marktteilnehmer als Vertragspartner"
genannt (Urteil B-831/2011, SIX, E. 1268).
13.3 Marktbeherrschende
Stellung
13.3.1 Für
die Koppelung muss dem ausführenden Unternehmen eine marktbeherrschende Stellung auf dem Markt des
Hauptprodukts zukommen. Eine besondere Stellung auf dem Markt des Zusatzprodukts ist nicht erforderlich
(Urteile B-831/2011, SIX, E. 1294; B-3618/2013, Hallenstadion,
E. 254; Amstutz/Carron, BSK-KG, Art. 7 N 719; Stäuble/Schraner,
DIKE-KG, Art. 7 N 504; Weber/Volz, a.a.O., Rz. 2.754).
13.3.2 Vorliegend
war die ehemalige Galenica-Gruppe mittels HCI auf dem Markt für die Aufnahme und den Erhalt in elektronischen
Datensätzen betreffend Medikamenteninformationen in der Schweiz marktbeherrschend (s. oben E. 9.3).
13.4 Vertragspartner
13.4.1 Als
Vertragspartner gelten diejenigen Marktteilnehmer, die mit dem marktbeherrschenden Unternehmen eine rechtlich
verbindliche Vereinbarung über die Annahme oder Erbringung des Hauptproduktes oder eines Zusatzproduktes
abschliessen bzw. abschliessen wollen (Urteil
B-831/2011, SIX,
E. 1303). Dabei werden aufgrund der ausdrücklichen Formulierung "annehmen oder erbringen"
die Vertragspartner sowohl auf der Nachfrageseite als auch auf der Angebotsseite erfasst (Botschaft KG,
BBl 1995 I 468, 576; Clerc/Këllezi, CR-Concurrence,
Art. 7 II N 271; Stäuble/Schraner, DIKE-KG, Art. 7
N 490; Weber/Volz, a.a.O., Rz. 2.752). Eine Koppelung
kann daher sowohl gegenüber Lieferanten als auch gegenüber Kunden erfolgen (Urteil B-831/2011,
SIX, E. 1304).
13.4.2 Vorliegend
bilden die Zulassungsinhaberinnen für die Aufnahme und den Erhalt in elektronischen Datensätzen
betreffend Medikamenteninformationen die potentiellen Vertragspartnerinnen der HCI.
13.5 Vorliegen
separater Produkte
13.5.1 Ein
Koppelungsgeschäft ist nur unzulässig, wenn es zwei getrennte Güter kombiniert. Von getrennten
Gütern spricht man dann, wenn die zusätzliche Leistung in keinem sachlichen Zusammenhang zur
Hauptleistung steht (Urteil 2C_113/2017, Hallenstadion, E. 6.2.2).
Das Zusatzprodukt muss ein vom Hauptprodukt unterscheidbares Produkt darstellen, das auf einem eigenen
Markt gehandelt wird oder zumindest gehandelt werden könnte und aus Sicht der Marktgegenseite Haupt-
und Zusatzprodukt auch tatsächlich unabhängig voneinander nachgefragt bzw. angeboten werden
(würden) (Urteile B-831/2011, SIX, E. 1312; B-3618/2013,
Hallenstadion, E. 255; Amstutz/Carron,
BSK-KG, Art. 7 N 721 ff.; Clerc/Këllezi, CR-Concurrence,
Art. 7 II N 276; Stäuble/Schraner, DIKE-KG, Art. 7
N 494 f.; Weber/Volz, a.a.O., Rz. 2.758).
13.5.2 Massgebend
für die Beurteilung im Einzelfall ist regelmässig eine marktorientierte Betrachtung (Urteile
B-831/2011, SIX, E. 1313;
B-3618/2013, Hallenstadion, E. 255;
Amstutz/Carron, BSK-KG, Art. 7 N 725; Weber/Volz,
a.a.O., Rz. 2.758), bei der eine individuell-typisierte Abgrenzung vorzunehmen ist. Soweit die Beurteilung
weitgehend auf Prognosen beruht, kann ausnahmsweise auch eine auswirkungsbasierte Beurteilung sachgerecht
sein (Urteile B-831/2011, SIX, E. 1313;
B-3618/2013,
Hallenstadion, E. 255; vgl. Entscheidung 2007/53/EG der der Kommission
vom 24. März 2004 betreffend ein Verfahren nach Artikel 82 EG-Vertrag und Artikel 54 EWR-Abkommen,
Comp/C-3/37.792 Microsoft Corp., ABl. 2004 L 32/23 Rn. 946 und
968; Urteil des EuG vom 17. September 2007 T-201/04 Microsoft/Kommission,
Slg. 2007 II-03601 Rn. 1089). Für diese Beurteilung ist weder auf besondere Sachverhaltskonstellationen
einer Verwendung der Produkte noch subjektiv-individuelle Vorstellungen einzelner Nachfrager, des marktbeherrschenden
Unternehmens oder der Konkurrenten, sondern allein auf die objektive Sichtweise des Durchschnittskunden
in Bezug auf die übliche Verwendung der jeweiligen Produkte abzustellen (Urteile B-831/2011, SIX,
E. 1313;
B-3618/2013, Hallenstadion, E. 255).
Auch die Terminologie oder die Geschichte der in Frage stehenden Güter sind untaugliche Kriterien
(Amstutz/Carron, BSK-KG, Art. 7 N 729).
13.5.3 Ob
die Produkte als separate Produkte angesehen werden, hängt von der Verbrauchernachfrage ab. Zwei
separate Produkte liegen dann vor, wenn ohne die Koppelung bzw. Bündelung eine grosse Anzahl von
Kunden das Koppelungsprodukt kaufen würden bzw. gekauft hätten, ohne auch das gekoppelte Produkt
beim selben Anbieter zu erwerben, so dass jedes der beiden Produkte unabhängig vom anderen hergestellt
werden kann. Als direkter Beweis für die Existenz zweier separater Produkte kann der Umstand gelten,
dass Verbraucher, wenn sie die Wahl haben, das Koppelungs- und das gekoppelte Produkt von unterschiedlichen
Quellen beziehen. Als indirekter Beweis kann die Marktpräsenz von Unternehmen, die auf die Fertigung
oder den Verkauf des gekoppelten Produkts (ohne das Koppelungsprodukt) spezialisiert sind, gelten. Der
Nachweis zweier verschiedener Güter kann auch auf der Basis des Verhaltens von Anbietern begründet
werden, die über keine marktbeherrschende Stellung verfügen und unter Bedingungen wirksamen
Wettbewerbs tätig sind: Tendieren diese dazu, die beiden Güter nicht zu kombinieren, kann davon
ausgegangen werden, dass ihr Angebot der Kundennachfrage am besten entspräche und dass folglich
zwei gesonderte Güter vorlägen (Amstutz/Carron,
BSK-KG, Art. 7 N 728; Ziff. 51 der Prioritätenmitteilung).
13.5.4 Die
Vorinstanz erwog, die Zulassungsinhaberinnen seien im Unterschied zu früher nur verpflichtet, die
Arzneimittelinformationen auf AIPS zu publizieren. Es bestehe jedoch keine gesetzliche Pflicht zur Aufnahme
in das Compendium. Im Hinblick auf die obligatorische Publikation auf AIPS erfolge eine redaktionelle
und technische Qualitätssicherung im Rahmen des Zulassungsgesuches durch Swissmedic. Dabei würden
die Zulassungsinhaberinnen vorgängig eine Qualitätssicherung durchführen, welche im Zulassungsverfahren
durch Swissmedic genehmigt werde. Durch dieses Verfahren werde die Qualität der Arzneimittelinformationen
gewährleistet und damit die den Zulassungsinhaberinnen obliegende Sorgfaltspflicht erfüllt.
Eine nachgelagerte erneute redaktionelle Qualitätssicherung sei nicht notwendig. Die vorgängige
Qualitätskontrolle könne durch die Zulassungsinhaberinnen selbst oder durch Externe durchgeführt
werden, was das Vorliegen getrennter Dienstleistungen beweise. Das gleiche gelte für den Prozess
des Uploads auf AIPS. Es bestehe keine Pflicht der Zulassungsinhaberinnen einen privaten Anbieter zu
engagieren, Outsourcing sei aber möglich. Gemäss Antworten der Zulassungsinhaberinnen auf den
Fragebogen des Sekretariates im Jahr 2013 hätten zumindest acht Unternehmen die Dienstleistung der
Qualitätskontrolle und des Uploads angeboten. Auch HCI wäre es offen gestanden, separat eine
Qualitätskontrolle für die Publikation auf AIPS und den Upload auf AIPS anzubieten.
13.5.5 Der
Upload auf AIPS müsse als zusätzlicher Arbeitsschritt vorgenommen werden, der von der Strukturierung
und Codierung bzw. der Aufnahme der Daten in die INDEX-Produkte unabhängig vollzogen werde.
13.5.6 Weiter
erwog die Vorinstanz, gewisse Arbeiten, die im Zusammenhang mit der Aufnahme der Daten in die Datenbank
eines Datenveredlers erbracht würden, wie beispielsweise die Strukturierung und Codierung der Daten,
seien so eng mit dieser verknüpft, dass eine Trennung der Dienstleistungen nicht möglich sei.
Die redaktionelle und technische Qualitätskontrolle müsse hingegen als zusätzlicher Arbeitsschritt
vorgenommen werden. Durch die Strukturierung und Codierung könne nicht mit dem gleichen Aufwand
oder mit unwesentlichen Mehraufwand gleichzeitig eine Qualitätssicherung vorgenommen werden. Hinzukomme,
dass diese Dienstleistung von HCI nur einen Mehrwert bringe, wenn sie vor der Publikation auf AIPS erfolge,
sie aber durch die Gestaltung der Module mit der Aufnahme ins Kompendium bzw. die INDEX-Datenbanken verknüpft
sei.
13.5.7 Bei
der Aufnahme der Daten in die Datenbank von HCI werden verschiedene Arbeiten ausgeführt und teilweise
vermischt. Einerseits werden die Daten strukturiert und codiert. Diese Arbeiten sind - wie von
der Vorinstanz festgestellt - mit der Aufnahme der Daten in die Datenbank so eng verknüpft,
dass eine Trennung der Dienstleistungen nicht möglich ist. Gleiches gilt für Qualitätssicherungsarbeiten,
die zwingend und direkt mit der Struktur und Codierung der Datenbanken von HCI verbunden sind. Auch diesbezüglich
liegen keine separaten Dienstleistungen vor. Weiter geben die Beschwerdeführerinnen an, für
ihr Produkt die Aktualität der Daten auf AIPS zu überprüfen. Dies stellt ebenfalls ein
logischer mit der Aufnahme der Daten in die Datenbank zusammenhängender Schritt dar, welcher nicht
abtrennbar ist.
13.5.8 Weiter
nimmt HCI redaktionelle und technische Qualitätskontrolle bei den Arzneimittelinformationen, d.h.
den Fach- und Patienteninformationen, vor, die von Swissmedic in einem Prüfungsvefahren geprüft
werden. Darüber hinaus beschränkt sich die Qualitätskontrolle von HCI nicht nur auf diese
Arzneimittelinformationen, die auch auf AIPS hochzuladen sind, sondern betreffen auch weitere Informationen
und Daten. Was die redaktionelle und technische Qualitätskontrolle der Arzneimittelinformationen,
d.h. der Fach- und Patienteninformationen betrifft, ist der Vorinstanz zuzustimmen, dass für diese
bereits im Rahmen des Zulassungsgesuches durch Swissmedic geprüfte Daten keine zusätzlich nachgelagerte
Qualitätskontrolle notwendig ist. Die Qualitätskontrolle dieser Informationen stellt eine separate
Dienstleistung dar, die unabhängig von der Aufnahme und dem Erhalt in elektronischen Datensätzen
betreffend Medikamenteninformationen bzw. in concreto der Aufnahme in die INDEX-Produkte und das Compendium
nachgefragt bzw. angeboten werden (kann). Dies folgt einerseits aus dem Umstand, dass für ersteres
eine regulatorische Pflicht besteht, für zweiteres hingegen nicht. Anderseits ergibt sich dies aus
dem Umstand, dass ersteres gemäss den Antworten der Zulassungsinhaberinnen auf den Fragebogen des
Sekretariates im Jahr 2013 zumindest von acht Unternehmen angeboten oder von den Zulassungsinhaberinnen
selbst durchgeführt wurde.
13.5.9 Auch
der Upload auf AIPS stellt ein zusätzlicher Arbeitsschritt dar, der von der Strukturierung und Codierung
bzw. der Aufnahme der Daten in die INDEX-Produkte unabhängig vollzogen wird. Dass dieser Arbeitsschritt
nicht zwingend mit den Dienstleistungen der Datenbankplattform im Markt für den Zugang zu veredelten
Daten verbunden ist, wird auch von den Beschwerdeführerinnen explizit anerkannt.
13.5.10 Die
Beschwerdeführerinnen rügen, die Vorinstanz habe keine Marktabgrenzung vorgenommen und auf
eine marktorientierte Analyse der Frage, ob die gekoppelten Dienstleistungen in unterschiedlichen Märkten
nachgefragt werden, verzichtet.
13.5.11 Die
Vorinstanz hat sich in der Verfügung mit dem Markt der Qualitätskontrolle bzw. der Marktabgrenzung
auseinandergesetzt und hierzu unterschiedliche Aspekte aufgeführt (s. oben E. 13.5.4
f.). Gestützt darauf kam sie zum Schluss, dass die redaktionelle und technische Qualitätskontrolle
der Arzneimittelinformationen im Hinblick auf die Publikation sowie der Upload dieser Informationen auf
AIPS einerseits und die Veredelung der Medikamenteninformationen (inkl. einer allfälligen, mit der
Erstellung des spezifischen Produktes zusammenhängenden [erneuten] Qualitätssicherung) andererseits
nicht dem gleichen Markt zuzuordnen sind und separate Märkte darstellen.
13.5.12 Für
die Qualitätskontrolle der Arzneimittelinformationen im Hinblick auf die Publikation und den Upload
dieser Informationen auf AIPS besteht eine regulatorische Pflicht. Dieses Dienstleistungspaket wir auf
dem (separaten sachlich relevanten) "Markt für Beratungs- und Unterstützungsdienstleistungen
während des Zulassungsverfahrens" gehandelt. Dieser Markt ist zeitlich unbefristet. Die auf
dem Markt gehandelten Leistungen sind aber nur solange von Interesse für die Nachfrager, wie das
jeweilige Zulassungsverfahren von Swissmedic noch nicht abgeschlossen ist.
13.5.13 In
der Pharmabranche ist es nicht unüblich, dass sich die Zulassungsinhaberinnen während des Zulassungsverfahrens
von einem externen Dienstleister beraten und unterstützen lassen. In einzelnen Fällen wird
die Abwicklung der Zulassung auch gänzlich outgesourct. In der Schweiz haben sich mehrere Unternehmen
in diesem Bereich spezialisiert (vgl. Stellungnahmen der Zulassungsinhaberinnen zum Auskunftsbegehren,
insb. Vorinstanz, act. 173, 196, 279 ff., 320 und 389). Es kann davon ausgegangen werden, dass das Dienstleistungspaket
"Qualitätskontrolle der Arzneimittelinformationen mit optionalem Gratisupload auf AIPS"
von HCI und Dritten ohne Weiteres separat auf dem Markt angeboten werden kann. Ebenso kann davonausgegangen
werden, dass die Zulassungsinhaberinnen dieses Dienstleistungspaket effektiv nachfragen würden und
hierfür eine gewisse Zahlungsbereitschaft bestehen würde. Dies insbesondere auch deshalb, weil
das Zulassungsverfahren im Endeffekt auch von der Qualität der Arzneimittelinformationen abhängig
ist. Reichen die Zulassungsinhaberinnen ihre Arzneimittelinformationen bereits von Beginn an in einer
hohen Qualität zur Genehmigung ein, geht das Zulassungsverfahren wesentlich schneller. Die Nachfrage
bzw. Zahlungsbereitschaft der Zulassungsinhaberinnen für das Dienstleistungspaket "Qualitätskontrolle
der Arzneimittelinformationen mit optionalem Gratisupload auf AIPS" sinkt jedoch gegen Null, sobald
das Zulassungsverfahren abgeschlossen und die Arzneimittelinformationen auf AIPS hochgeladen sind.
13.5.14 Unerheblich
ist im Übrigen ob Dritte nur diese Dienstleistungen
oder (teilweise) gleichzeitig
weitere Dienstleistungen auf dem "Markt für Beratungs- und Unterstützungsdienstleistungen
während des Zulassungsverfahrens von Swissmedic" anbieten bzw. übernehmen. Insofern lässt
sich aus dem Vorbringen der Beschwerdeführerinnen, die meisten derjenigen Zulassungsinhaberinnen,
welche die Qualitätskontrolle und den Upload auf AIPS an Externe ausgelagert hätten, hätten
den gesamten regulatorischen Bereich an Dritte übertragen, nichts zu ihren Gunsten ableiten.
13.5.15 Die
Beschwerdeführerinnen machen weiter geltend, ihre Qualitätssicherung beziehe sich auf die zu
verarbeitenden Informationen im Kontext der Strukturierung und Codierung der Daten und erfolge im Hinblick
auf die Integration der Daten in ihre Datenbanken. Sie stelle damit eine notwendige "Begleiterscheinung"
ihrer Dienstleistung dar. Die Arbeiten seien sehr eng miteinander verknüpft. In der Eingabe vom
16. November 2018 legen die Beschwerdeführerinnen zudem dar, es verzichte nur ein geringer Prozentsatz
der Zulassungsinhaberinnen auf die Qualitätskontrolle für die Fachinformationen, seit sie diese
aufgrund des Entscheids der Vorinstanz optional anbiete. Bei der Weiterverarbeitung der Daten im INDEX
müsse HCI aber dennoch eine Qualitätskontrolle durchführen, welche nahezu alle relevanten
Kapitel erfasse, die HCI auch im Rahmen der beauftragten Prüfung der Fachinformation zu kontrollieren
habe.
13.5.16 Bei
der Beurteilung, ob zwei getrennte Güter vorliegen, ist allein auf die objektive Sichtweise des
Durchschnittskunden abzustellen, die subjektiv-individuellen Vorstellungen des marktbeherrschenden Unternehmens
sind nicht massgebend. Entsprechend ist es für die Beurteilung nicht relevant, wenn die Beschwerdeführerin
2 ihre Prozesse so gestaltet, dass die Arbeiten eng miteinander verbunden und vermischt sind. Massgebend
ist alleine, dass die Qualitätskontrolle der Arzneimittelinformationen mit optionalem Upload auf
AIPS bei einer objektiven Betrachtung von einem Durchschnittskunden separat nachgefragt werden kann.
Der geltend gemachte Umstand, dass trotz neuer Optionalität die Mehrheit der Zulassungsinhaberinnen
auf die Qualitätskontrolle der HCI nicht verzichten würde, stellt ein späterer Verlauf
unter anderen tatsächlichen Gegebenheiten dar. Aus einem solchen können aber - gerade
bei komplexen Märkten und in Zusammenhang mit Innovationswettbewerb - kaum aussagekräftige
Schlüsse für frühere Perioden gezogen werden.
13.5.17 Weiter
bringen die Beschwerdeführerinnen vor, die Qualitätskontrolle von HCI werde durch die Überprüfung
einer Sprachversion (nicht aber der Übersetzungen) durch Swissmedic in keiner Weise ersetzt. HCI
entdecke sowohl in den von Swissmedic geprüften Arzneimittelinformationen als auch - und das
sei häufiger - in den von Swissmedic nicht geprüften Übersetzungen regelmässig
Fehler. Da die Daten derart sensibel seien, könne der geringste Fehler katastrophale Auswirkungen
haben. Entsprechend bilde die Qualitätssicherung durch Swissmedic keinen Ersatz für die Qualitätskontrolle
von HCI.
13.5.18 Die
Vorinstanz hält hierzu zu Recht fest, dass weder den Zulassungsinhaberinnen bezüglich ihrer
eigenen Produkte der Fachverstand und die notwendigen Fähigkeiten abgesprochen werden kann, noch
Swissmedic betreffend der von ihr geprüften Version der Arzneimittelinformationen. Hinzukommt, dass
die Zulassungsinhaberinnen selbst ein grosses Interesse an fehlerfreien Arzneimittelinformationen haben.
So sind für die Korrektheit und Aktualität der Arzneimittelinformationen, inkl. der korrekten
Übersetzung der Texte, auf AIPS allein die Zulassungsinhaberinnen verantwortlich (vgl. www.swissmedicinfo.ch/Accept.aspx?ReturnUrl=%2f
[abgerufen am 18.08.2020]). Was die beiden übersetzten Sprachversionen betrifft, welche nicht von
Swissmedic geprüft werden, könnte die Patientensicherheit auch gewährleistet werden, indem
HCI für die Aufnahme der Daten in ihre Datenbank voraussetzt, dass auch diese beiden Versionen vorgängig
einer externen Qualitätssicherung unterzogen worden sind. Eine Qualitätskontrolle der beiden
übersetzten Sprachversionen der Arzneimittelinformationen hat auf jeden Fall nicht zwingend zusammen
mit der Dienstleistung der Aufnahme und Erhalt in elektronischen Datensätzen betreffend Medikamenteninformationen
bzw. in concreto zusammen mit der Aufnahme in die INDEX-Produkte und das Compendium zu erfolgen.
13.5.19 Die
Beschwerdeführerinnen rügen sodann, dass die Leistungserbringerinnen und -erbringer nicht befragt
worden seien. Eine Datenbank ohne Qualitätskontrolle befriedige deren Nachfrage nicht. Auf dieses
Vorbringen wird unten bei der Prüfung der sachlichen Rechtfertigungsgründe einzugehen sein
(s. E. 13.8.14).
Bei der Beurteilung, ob separate Produkte vorliegen, ist das Argument unwesentlich. Hier gilt es wie
vorerwähnt zu prüfen, ob aus Sicht der Marktgegenseite Haupt- und Zusatzprodukt unabhängig
voneinander nachgefragt bzw. angeboten werden (würden). Marktgegenseite stellen im vorliegenden
Kontext aber nicht die Leistungserbringerinnen und -erbringer, sondern die Zulassungsinhaberinnen dar.
13.5.20 Die
Beschwerdeführerinnen machen schliesslich geltend, mit dem Modul D3 ein Angebot gehabt zu haben,
das sonstige Dienstleistungen und namentlich die Qualitätssicherung im Hinblick auf die Publikation
abgedeckt hätte, dieses aber nicht nachgefragt worden sei. Daraus folgern die Beschwerdeführerinnen,
dass kein Markt für die Qualitätssicherung im Hinblick auf die Publikation bestehe. Die Vorinstanz
geht hingegen davon aus, dass das Modul D3 im vorliegend relevanten Bereich der Qualitätssicherung
nicht über das Basismodul hinausgehe, das bereits gebündelt an die Aufnahme in die Datenbank
die redaktionelle Qualitätssicherung angeboten werde. Die von den Beschwerdeführerinnen geltend
gemachte fehlende Nachfrage sei deshalb in der Koppelung selbst begründet. Durch die Koppelung werde
die gesonderte Nachfrage für das gekoppelte Gut eliminiert, da sie bereits über die Nachfrage
nach dem koppelnden Gut gestillt werde. Die Beschwerdeführerinnen entgegnen, dass im Jahr 2013 rund
[...] der Zulassungsinhaberinnen keine Verträge mit HCI abgeschlossen hätten und von ihnen
das Modul D3 dennoch nicht nachgefragt worden sei, weshalb die Schlüsse der Vorinstanz nicht zutreffen
würden.
13.5.21 Aus
der kurzen Phase von 2013, in welcher gewisse Zulassungsinhaberinnen vorübergehend keine Verträge
mit HCI abgeschlossen hatten, lassen sich jedoch keine aussagekräftigen Schlüsse ziehen. Auch
die Beschwerdeinstanz erachtet es als naheliegend, dass die mangelnde Nachfrage des Modul D3, was die
Qualitätskontrolle der Arzneimittelinformationen betrifft, in der Koppelung selbst begründet
ist. In jedem Fall lässt sich aus der mangelnden Nachfrage des Moduls D3 nicht auf das fehlende
Vorliegen von separaten Produkten schliessen.
13.5.22 Was
den Arbeitsschritt des Uploads auf AIPS betrifft, machen die Beschwerdeführerinnen geltend, es bestehe
gar kein separater Markt, da die Dienstleistung derart marginal sei. Der Aufwand für den Upload
einer Fach- und Patienteninformation betrage Sekunden bzw. maximal wenige Minuten. Ein separates Angebot
würde auf keine Nachfrage stossen.
13.5.23 Dieses
Vorbringen ist jedoch unwesentlich, da die Qualitätskontrolle der Arzneimittelinformationen und
der (optionale) Upload auf AIPS als gemeinsames Dienstleistungspaket zu begreifen ist (s. oben E. 13.5.12
f.). Doch auch selbst wenn bei der Qualitätskontrolle und dem Upload auf AIPS von zwei separaten
Dienstleistungen ausgegangen würde, die auf dem "Markt für Beratungs- und Unterstützungsdienstleistungen
während des Zulassungsverfahrens von Swissmedic" gehandelt würden, überzeugt dieses
Argument nicht. Denn einerseits stellt bereits der Umstand, dass HCI unterdessen den Upload auf AIPS
als kostenpflichtige Einzelleistung anbietet, ein Hinweis auf eine mögliche Nachfrage und damit
ein Beleg für einen separaten Markt dar. Andererseits kann aus dem blossen Umstand, dass eine Dienstleistung
nur wenige Minuten in Anspruch nimmt, nicht geschlossen werden, dass dafür kein separater Markt
bestehen kann. In unserer stark arbeitsteiligen Gesellschaft und Wirtschaft gibt es in vielen Bereichen
durchaus eine separate Nachfrage bzw. einen separaten Markt für Dienstleistungen, die an sich nur
sehr wenig Zeit in Anspruch nehmen.
13.5.24 Zusammengefasst
kann festgehalten werden, dass bezüglich gewisser Teilarbeiten die Qualitätskontrolle nicht
als separate Dienstleistung betrachtet werden kann. Dies gilt für Qualitätssicherungsarbeiten,
die zwingend und direkt mit der Struktur der Datenbanken von HCI verbunden sind und betreffend die Überprüfung
der Aktualität der Informationen. Die Dienstleistung Qualitätskontrolle der auf AIPS hochzuladenden
Arzneimittelinformationen mit anschliessendem (optionalem) Upload auf AIPS, d.h. der Fach- und Patienteninformationen
in den drei Sprachversionen, stellt jedoch eine von der Aufnahme und dem Erhalt in elektronischen Datensätzen
betreffend Medikamenteninformationen bzw. in concreto der Aufnahme in die INDEX-Produkte und das Compendium
unabhängige und getrennte Dienstleistung dar.
13.6 Verknüpfung
von Haupt- und Zusatzprodukt
13.6.1 Eine
Koppelung bzw. Kombination von Haupt- und Zusatzprodukt liegt vor, wenn diese vom marktbeherrschenden
Unternehmen in einer Weise angeboten werden, dass für die Marktgegenseite die Notwendigkeit zur
gemeinsamen Abnahme von Haupt- und Zusatzprodukt besteht (Urteile 2C_113/2017, Hallenstadion,
E. 6.2.2; B-831/2011, SIX, E. 1328;
B-3618/2013,
Hallenstadion, E. 256; Amstutz/Carron,
BSK-KG, Art. 7 N 732; Clerc/Këllezi, CR-Concurrence,
Art. 7 II N 274; Weber/Volz, a.a.O., Rz. 2.761). Der Abnehmer
ist in der Wahl der zusätzlichen Leistung nicht frei (Urteil 2C_113/2017, Hallenstadion,
E. 6.2.2).
13.6.2 Im
Allgemeinen kann eine direkte Koppelung zweier Güter auf verschiedene Arten erfolgen: Eine vertragliche
Koppelung liegt vor, wenn ein marktbeherrschendes Unternehmen seine Handelspartner de iure verpflichtet,
beide Güter zu erwerben. Hingegen liegt eine technische Koppelung vor, falls die Güter durch
deren physische Ausgestaltung nur gemeinsam bezogen werden können. Schliesslich kann eine Koppelung
auch durch ökonomische Anreize erfolgen, falls beide Güter zwar separat erhältlich sind,
aber beispielsweise der separate Bezug nur eines der Güter wirtschaftlich nicht sinnvoll ist (Amstutz/Carron,
BSK-KG, Art. 7 N 737). Mit anderen Wort liegt eine ökonomische Koppelung vor, wenn die gleichzeitige
Nachfrage von Haupt- und Zusatzprodukt aufgrund spezifischer ökonomischer Anreize wie die Ausgestaltung
von Gesamtpreisen oder Gewährung von Rabatten und sonstigen Vergünstigungen bei einer gemeinsamen
Abnahme bzw. Lieferung von Haupt- und Zusatzprodukt für die Marktgegenseite bei realistischer Betrachtung
offensichtlich vorzuziehen ist (Urteil B-831/2011, SIX, E. 1330).
13.6.3 Die
Notwendigkeit zu einer Abnahme bzw. Erbringung von verschiedenen separaten Produkten ist immer dann gegeben,
wenn sich aufgrund der konkreten vertraglichen oder faktischen Umstände des Einzelfalls eine Zwangswirkung
zum Erwerb oder zur Abgabe von mindestens zwei Produkten für den potentiellen Geschäftspartner
des marktbeherrschenden Unternehmens einstellt. In welcher Art und Weise und mit welchen Mitteln diese
Zwangswirkung von Seiten des marktbeherrschenden Unternehmens herbeigeführt wird, ist dabei unerheblich.
Denn es existiert kein numerus clausus an tatbestandmässigen Varianten einer Verknüpfung (Urteil
B-831/2011, SIX, E. 1331).
13.6.4 Für
das Vorliegen einer Kombination ist es nicht erforderlich, dass das marktbeherrschende Unternehmen Zwang
gegenüber der Marktgegenseite ausübt. Bei einer vertraglichen Kombination ist es bereits ausreichend,
dass die Marktgegenseite nicht frei über die Wahl des Zusatzprodukts entscheiden kann. Eine entsprechende
Wahlmöglichkeit ist bereits dann nicht gegeben, wenn die Marktgegenseite aufgrund der Ausgestaltung
des Angebots durch das marktbeherrschende Unternehmen davon ausgehen kann, dass eine fehlende Abnahme
des Zusatzprodukts zum Scheitern des Hauptgeschäfts führen wird (Urteile B-831/2011, SIX,
E. 1335; B-3618/2013, Hallenstadion, E. 260).
13.6.5 Keine
Voraussetzung für eine Kombination von Haupt- und Zusatzprodukt stellen die Vereinbarung eines spezifischen
Entgelts für das Zusatzprodukt oder die Verpflichtung zur Nutzung des Zusatzprodukts dar (Urteile
B-831/2011, SIX, E. 1339; B-3618/2013, Hallenstadion,
E. 262). Ebenfalls keine Voraussetzung bildet das Vorhandensein eines Missverhältnisses zwischen
einer allfälligen Gegenleistung für das Zusatzprodukt beim Verbundgeschäft oder der Gegenleistung
für Haupt- und Zusatzprodukt beim Bündelgeschäft (Urteile B-831/2011, SIX,
E. 1338; B-3618/2013, Hallenstadion, E. 262; Amstutz/Carron,
BSK-KG, Art. 7 N 741; Clerc/Këllezi, CR-Concurrence,
Art. 7 II N 270).
13.6.6 Die
Vorinstanz erwog, HCI koppele den Bezug der Qualitätskontrolle vertraglich mit der Aufnahme in das
Compendium und die INDEX-Daten im Basismodul D1 + E1. Betreffend den Upload der Daten auf AIPS erwog
die Vorinstanz, dass dieser zwar nicht zwangsläufig habe bezogen werden müssen. Er sei aber
gratis zum Basismodul D1+E1 angeboten worden. Einzeln werde er nicht angeboten. Entsprechend handle es
sich um eine vertragliche Koppelung.
13.6.7 Die
Erwägungen der Vorinstanz betreffend die Qualitätskontrolle sind nicht zu beanstanden. Es liegt
eine reine Bündelung vor, da die Dienstleistungen nicht getrennt erhältlich waren.
13.6.8 Die
Beschwerdeführerinnen bringen jedoch vor, mit dem Modul D3 sei ein separates Angebot für qualitätssichernde
Dienstleistungen verfügbar gewesen. Dieses Vorbringen vermag jedoch nicht zu überzeugen.
Denn der Inhalt eines Koppelungsgeschäfts besteht u.a. darin, dass der Abschluss eines Geschäfts
über ein bestimmtes (Haupt-)Produkt ("koppelndes Gut") - in casu die Aufnahme und
der Erhalt in elektronischen Datensätzen betreffend Medikamenteninformationen bzw. in concreto der
Aufnahme in die INDEX-Produkte und das Compendium - von Zugeständnissen für die Abnahme
oder die Lieferung eines weiteren (Zusatz-)Produkts ("gekoppeltes
Gut") - in casu die Qualitätskontrolle - abhängig gemacht wird. Ob hierbei
das Zusatzprodukt auch separat angeboten wird, ist unerheblich. Entscheidend ist, dass das koppelnde
Gut nur bei Abnahme des gekoppelten Gutes erhältlich ist. Hinzukommt, dass es fraglich erscheint,
dass im Modul D3 genau die identischen Qualitätskontrollen vorgenommen wurden wie bei den in den
Basismodulen D1 + E1 enthaltenen.
13.6.9 Soweit
die Beschwerdeführerinnen zudem geltend machen, die Validierung der Daten sei eine notwendigerweise
vorausgesetzte Eigenschaft der Daten von HCI, kann auf E.13.5
verwiesen werden. Es handelt sich bei Qualitätskontrolle der Arzneimittelinformationen (mit [optionalem]
Upload auf AIPS) und der Aufnahme der Daten in die Datenbanken der Beschwerdeführerinnen um zwei
separate Dienstleistungen.
13.6.10 Betreffend
Upload auf AIPS rügen die Beschwerdeführerinnen, die Vorinstanz verwechsle das gekoppelte Gut
mit dem koppelnden Gut. Die Vorinstanz habe weder eine entsprechende Marktabgrenzung vorgenommen, noch
sei sie zum Schluss gekommen, dass HCI auf dem Markt für den Upload von Fach- und Patienteninformationen
eine marktbeherrschende Stellung einnehme. Es käme höchstens eine ökonomische Koppelung
in Frage, indem HCI Anreize setze, die Upload-Dienstleistung bei HCI zu beziehen. Diese Dienstleistung
sei aber derart marginal, dass deren optionalen Bezug ohne gesondertes Entgelt vernünftigerweise
nicht als ökonomische Koppelung angesehen werden könne.
13.6.11 Die
Koppelung entspringt einer Vertragsklausel, namentlich Ziffer 2 der "Vereinbarung zur Publikation
von Informationen im Arzneimittel-Kompendium der Schweiz® und in den INDEX-Produkten", wonach
der Upload der Daten auf AIPS kostenlos zum Basismodul D1+E1 dazu angeboten wurde.
13.6.12 Es
stand den Zulassungsinhaberinnen aber frei, dieses kostenlose Zusatzangebot des Uploads zum Basismodul
D1+E1 zu beziehen. Ein Zwang, das gekoppelte Gut zusammen mit dem koppelnden Gut zu beziehen, bestand
nicht. Oder mit anderen Worten gesagt, hat HCI die Aufnahme und den Erhalt in elektronischen Datensätzen
betreffend Medikamenteninformationen auch dann angeboten und verkauft, wenn die Dienstleistung des Uploads
auf AIPS nicht in Anspruch genommen wurde. Somit kann weder eine Bündelung ("pure bundling")
noch ein Verbundgeschäft ("tying") vorliegen. Es kann nur ein Anreizgeschäft ("mixed
bundling") in Frage stehen. Beim Anreizgeschäft ("mixed
bundling") ist der Anbieter - anders als bei den anderen
beiden Koppelungstechniken - grundsätzlich bereit die Güter auch separat anzubieten,
jedoch erhält der Abnehmer einen reduzierten Preis, wenn er sie zusammen erwirbt. Vorliegend wurde
zwar nur das koppelnde Gut einzeln angeboten, während das gekoppelte Gut nicht separat angeboten
wurde. Indem das gekoppelte Gut kostenlos zum koppelnden Gut angeboten wurde, besteht aber ein sehr hoher
ökonomischer Anreiz, das gekoppelte Gut ebenfalls bei HCI zu beziehen. Insofern liegt offensichtlich
eine dem Anreizgeschäft ("mixed bundling") vergleichbare
ökonomische Koppelung der beiden Dienstleistungen vor.
13.6.13 Auf
das Vorbringen der Beschwerdeführerinnen, aufgrund der Marginalität der Dienstleistung liege
keine ökonomische Koppelung vor, ist bei der Prüfung der sachlichen Rechtfertigungsgründen
einzugehen.
13.6.14 Eine
Koppelung von Haupt- und Zusatzprodukt ist somit gegeben.
13.7 Wettbewerbsbeschränkender
Effekt
13.7.1 Die
Koppelung der Produkte muss für den Wettbewerb auf dem Markt des Hauptprodukts oder auf dem Markt
des Zusatzprodukts zu einer nachteiligen Konstellation führen (Urteile B-831/2011, SIX,
E. 1376).
13.7.2 In
der Literatur werden verschiedene Auffassungen betreffend Charakter, Inhalt, Ausmass und Nachweis dieses
nachteiligen Effekts vertreten. Nach der einen Ansicht muss die Kombination von Haupt- und Zusatzprodukt
eine Wettbewerbsbeeinträchtigung zur Folge haben (Amstutz/Carron,
BSK-KG, Art. 7 N 746 ff.). Für deren Feststellung sei von der Wettbewerbsbehörde eine umfassende
Analyse vorzunehmen, inwieweit ein Verdrängungseffekt zu Lasten der Konkurrenten oder ein Ausbeutungseffekt
zu Lasten der Marktgegenseite vorliege. Nach anderer Ansicht, wird angenommen, dass zumindest bei einer
Verknüpfung von nicht komplementären Produkten für das Vorliegen einer Koppelung eine
spezifische Beeinträchtigung des Wettbewerbs vorliegen müsse (Stäuble/Schraner,
DIKE-KG, Art. 7 N 503 f.; Weber/Volz, a.a.O., Rz. 2.769).
Nach weiterer Ansicht ist eine Verknüpfung von Haupt- und Zusatzprodukt immer dann als wettbewerbswidrig
zu qualifizieren, soweit keine Rechtfertigung für eine Verknüpfung der separaten Produkte aufgrund
von sachlich angemessenen Gründen besteht (Borer, a.a.O.,
Art. 7 Rz. 27; Clerc/Këllezi,
CR-Concurrence, Art. 7 II N 278;
David/Jacobs, a.a.O., Rz. 746; für komplementäre Güter im Ergebnis wohl auch Stäuble/Schraner,
DIKE-KG, Art. 7 N 502; Weber/Volz, a.a.O., Rz. 2.765
und 2.767). Danach bedürfe es keiner über die Aspekte der Rechtfertigung hinausgehenden Abklärungen
für die Feststellung eines nachteiligen Effekts.
13.7.3 Die
bisherige Entscheidungspraxis der Europäischen Kommission sieht keine Untersuchung der tatsächlichen
Auswirkungen vor. Es sei bei einem Koppelungsgeschäft per se von einer Ausschlusswirkung auf dem
jeweiligen Markt auszugehen (vgl. Entscheidung Kommission Microsoft,
ABl. 2004 L 32/23 Rn. 841). Die EU-Rechtsprechung bezieht ebenfalls keine Analyse der tatsächlichen
Auswirkungen in ihre Prüfung des Koppelungsgeschäfts mit ein (vgl. Urteil EuG Microsoft/Kommission,
Slg. 2007 II-03601 Rn. 868). Demgegenüber anerkennt die Europäische Kommission in ihren Durchsetzungsprioritäten
das Element einer wahrscheinlichen
oder tatsächlichen Marktverschliessung als
notwendiges Merkmal eines Koppelungsgeschäfts (Prioritätenmitteilung; zum Ganzen ausführlicher:
Urteil 831/2011, SIX, E. 1381 und 1383 f.). Die Prioritätenmitteilung
widerspricht damit der Entscheidungspraxis der Europäischen Kommission zumindest insoweit, als sie
das Regel-Ausnahmeverhältnis umkehrt.
13.7.4 Das
Bundesverwaltungsgericht hielt im Urteil B-3618/2013 vom 24. November 2016 i.S. Hallenstadion
fest, für die Beurteilung eines Koppelungsgeschäfts sei der Umstand massgebend, dass ein sich
aus der Koppelung ergebender negativer Effekt für die Marktgegenseite oder die Konkurrenten des
marktbeherrschenden Unternehmens vorhanden sein und demzufolge im Einzelfall auch eine Ausbeutung oder
eine Behinderung des Wettbewerbs im Sinne von Art. 7 Abs. 1 KG vorliegen müsse. Lägen die Voraussetzungen
der Marktbeherrschung und der Kombination von getrennten Produkten durch das marktbeherrschende Unternehmen
vor, so sei grundsätzlich davon auszugehen, dass ein solcher negative Effekt gegeben sei, weil der
Absatz des Zusatzprodukts in derartigen Fällen nicht allein auf dessen originären Leistungsfaktoren
beruhe, sondern an die Abnahme des Hauptprodukts anknüpfe. Daher sei die Wettbewerbsmässigkeit
einer Produktekombination regelmässig nur bei Vorliegen eines ausreichenden Rechtfertigungsgrunds
gegeben. Ausnahmsweise sei es aber möglich, dass für eine bestimmte Kombination von separaten
Produkten ein nachteiliger Effekt nicht festgestellt werden könne, weshalb dann weder eine Ausbeutung
der Marktgegenseite noch eine Behinderung von Konkurrenten gegeben sei (Urteil B-3618/2013, Hallenstadion,
E. 264 m.H. auf RPW 2005/1 S. 46 Rz. 59 und 63, TopCard-Angebot der Bergbahnen
Lenzerheide-Valbella, Klosters-Davos und Flims-Laax-Falera).
13.7.5 Im
Urteil B-831/2011 vom 18. Dezember 2018 i.S. SIX setzte sich das
Bundesverwaltungsgericht jüngst erneut eingehend mit der Beurteilung des Aspekts, ob und inwieweit
die tatsächlichen Auswirkungen zu untersuchen und notwendigerweise bestimmte qualitative, quantitative
oder temporäre Anwendungsschwellen für die Feststellung eines nachteiligen Effekts bei Koppelungssachverhalten
zu berücksichtigen sind, auseinander. Es erwog, dass gegen die Anerkennung bestimmter quantitativer,
qualitativer oder temporalen Anwendungsschwellen neben dem Wortlaut des Regelbeispiels und der Entstehungsgeschichte,
die keinerlei Hinweise auf die Anwendung entsprechender Kriterien aufweisen, insbesondere auch der Sinn
und Zweck der Vorschrift spreche und legte hierzu ausführlich verschiedene Aspekte dar. Für
die Anerkennung einer wettbewerbswidrigen Koppelung gemäss Art. 7 KG bedürfe es keiner besonderen
quantitativen, qualitativen oder temporären Anwendungsschwellen. Der Aspekt des nachteiligen Effekts
bilde ein ungeschriebenes Tatbestandsmerkmal im Sinne eines Ausschlusskriteriums für Sachverhalte,
bei denen der Eintritt einer Wettbewerbsverfälschung entgegen den üblichen Konstellationen
von vornherein mit Sicherheit ausgeschlossen werden könne, weshalb es keiner weiteren Abklärung
des Vorliegens von sachlichen Rechtfertigungsgründen bedürfe. Das Bundesverwaltungsgericht
bestätigte seine Rechtsprechung, wonach bei Vorliegen einer Verknüpfung von separaten Produkten
durch ein marktbeherrschendes Unternehmen grundsätzlich davon auszugehen ist, dass ein für
den Wettbewerb negativer Effekt vorliegt, weil der Absatz des Zusatzprodukts in derartigen Fällen
nicht allein auf dessen originären Leistungsfaktoren beruht, sondern an die Abnahme des Hauptprodukts
anknüpft. Daher sei die Wettbewerbsmässigkeit einer Produkteverbindung regelmässig nur
bei Vorliegen einer ausreichenden Rechtfertigung aufgrund eines sachlich angemessenen Grundes gegeben.
Schliesslich bestätigte das Bundesverwaltungsgericht auch, dass in Ausnahmefällen die Feststellung
eines nachteiligen Effekts für eine bestimmte Verknüpfung von separaten Produkten nicht möglich
sein werde. Wenn im Einzelfall entsprechende Anhaltspunkte vorlägen, sei in solchen Fällen
eine Abklärung durch die Wettbewerbsbehörden vorzunehmen (Urteil B-831/2011, SIX,
E. 1385-1402).
13.7.6 Das
Bundesgericht hielt im Urteil 2C_113/2017 vom 12. Februar 2020 i.S. Hallenstadion
fest, ein Koppelungsgeschäft sei kartellrechtlich relevant, wenn daraus eine Wettbewerbsbeschränkung
resultiere. Dies sei insbesondere einerseits dann gegeben, wenn das marktbeherrschende Unternehmen seine
Stellung ausnutze, um seine Lieferanten oder Abnehmer zur Belieferung bzw. Abnahme eines Gutes zu bewegen,
das sie gar nicht oder nicht zu den vom marktbeherrschenden Unternehmen vorgegebenen Geschäftsbedingungen
absetzen bzw. erwerben möchte. Andererseits sei dies der Fall, wenn das marktbeherrschende Unternehmen
seine Stellung missbrauche, um seine Marktmacht auf den Markt des gekoppelten Gutes, auf dem es bislang
nicht marktbeherrschend sei, zu übertragen. Das im Urteil 2C_113/2017 zu beurteilende strittige
Koppelungsgeschäft führe zu diesen beiden nachteiligen Wettbewerbseffekten. Ebenso werde durch
das Koppelungsgeschäft die beherrschende Stellung des marktbeherrschenden Unternehmens verstärkt,
was zu einer weiteren Strukturverschlechterung führe (Urteil 2C_113/2017, Hallenstadion,
E. 6.2.3 f.).
13.7.7 Die
Vorinstanz erwog, die Koppelungs- bzw. Bündelungsstrategie von HCI sei dauerhaft gewesen. Durch
die zusätzliche Bündelung mit der Qualitätssicherung sei es HCI möglich gewesen Konkurrenten,
die lediglich die Qualitätssicherung angeboten hätten, zu verdrängen bzw. deren Wettbewerbsstellung
zu verschlechtern. Zudem hätten auch die Zulassungsinhaberinnen die Qualitätssicherung bei
HCI beziehen müssen, auch wenn sie dies vielleicht gar nicht gewünscht hätten. Der Upload
der Arzneimittelinformationen auf AIPS habe zwar nicht zwangsläufig bei HCI bezogen werden müssen.
Da dieser kostenlos dazu angeboten worden sei, habe aber ein hoher ökonomischer Anreiz bestanden,
den Upload über HCI abzuwickeln, um Kosten zu sparen. Entsprechend verdränge die Koppelung
Konkurrenten, die den Upload auf AIPS anböten.
13.7.8 Weiter
erwog die Vorinstanz, es seien durch die Koppelung gleichzeitig auch Marktzutrittsschranken aufgebaut
worden, da ein potentieller Wettbewerber, der nur die Qualitätskontrolle und/oder nur den Upload
auf AIPS anbiete, auch in den nachgelagerten Markt der veredelten maschinenlesbaren Daten einsteigen
müsse, um HCI wirksam konkurrieren zu können. Aber auch die Zulassungsinhaberinnen würden
benachteiligt werden. Denn würden sie die Qualitätskontrolle selbst vornehmen oder einen Dritten
beauftragen, würde sich das ausschliesslich kostentreibend auswirken, da sie für die gleiche
Dienstleistung HCI erneut bezahlen müssten.
13.7.9 Die
Beschwerdeführerinnen sind der Auffassung, dass aus dem Urteil des Bundesverwaltungsgerichts B-3618/2013
vom 24. November 2016 i.S. Hallenstadion nicht per se von der
Unzulässigkeit einer Koppelung auf eine Wettbewerbsbeschränkung geschlossen werden dürfe.
Das Vorliegen einer Wettbewerbsbeschränkung müsse separat geprüft und eigenständig
nachgewiesen werden. Die Ausführungen des Bundesgerichts in BGE 139 I 72 und von David/Jacobs,
wonach die negativen Effekte - die Wettbewerbsbehinderung - festgestellt werden müssten,
würden auch für Koppelungsgeschäfte gelten. Dies decke sich auch mit der jüngeren
Rechtsprechung der EU.
13.7.10 Es
ist kein Grund ersichtlich von der noch jungen Rechtsprechung des Bundesverwaltungsgerichts in den Urteilen
B-3618/2013 i.S. Hallenstadion und B-831/2011 i.S. SIX
abzuweichen. Das Bundesgericht hat sich im Urteil 2C_113/2017 i.S. Hallenstadion
nicht explizit zu dieser Rechtsprechung geäussert. Entsprechend ist bei der Beurteilung eines Koppelungsgeschäftes,
wenn die Voraussetzungen der Marktbeherrschung und der Kombination von getrennten Produkten durch das
marktbeherrschende Unternehmen vorliegen, davon auszugehen, dass ein aus der Koppelung ergebender negativer
Effekt für die Marktgegenseite oder die Konkurrenten vorliegt, weil der Absatz des Zusatzprodukts
in derartigen Fällen nicht allein auf dessen originären Leistungsfaktoren beruht, sondern an
die Abnahme des Hauptprodukts anknüpft. Ausnahmsweise ist es aber möglich, dass für eine
bestimmte Kombination von separaten Produkten ein nachteiliger Effekt nicht festgestellt werden kann,
weshalb dann weder eine Ausbeutung der Marktgegenseite noch eine Behinderung von Konkurrenten gegeben
ist.
13.7.11 Das
bedeutet zwar nicht, dass die Ausbeutungs- und Behinderungswirkungen der Koppelung per se als gegeben
betrachtet werden können und im Einzelfall keine Abklärungen mehr notwendig sind. Vielmehr
kann bei dieser Ausgangslage eine summarische Prüfung als ausreichend angesehen werden, soweit dabei
keine Anhaltspunkte auszumachen sind, die darauf hindeuten würden, dass eine besondere Konstellation
von einer Kombination von separaten Produkten vorliegt, bei welcher kein nachteiliger Effekt festzustellen
ist.
13.7.12 Die
Erwägungen der Vorinstanz genügen diesen Anforderungen. Es ist mit der Vorinstanz davon auszugehen,
dass die Zulassungsinhaberinnen die Qualitätssicherung bei HCI beziehen mussten, auch wenn sie dies
gar nicht wünschten. Nach erfolgter Qualitätskontrolle im Rahmen des Zulassungsverfahren -
bestand unabhängig, ob die Zulassungsinhaberinnen diese Qualitätskontrolle selbst vornahmen
oder einen Dritten hierfür beauftragten - regelmässig kein Bedarf mehr auf Seiten der
Zulassungsinhaberinnen für eine erneute Qualitätskontrolle durch HCI. Die Erwägungen der
Vorinstanz sind auch insofern nicht zu beanstanden, als sie zum Schluss kommt, dass es durch die Bündelung
mit der Qualitätssicherung auch möglich war, Konkurrenten, die Qualitätssicherung anboten,
zu verdrängen bzw. deren Wettbewerbsstellung zu verschlechtern. Ebenso zutreffend hat die Vorinstanz
festgestellt, dass die Koppelung mit dem Upload auf AIPS Konkurrenten verdränge, die den Upload
auf AIPS ebenfalls anboten oder anbieten wollten.
13.7.13 Die
Beschwerdeführerinnen bringen im Zusammenhang mit der Verdrängung von Konkurrenten vor, die
meisten Zulassungsinhaberinnen würden den gesamten regulatorischen Bereich und nicht nur die Qualitätssicherung
oder den Upload an Dritte übertragen. Daraus lässt sich aber nichts zugunsten der Beschwerdeführerinnen
ableiten. Denn durch die zusätzliche Bündelung mit der Qualitätssicherung (mit Upload
auf AIPS) ist es HCI möglich Konkurrenten, die ebenfalls die Qualitätssicherung (mit Upload
auf AIPS) anbieten - auch wenn sie in der Regel weitere oder gar die gesamten Dienstleistungen
des regulatorischen Bereichs anbieten - , zu verdrängen bzw. deren Wettbewerbsstellung im
Bereich des (Teil)Angebots "Qualitätssicherung (mit optionalem Upload auf AIPS) " zu verschlechtern.
13.7.14 Weiter
bestreiten die Beschwerdeführerinnen die vorinstanzliche Begründung, wonach durch die Koppelung
Marktzutrittsschranken aufgebaut würden, weil ein potentieller Wettbewerber, der nur die Qualitätskontrolle
und/oder nur den Upload auf AIPS anbiete, auch in den nachgelagerten Markt der veredelten maschinenlesbaren
Daten einsteigen müsse, um HCI wirksam konkurrieren zu können. Zwar weisen sie dabei zutreffend
daraufhin, dass auf dem Schweizer Markt Unternehmen tätig sind, die die Zulassungsinhaberinnen bei
der Erstellung der Zulassungsdossier unterstützen und ebenfalls Qualitätssicherung anbieten
würden. Daraus kann jedoch nicht geschossen werden, dass durch die Koppelung keine Marktzutrittsschranken
aufgebaut wurden. Einem potentiellen Wettbewerber ist es aufgrund der Koppelung nicht möglich, HCI
wirksam zu konkurrieren, wenn er nur die Qualitätssicherung mit (optionalem) Upload auf AIPS anbietet.
Vielmehr muss ein Wettbewerber in den nachgelagerten Markt der veredelten maschinenlesbaren Daten einsteigen
oder in den Markt für Beratungs- und Unterstützungsdienstleistungen während des Zulassungsverfahrens
eintreten, so wie es die von den Beschwerdeführerinnen erwähnten Unternehmen getan haben.
13.7.15 Die
Koppelung war zudem dauerhaft und hat zu einer Zeit Wirkung entfaltet, als die Märkte sich potentiell
hätten entwickeln und öffnen können. Beide Faktoren erhöhen die Gefahr einer wettbewerbswidrigen
Marktverschliessung. Unter diesen Umständen und aufgrund der oben dargelegten Anforderungen an die
Prüfung des Vorliegens einer wettbewerbsbeschränkenden Wirkung hat die Vorinstanz eine solche
zu Recht bejaht, ohne weitere Erhebungen zu den Wirkungen mittels Fragebogen und Befragungen durchzuführen.
13.7.16 An
diesem Schluss vermögen im Übrigen auch die mit Eingabe vom 16. November 2018 gemachten Vorbringen
der Beschwerdeführerinnen, sie habe die als kartellrechtswidrig angesehenen Verhaltensweisen vorläufig
eingestellt, woraufhin sich die Wettbewerbsverhältnisse nicht geändert hätten, was zeige,
dass die Verhaltensweise auch im Untersuchungszeitraum keine Bedeutung gehabt habe, nichts ändern.
13.7.17 Denn
zum einen können aus dem späteren Verlauf unter anderen tatsächlichen Gegebenheiten -
gerade bei komplexen Märkten und in Zusammenhang mit Innovationswettbewerb - kaum aussagekräftige
Schlüsse für frühere Perioden gezogen werden. Zum anderen ist es bei der Verwirklichung
des Koppelungstatbestandes unerheblich, in welchem Ausmass die Zulassungsinhaberinnen ausgebeutet und
die Konkurrenten tatsächlich behindert wurden. Wie vorstehend ausgeführt setzt der Tatbestand
keine Überschreitung einer quantitativen Anwendungsschwelle voraus. Hinzukommt, dass Art. 7 KG -
wie vorne dargelegt - weder die Voraussetzung statuiert, dass nachteilige Einwirkungen auf den
Wettbewerb tatsächlich eintreten, noch die Voraussetzung, dass die konkreten tatsächlichen
Auswirkungen im Rahmen einer ex-post-Betrachtung zu berücksichtigen sind. Massgebend ist vielmehr
allein das Potential des jeweiligen wirtschaftlichen Verhaltens eines marktbeherrschenden Unternehmens
zur Herbeiführung einer weiteren Beeinträchtigung des Wettbewerbs, der aufgrund der Stellung
des marktbeherrschenden Unternehmens bereits geschwächt ist (Urteil B-831/2011, SIX,
E. 1406).
13.7.18 Soweit
die weiteren Vorbringen der Beschwerdeführerinnen die geltend gemachten Effizienzgewinne betreffen,
ist auf diese bei der Prüfung von sachlichen Rechtfertigungsgründe unter E. 13.8
einzugehen.
13.8 Sachliche
Rechtfertigungsgründe
13.8.1 Eine
Verbindung von verschiedenen Produkten kann anerkanntermassen nicht nur nachteilige Auswirkungen auf
die Wahlfreiheit der Vertragspartner des marktbeherrschenden Unternehmens aufweisen, sondern allenfalls
auch wünschenswerte Wirkungen entfalten, die bei einer gesamthaften Betrachtung des Einzelfalls
sogar zu einer positiven Beurteilung der jeweiligen Verbindung führen. Es bedarf daher einer Abgrenzung
von nachteiligen Koppelungsgeschäften gegenüber vorteilhaften Kombinationsgeschäften (Urteil
B-831/2011, SIX, E. 1415).
13.8.2 Ein
Koppelungsgeschäft ist zulässig, wenn es durch sachliche Gründe gerechtfertigt werden
kann. Solche Gründe liegen dann vor, wenn objektiv überzeugende, zwingende technische oder
wirtschaftliche Gründe oder gewisse Erfordernisse der Qualitätssicherung für die Zusammenfassung
des betreffenden Leistungsangebotes sprechen. Auch Sicherheitsaspekte werden als sachliche Rechtfertigungsgründe
angeführt (Botschaft KG, BBl 1995 I 468, 576; RPW 2014/4 S. 670 ff. Rz. 207, Preispolitik
und andere Verhaltensweisen der SDA; RPW 2005/1 S. 46 ff. Rz. 54, TopCard-Angebot
der Bergbahnen Lenzerheide-Valbella, Klosters-Davos und Flims-Laax-Falera; Borer,
a.a.O., Art. 7 Rz. 27; Weber/Volz, a.a.O., Rz. 2770; Stäuble/Schraner,
DIKE-KG, Art. 7 N 505; Amstutz/Carron, BSK-KG, Art. 7 N
777).
13.8.3 Nach
Zäch und Amstutz/Carron
können sachliche Rechtfertigungsgründe zudem gegeben sein, wenn es um die Verbrauchersicherheit,
die öffentliche Gesundheit, den Schutz der Anwender oder das Anliegen, eine Produkthaftpflicht zu
vermeiden geht (Amstutz/Carron, BSK-KG, Art. 7 N 777; Zäch,
a.a.O., Rz. 708).
13.8.4 Im
Weiteren kann ein allenfalls bestehender Handelsbrauch für die gemeinsame Vermarktung der betreffenden
Leistungen sprechen. Dieser sollte jedoch nicht vom Marktbeherrscher allein begründet worden sein
(Botschaft KG, BBl 1995 I 468, 576; Weber/Volz, a.a.O.,
Rz. 2.772, Stäuble/Schraner, DIKE-KG, Art. 7 N 506;
Amstutz/Carron, BSK-KG, Art. 7 N 777). Problematisch erscheint,
dass dieses Kriterium vergangenheitsbezogen ist und dadurch unter Umständen sinnvolle technologische
Innovationen und neue Produktintegrationen behindert werden, weil es sich auf frühere Geschehnisse
zurückbezieht (Weber/Volz, a.a.O., Rz. 2.772).
Eine Rechtfertigung ist auch dann nicht möglich, wenn der Handelsbrauch zur weiteren Beschränkung
des Wettbewerbs auf einem beherrschten Markt führt (Stäuble/Schraner,
DIKE-KG, Art. 7 N 506).
13.8.5 Einfache
praktische Gründe, die zwar eine bessere Praktikabilität gewährleisten, genügen nicht
(Amstutz/Carron, BSK-KG, Art. 7 N 777 m.w.H.).
13.8.6 Zur
Frage, ob und inwieweit auch wirtschaftliche Aspekte, insbesondere in Form einer Einsparung von Produktions-,
Vertriebs- und Transaktionskosten, als Rechtsfertigungsgrund für ein Koppelungsgeschäft anzuerkennen
sind, stellte das Bundesverwaltungsgericht im Urteil B-3618/2013 vom 24. November 2016 i.S. Hallenstadion
fest, dass dies bislang nicht abschliessend geklärt wurde. Der Bundesrat verweise in der Botschaft
nur auf "zwingende wirtschaftliche" Gründe. Bei der Verfügung der WEKO vom 7. Juli
2008 i.S. Publikation von Arzneimittelinformationen sei nicht
ersichtlich, ob die geringfügige Kosteneinsparung als Rechtfertigungsgrund zu gelten habe oder ob
angesichts der Notwendigkeit zur Vornahme gewisser Korrekturen bei jeglicher Publikation die entsprechenden
Arbeiten überhaupt das Ausmass selbständiger Korrekturarbeiten angenommen hätten. Von
der Lehre werde der Rechtfertigungsgrund der Effizienzgewinn teilweise grundsätzlich anerkannt;
ebenso im europäischen Wettbewerbsrecht (Urteil B-3618/2013, Hallenstadion,
E. 266 m.H. Botschaft KG, BBl 1995 I 468, 576; RPW 2008/3 S. 385 ff., Rz. 203 f., Publikation
von Arzneimittelinformationen; Amstutz/Carron, BSK-KG,
Art. 7 N 778; Weber/Volz, a.a.O., Rz. 2.770; Fuchs/Möschel,
a.a.O., Art. 102 Rz. 293; Ziff. 62 der Prioritätenmitteilung).
Weiter schloss das Bundverwaltungsgericht im Urteil B-3618/2013 vom 24. November 2016 i.S. Hallenstadion,
der blosse Umstand, dass ein marktbeherrschendes Unternehmen das Zusatzprodukt aus Sicht der Marktgegenseite
günstiger anbiete, sei jedenfalls nicht ausreichend, weil insoweit auch eine verdeckte Quersubventionierung
durch das marktbeherrschende Unternehmen zu Lasten der Konkurrenten auf dem Markt der Zusatzprodukte
vorliegen könne. Eine entsprechende Quersubventionierung von dem vom Unternehmen beherrschten Markt
des Hauptprodukts zu dem vom Unternehmen (noch) nicht beherrschten Markt des Zusatzprodukts müsse
zum Schutz der Konkurrenten auf dem Markt des Zusatzprodukts ausgeschlossen werden (Urteil B-3618/2013,
Hallenstadion, E. 266 m.H. auf Ziff. 60 der Prioritätenmitteilung,
wonach bei einer preisbezogenen Anreizkopplung die Preise für beide Produkte über den durchschnittlichen
langfristigen Zusatzkosten liegen müssen).
13.8.7 Das
Bundesgericht liess im Urteil 2C_985/2015 vom 9. Dezember 2019 i.S. ADSL
II die Frage, ob Effizienzgründe geltend gemacht und berücksichtigt werden können,
weiterhin offen. Unabhängig davon gelte, dass durch möglicherweise rechtfertigendes Verhalten
wirksamer Wettbewerb nicht beseitigt werden dürfe (Urteil 2C_985/2015, ADSL
II, E. 5.9).
13.8.8 Jede
Rechtfertigung muss dem Gebot der Verhältnismässigkeit entsprechen (Amstutz/Carron,
BSK-KG, Art. 7 N 779; Weber/Volz, a.a.O., Rz. 2.773; Clerc/Këllezi,
CR-Concurrence, Art. 7 II N 282; Stäuble/Schraner,
DIKE-KG, Art. 7 N 510 f.). Notwendig ist ein Verhalten nur dann, wenn sich der bezweckte Erfolg nicht
auf anderem, weniger wettbewerbsfeindlichem Weg erzielen lässt (Urteil 2C_985/2015, ADSL
II, E. 5.9).
13.8.9 Die
Beschwerdeführerinnen brachten vor der Vorinstanz vor, das Compendium und die INDEX-Datenbank würden
äusserst sensitive Daten (Patientensicherheit) enthalten, für deren Korrektheit HCI ihren Vertragspartnern
gegenüber Gewähr leiste. Dies mache es unabdingbar, dass HCI bei jeder Aufnahme von Fach- und
Patienteninformationen sich selber von deren Korrektheit und Vollständigkeit überzeugen müsse.
Eine entsprechende redaktionelle und technische Qualitätssicherung gehöre zu den grundlegenden
Anforderungen an eine sorgfältige und verantwortungsbewusste Leistungserbringung. Damit sei auch
der Erfolg der Daten von HCI zu erklären.
13.8.10 Die
Vorinstanz erwog, in der Untersuchung Publikation von
Arzneimittelinformationen sei zwar argumentiert worden, dass die Korrekturarbeiten im Vergleich
zu den Standardprozesskosten vernachlässigbar tief seien und eine Trennung der Dienstleistung wahrscheinlich
insgesamt zu höheren Kosten führen würde. Vorliegend sei der Sachverhalt jedoch ein anderer,
da es sich nicht um die gesetzlich vorgesehene Publikation handle, sondern um die Aufnahme in eine Datenbank
eines Datenveredlers, zu welcher die Zulassungsinhaberinnen nicht durch gesetzliche oder regulatorische
Vorgaben verpflichtet seien. Daher sei es irrelevant, ob die redaktionelle und technische Qualitätssicherung
bloss einen vernachlässigbaren Teil der Kosten ausmache. Nach erfolgter Publikation bestehe keine
Nachfrage nach einer erneuten Kontrolle der Arzneimittelinformationen.
13.8.11 Weiter
prüfte die Vorinstanz, ob die redaktionelle und technische Qualitätskontrolle zu Effizienzgewinnen
führe oder die Verdrängungseffekte überwiegen. Dabei erwog sie, die Strukturierung und
die Codierung sei in einem logischen, engen Zusammenhang mit der Aufnahme der Daten in die Datenbank
verbunden, die redaktionelle und technische Qualitätskontrolle hingegen nicht zwingend vorzunehmen.
Die Arzneimittelinformationen könnten ohne weitere Kontrolle aus AIPS aufgenommen, in die entsprechende
Struktur gebracht und codiert werden. Für die redaktionelle und technische Qualitätskontrolle
sei ein zusätzlicher Arbeitsschritt zu erbringen, der unabhängig von der Aufnahme in die Datenbank
bestehe. Eine weitere Qualitätskontrolle sei aber nicht im Interesse der Zulassungsinhaberinnen,
da diese potentiell eine solche Dienstleistung bereits eingekauft oder selbst entsprechende Aufwände
gehabt hätten.
13.8.12 Die
Beschwerdeführerinnen wiederholen die vor der Vorinstanz vorgebrachten Rechtfertigungsgründe
im vorliegenden Verfahren und rügen, die Vorinstanz habe sich inhaltlich nicht mit diesen auseinandergesetzt.
Die Validierung der Arzneimittelinformationen bilde einen zentralen Erfolgsfaktor für das Angebot
von HCI. Durch die Überprüfung sei HCI in der Lage, regelmässig Fehler in den von den
Zulassungsinhaberinnen gelieferten Daten zu korrigieren. Damit verhindere sie folgenschwere Medikationsfehler
und leiste einen Beitrag für die Patientensicherheit. Die geltend gemachten Gründe seien anerkannte
legitimate bussiness reasons.
13.8.13 Nach
erfolgter Publikation besteht kein Bedarf nach einer erneuten Kontrolle der Arzneimittelinformationen.
Dies gilt auch mit Blick auf die geltend gemachten Rechtfertigungsgründe der Patientensicherheit
bzw. des Verbraucherschutzes und der öffentlichen Gesundheit. Diesen Interessen wird bereits durch
die gesetzlich vorgesehene Qualitätskontrolle vor der Publikation der Arzneimittelinformationen
Rechnung getragen. Entsprechend lässt sich eine erneute Qualitätskontrolle, die an die Aufnahme
in die Datenbanken der HCI gekoppelt wird, nicht mit Gründen der Patientensicherheit rechtfertigen.
Die Qualitätskontrolle im Hinblick auf die Publikation muss nicht zwingend mit derjenigen eines
Datenveredlers im Hinblick auf sein eigenes Produkt erfolgen. Sollten nachträglich in vielen Arzneimittelinformationen
noch Fehler gefunden werden, die folgenschwere Medikationsfehler verursachen können, wäre es
viel mehr geboten, die Qualitätskontrolle im Hinblick auf die Publikation der Arzneimittelinformationen
zu verbessern. Denn auch Fehler in den Fach- und Patienteninformationen auf AIPS und in den Beipackzettel
können zu solchen Medikationsfehlern führen.
13.8.14 Im
Übrigen bringen die Beschwerdeführerinnen zwar vor, das Compendium und die INDEX-Datenbank
würden äusserst sensitive Daten enthalten, für deren Korrektheit HCI ihren Vertragspartnern
gegenüber Gewähr leiste. Eine Datenbank ohne Qualitätssicherung würde die Nachfrage
der Leistungserbringerinnen und -erbringer nicht befriedigen. Die Beschwerdeführerinnen belegen
jedoch nicht, dass sie gegenüber ihren Vertragspartnern eine Haftung übernehmen, wenn in ihrer
Datenbank Fehler vorhanden sind, die durch fehlerhafte Arzneimittelinformationen auf AIPS oder durch
Fehler in den durch die Zulassungsinhaberinnen übermittelten Arzneimittelinformationen entstanden
sind. Vielmehr finden sich in den Akten gegenteilige Vertragsbestimmungen, wie beispielsweise im Vertrag
betreffend Zusammenarbeit und Vertrieb mit der D._______ vom 16. bzw. 26. Februar 2007 (vgl. Vorinstanz,
act. 616 und Beilage zu act. 1120):
"8. Haftung
und Qualitätssicherung
e-mediat stellt die von ihr erstellten Datenbanken und Webservices mit
grösstmöglicher Qualität zur Verfügung. In diesem Zusammenhang haftet e-mediat nur
im Rahmen ihrer allgemeinen Geschäftsbedingungen, bzw. der Lizenzbestimmungen mit den Endnutzern
der Datenbankprodukte. Weitergehende Ansprüche werden sowohl gegenüber [...] als auch deren
Kunden soweit als gesetzlich möglich wegbedungen Diese Haftungsbestimmungen sind integraler Bestandteil
der Lizenzbedingungen zwischen e-mediat und ihren Lizenznehmern und gelten sinngemäss auch gegenüber
[...]. [...] verpflichtet sich, in ihren Kunden-Verträgen explizit auf diese Bedingungen
zu verweisen, bzw. ihren Kunden zu überbinden.
[...]"
In den allgemeinen Geschäftsbedingungen (vgl. Vorinstanz, act. 616, S. 26 ff., 28)
finden sich in Ziffer 8 sodann die folgenden Bestimmungen:
"8. Gewährleistung
8.1 e-mediat verpflichtet sich, ihre Leistungen sorgfältig zu erbringen,
sie übernimmt jedoch, vorbehältlich ausdrücklich abweichender Vereinbarung im Vertrag,
keine Erfolgshaftung. Sie gewährleistet nicht, dass die Nutzung ihrer Leistungen ohne Fehler und
ohne Unterbruch möglich ist. [...]
8.2 [...]
8.3 Soweit die Leistungen von e-mediat Informationen des Kunden oder
Dritter zum Gegenstand haben, übernimmt e-mediat keine Gewähr für den Inhalt dieser Informationen
und ist nicht verpflichtet, diesen zu überprüfen. Die Verantwortung und Haftung für den
Inhalt solcher Informationen liegt ausschliesslich beim Kunden und den betreffenden Dritten."
Als weiteres Beispiel kann ein Lizenzvertrag vom 8. bzw. 9. September 2011 betreffend
Nutzung von
Daten für Grossisten (logINDEX) angeführt werden (vgl. Vorinstanz, act. 590, S. 6 ff.). In
dessen Ziffer 14 wird vereinbart, dass technische und/oder inhaltliche Fehler und Lücken der gelieferten
Daten vom Grossisten rasch möglichst an e-mediat zu melden seien und diese sodann von e-mediat berichtigt
oder bei der nächsten Aktualisierung bereinigt werden. Weitergehende Garantien und Gewährleistungsrechte
wurden ausgeschlossen. Ebenso wurden in Ziffer 15 sämtliche Ansprüche (ausser den in Ziffer
14 genannten) ausgeschlossen, "soweit einem solchen Haftungsausschluss nicht zwingende Gesetzesbestimmungen
entgegenstehen". Eine ähnliche Regelung findet sich sodann beispielsweise auch in einem Lizenzvertrag
über den Vertrieb von Dienstleistungen an Endkunden für Softwarehäuser vom 8. bzw. 9.
September 2011 (vgl. Vorinstanz, act. 608, S. 4 ff.). Gemäss Ziffer 7 des Lizenzvertrages ist das
Softwarehaus verpflichtet, "mit jedem Endkunden, an welchen es ein Dienstleistungspaket weitergibt,
in eigenem Namen eine Vereinbarung über die Nutzung gemäss Beilage 2 zu diesem Vertrag abzuschliessen".
In dieser "Beilage 2 Nutzungsbedingungen" findet sich sodann nachfolgende ähnliche Vertragsbestimmung:
3. [...] Inhaltliche Fehler und Lücken der Daten sind vom Benützer
raschmöglichst dem Lizenzgeber zu melden und werden bei der nächsten Aktualisierung der Datendienstleistungen
[...] bereinigt. Weitergehende Garantien und Gewährleistungsrechte bestehen nicht und werden
hiermit ausgeschlossen. [...]
Es finden sich in den Akten somit zahlreiche Verträge mit Softwarehäuser, die Vertragsbestimmungen
enthalten, die solche Haftungs- und Gewährleistungsansprüche explizit ausschliessen.
13.8.15 Schliesslich
machen die Beschwerdeführerinnen geltend, die Vorinstanz habe in der angefochtenen Verfügung
selber ausgeführt, der Umstand, dass HCI an sich selbst den Anspruch habe, unabhängig vom Vorprozess
ihrerseits die Arzneimittelinformationen nochmals auf Richtigkeit zu überprüfen stelle ein
legitimer geschäftspolitischer Entscheid dar. Nach der Auffassung der Beschwerdeführerinnen
kann damit nichts Anderes gemeint sein als ein legitimate business reason. Dies trifft jedoch nicht zu.
So hat die Vorinstanz explizit festgehalten, dass dieser "legitime geschäftspolitische Entscheid"
indes keinen Rechtfertigungsgrund begründe.
13.8.16 Die
Vorbringen der Beschwerdeführerinnen im Zusammenhang mit der Patientensicherheit verfangen demnach
nicht.
13.8.17 Nach
den Erwägungen der Vorinstanz ist es denkbar, dass der Upload auf AIPS mit geringen Kosten verbunden
ist. Trotzdem würden die Verdrängungswirkungen überwiegen. Es werde der ökonomische
Druck für die Aufnahme in die INDEX-Daten verwendet, um konkurrierende Anbieter der Dienstleistung
des Uploads der Arzneimittelinformationen auf AIPS zu verdrängen.
13.8.18 Die
Beschwerdeführerinnen stellen sich demgegenüber auf den Standpunkt, der Upload sei als unentgeltliche
Zusatzleistung durch Effizienzgründe gerechtfertigt. Diese Leistung werde nur mit marginalem Zusatzaufwand
erbracht. Die Praxis sei mit der in der Verfügung der Vorinstanz vom 7. Juli 2008 in Sachen Publikation
von Arzneimittelinformationen (RPW 2008/3 S. 385 ff.) beurteilten früheren Korrekturarbeitspraxis
vergleichbar, welche als aus Effizienzgründen gerechtfertigt beurteilt worden sei. Schliesslich
halte die Vorinstanz selbst fest, möglicherweise sei der Upload mit geringen Kosten verbunden und
begründe nicht, weshalb vorliegend die Verdrängungswirkungen überwiegen sollten.
13.8.19 In
der Untersuchung Publikation von Arzneimittelinformationen hat
die WEKO argumentiert, die Korrekturarbeiten seien im Vergleich zu den Standardprozesskosten vernachlässigbar
tief und eine Trennung der Dienstleistungen führe wahrscheinlich insgesamt zu höheren Kosten.
Eine ähnliche Argumentation wäre allenfalls auch vorliegend hinsichtlich des Uploads auf AIPS
denkbar. Wie bereits von der Vorinstanz festgestellt, unterscheidet sich der Sachverhalt aber insofern,
als es sich vorliegend bei der gebündelten Dienstleistung (Aufnahme in die Datenbank der HCI) nicht
um eine gesetzlich oder regulatorisch vorgesehene Publikation handelt. Ausserdem wird eine Rechtfertigung
aus Effizienzgründen beim blossen Umstand, dass ein marktbeherrschendes Unternehmen das Zusatzprodukt
aus Sicht der Marktgegenseite günstiger anbietet, nicht anerkannt. Denn in diesem Fällen kann
auch eine verdeckte Quersubventionierung durch das marktbeherrschende Unternehmen zu Lasten der Konkurrenten
auf dem Markt der Zusatzprodukte vorliegen, welche zum Schutz der Konkurrenten auf dem Markt des Zusatzprodukts
ausgeschlossen werden muss (s. oben E. 13.8.6).
13.8.20 Die
geltend gemachte Rechtfertigung aus Effizienzgründen in Bezug auf den Upload auf AIPS verfängt
somit nicht. Das Argument der marginalen Zusatzkosten und der noch im Jahr 2008 zulässigen Koppelung
im regulierten Bereich ist im Übrigen - wie von der Vorinstanz zutreffend festgehalten und
von den Beschwerdeführerinnen im Beschwerdeverfahren auch nicht beanstandet - auch in Bezug
auf die Qualitätskontrolle nicht stichhaltig.
13.8.21 Andere
Rechtfertigungsgründe wurden weder geltend gemacht noch sind solche ersichtlich.
13.9 Fazit
Als Ergebnis der Prüfung im Beschwerdeverfahren ist festzustellen, dass die vorgenommene Koppelung
der Qualitätssicherung und des Uploads auf AIPS mit der Aufnahme in das Kompendium und die INDEX-Daten
ein wettbewerbswidriges Verhalten in der Missbrauchsform einer Koppelung gemäss Art. 7 Abs. 1 i.V.m.
Abs. 2 Bst. f KG darstellt.
14. Massnahmen
14.1 Die
Vorinstanz erwog, bei Vorliegen einer unzulässigen Wettbewerbsbeschränkung könnten Massnahmen
zu deren Beseitigung angeordnet werden, indem den betroffenen Parteien die sanktionsbewehrte Pflicht
zu einem bestimmten Tun oder Unterlassen auferlegt werde. Sie verfügte daher als Massnahme, dass
es Galenica und HCI untersagt werde, in ihren Verträgen mit den Softwarehäusern Vertragsklauseln
zu verwenden und durchzusetzen, die eine Alleinbezugspflicht der Softwarehäuser für zusätzliche
Partner und Produkt-Stamm-Daten bei HCI oder eine Untersagung der anderweitigen Verwendung der Strukturen
der auf der Datenbank der Galenica-Gruppe beruhenden Software für die Softwarehäuser vorsehen
(Ziffer 2 der angefochtenen Verfügung). Weiter verfügte die Vorinstanz als Massnahme, dass
Galenica und HCI verpflichtet werden, den Zulassungsinhaberinnen die Dienstleistung der Aufnahme der
Medikamenteninformationen in die Indices und andere Dienstleistungen entbündelt anzubieten. Galenica
und HCI wurden verpflichtet, die redaktionelle und technische Qualitätskontrolle der Arzneimittelinformationen
sowie den Upload der Arzneimittelinformationen auf AIPS zu kostenbasierten Preisen anzubieten (Ziffer
3 der angefochtenen Verfügung).
14.2 Die
Beschwerdeführerinnen beantragen die Aufhebung der Ziffern 2 und 3 der angefochtenen Verfügung,
dies jedoch mit der Begründung, dass die fraglichen Verhaltensweisen keine unzulässigen Verhaltensweisen
i.S.v. Art. 7 Abs. 1 i.V.m. Abs. 2 Bst. e und f KG seien. Darüber hinaus bringen sie vor, die Beschwerdeführerin
1 sei infolge der Umstrukturierungen nicht mehr die Muttergesellschaft der Beschwerdeführerin 2.
Die Beschwerdeführerin 1 sei nicht mehr im Vertrieb und Verkauf von Arzneimitteln in der Schweiz
tätig, sondern international ausgerichtet und stelle insbesondere Eisenpräparate her. Daher
mache es keinen Sinn, ihr Verhaltensvorschriften aufzuerlegen, die keinen Zusammenhang zu ihr aufweisen
würden.
14.3 Kommt
die WEKO zur Überzeugung, dass in einem konkreten Fall eine unzulässige Wettbewerbsbeschränkung
i.S.v. Art. 5 oder 7 KG vorliegt, und will sie Massnahmen anordnen, so stellt sie zunächst fest,
dass ein Unternehmen an einer solchen beteiligt war bzw. diese verursacht hat. Zur Beseitigung dieser
Beschränkung kann die WEKO Massnahmen anordnen, indem sie den betroffenen Parteien die Pflicht zu
einem bestimmten Tun oder Unterlassen auferlegt (Izumi/Krimmer,
DIKE-KG, Art. 30 N 24; Zirlick/Tagmann, BSK-KG, Art.
30 N 58 und 59). Beim Begriff der Massnahmen handelt es sich um einen unbestimmten Rechtsbegriff der
im Einzelfall durch die Anwendung des materiellen Kartellrechts zu konkretisieren ist (Stefan
Bilger, Das Verwaltungsverfahren zur Untersuchung von Wettbewerbsbeschränkungen, 2002, S.
359). Es besteht kein numerus clausus der möglichen Massnahmen (Bilger,
a.a.O., S. 359 f.; Izumi/Krimmer, DIKE-KG, Art. 30 N 25).
Die zutreffenden Massnahmen sind abhängig von der Art und Intensität der als unzulässig
festgestellten Wettbewerbsbeschränkung. Die Massnahmen müssen geeignet und notwendig sein,
um die festgestellten Wettbewerbsbeschränkungen zu beseitigen (Bilger,
a.a.O., S. 359 f; Izumi/Krimmer, DIKE-KG, Art. 30 N 25;
Zirlick/Tagmann, BSK-KG, Art. 30 N 59).
14.4 Die
von der WEKO angeordneten Massnahmen zu einem bestimmten Tun oder Unterlassen sind sanktionsbewehrt i.S.v.
Art. 50 und 54 KG
(Izumi/Krimmer, DIKE-KG,
Art. 30 N 25; Zirlick/Tagmann, BSK-KG, Art. 30 N 58).
Materiell handelt es sich bei solchen behördlichen Anordnungen um Gestaltungsverfügungen (Bilger,
a.a.O., S. 360; Zirlick/Tagmann, BSK-KG, Art. 30 N 59 und
59b).
14.5 Die
vorliegend beurteilten Verhaltensweisen stellen unzulässige Verhaltensweisen i.S.v. Art. 7 Abs.
1 i.V.m. Abs. 2 Bst. e und f KG dar. Der Antrag auf Aufhebung der Ziffern 2 und 3 der vorinstanzlichen
Verfügung wegen Nichtvorliegens von unzulässigen Verhaltensweisen ist somit abzuweisen. Die
Massnahmen in Ziffer 2 und 3 der angefochtenen Verfügung erscheinen genügend präzis formuliert
sowie geeignet und notwendig, um die unzulässigen Wettbewerbsbeschränkungen zu beseitigen.
Die Beschwerdeführerinnen bringen im Beschwerdeverfahren zwar vor, ihre Verhaltensweisen unterdessen
angepasst zu haben und die Wettbewerbsbeschränkungen beseitigt zu haben. An den angeordneten Massnahmen
gemäss Ziffer 2 und 3 ist jedoch hinsichtlich zukünftig möglichen Verhaltensänderungen
dennoch festzuhalten.
14.6 Die
Beschwerdeführerin 1 ist in infolge der Umstrukturierungen nicht mehr die Muttergesellschaft der
Beschwerdeführerin 2. Die Beschwerdeführerin 1 hat somit keine Kontroll- und Einflussmöglichkeiten
mehr auf die Beschwerdeführerin 2. Die Beschwerdeführerin 1 ist auch nicht mehr im Bereich
Vertrieb und Verkauf von Arzneimitteln tätig. Da es sich bei den Massnahmen von Ziffern 2 und 3
des vorinstanzlichen Dispositivs um i.S.v. Art. 50 und 54 KG sanktionsbewehrte Massnahmen handelt, die
Beschwerdeführerin 1 aber weder im fraglichen Bereich tätig ist, noch Kontroll- und Einflussmöglichkeiten
auf die Beschwerdeführerin 2 hat, erscheint es angezeigt, diese in die Zukunft gerichteten Massnahmen
nur der Beschwerdeführerin 2 aufzuerlegen, auch wenn beide Beschwerdeführerinnen als Adressatinnen
der Sanktionsverfügung qualifiziert wurden (s. oben E. 3,
insb. E. 3.18
f.).
15. Sanktionierung
Art. 49a Abs. 1 KG sieht vor, dass ein Unternehmen, das an einer unzulässigen Abrede nach Art.
5 Abs. 3 und 4 KG beteiligt ist oder sich nach Art. 7 KG unzulässig verhält, mit einer Sanktion
belastet wird. In casu liegt ein Missbrauch von Marktmacht durch Einschränkung des Absatzes i.S.v. Art. 7
Abs.1 i.V.m. Art. 7 Abs. 2 Bst. e KG und durch Koppelung i.S.v. Art. 7 Abs. 1 i.V.m. Art. 7 Abs.
2 Bst. f KG vor.
Die Vorinstanz hat gegen die Beschwerdeführerinnen eine Busse in der Höhe von Fr. 4'546'123.-
ausgesprochen.
15.1 Vorwerfbarkeit
15.1.1 Eine Sanktionierung
nach Art. 49a Abs. 1 KG setzt ein Verschulden im Sinne von Vorwerfbarkeit voraus. Dieses
stellt das subjektive Tatbestandsmerkmal von Art. 49a Abs. 1 KG dar (Urteile 2C.484/2010, Publigroupe,
E. 12.2.2 [nicht publizierte Erwägung in BGE 139 I 72];
B-771/2012, Cellere,
E. 9.3.1; B-506/2010, Gaba, E. 14.3.5; B-581/2012,
Nikon, E. 8.2; B-7633/2009,
ADSL II, Rz. 654 ff.).
15.1.2
Dem Unternehmen muss zumindest eine objektive Sorgfaltspflichtverletzung
im Sinne eines Organisationsverschulden angelastetet werden können (Urteile
2C_985/2015, ADSL II, E. 8.5.2; 2C_484/2010, Publigroupe,
E.12.2.2 [nicht publizierte Erwägung in BGE 139 I 72]; Weber/Volz,
a.a.O., Rz. 3.220; Krauskopf, DIKE-KG,
Art. 49a Abs. 1-2 N 26). Bei der Abklärung eines Organisationsmangels wird geprüft, was
das Unternehmen bei richtiger Organisation hätte wissen bzw. welche Handlungen es hätte verhindern
müssen. Fehlte das notwendige Wissen bzw. war es dem Unternehmen nicht verfügbar, wäre
es aber bei pflichtgemässer Organisation verfügbar gewesen, besteht ein Organisationsmangel
(Niggli/Riedo, BSK-KG, vor Art. 49a-53 N 132). Muss einem Unternehmen bzw.
den Organen aufgrund der Umstände bewusst sein, dass ein Verhalten heikel ist und eine Sanktionierung
droht, und sieht es gleichwohl nicht von seiner Verhaltensweise ab, liegt regelmässig ein solcher
Mangel vor (Krauskopf, DIKE-KG, Art. 49a Abs. 1-2 N 26).
15.1.3 Die
Vorinstanz erwog, der ehemaligen Galenica-Gruppe sei mehr als ein blosser Organisationsmangel vorzuwerfen,
es liege ein zumindest eventualvorsätzlicher Kartellrechtsverstoss vor. Bei der ehemaligen Galenica-Gruppe
seien tatsächliche Kenntnisse des Kartellgesetzes vorhanden gewesen, da sie bereits wiederholt in
kartellrechtliche Verfahren involviert gewesen sei. Zur Zeit der Festlegung der Strategie zur Umsetzung
der Änderung der regulatorischen Rahmenbedingungen sei überdies bereits die Vorabklärung
i.S. Medikamentenvertrieb in der Schweiz am Laufen gewesen. Noch im Dezember 2011 und damit vor Einführung
des Leistungskataloges 2013 sei e-mediat im Rahmen dieser Vorabklärung ein Auskunftsbegehren zugestellt
worden. Schliesslich sei zu einem früheren Zeitpunkt betreffend den Vertrieb der Datenbank eine
Ausstiegsklausel für Softwarehäuser eingebaut worden, falls die WEKO eingreifen sollte.
15.1.4 Weiter
erwog die Vorinstanz, die ehemalige Galenica-Gruppe habe sich auch ihrer marktbeherrschenden Stellung
auf beiden abgegrenzten Märkten bewusst sein müssen. Der Markt, auf welchem sie mit Verfügung
vom 7. Juli 2008 festgestellt habe, dass Documed eine marktbeherrschende Stellung habe, sei dem hier
zu beurteilenden Markt benachbart. Weiter habe die ehemalige Galenica-Gruppe gewusst, dass Galdat lange
Zeit das einzige Produkt auf dem entsprechenden Markt gewesen sei und bei der Offertstellung im Jahr
2012 sei sie von einer Marktabdeckung von mehr als 90% ausgegangen. Entsprechend habe sich die ehemalige
Galenica-Gruppe während der Festlegung der Strategie möglicher kartellrechtlich unzulässiger
Verhaltensweisen bewusst sein müssen und habe solche zumindest billigend in Kauf genommen. Auch
nach der Eröffnung der Untersuchung habe die ehemalige Galenica-Gruppe ihr Verhalten nicht eingestellt,
obwohl ihr durch die Untersuchungseröffnung eine mögliche kartellrechtliche Problematik erneut
ins Gedächtnis gerufen worden sei. Somit habe sie während der gesamten Zeit die mögliche
Kartellrechtwidrigkeit der verschiedenen Verhaltensweisen zumindest billigend in Kauf genommen.
15.1.5 Die
Beschwerdeführerinnen bestreiten, dass sie ein Verschulden am Kartellrechtsverstoss treffe. Sie
bringen vor, im Zusammenhang mit dem früheren Kartellrechtsverfahren gegen Documed und dem Vorwurf
der Koppelung sei die Erfüllung des Tatbestandes nicht vorhersehbar gewesen. Denn in der Verfügung
der Vorinstanz vom 7. Juli 2008 seien die Qualitätssicherung und die Publikation gerade nicht als
Koppelung qualifiziert worden. Weshalb dies vorliegend anders sein solle und für HCI habe ersichtlich
sein müssen, sei unklar und könne ihnen nicht vorgeworfen werden. Zudem habe im Schreiben des
Sekretariates vom 6. Dezember 2012, mit welchem ihnen die Untersuchungseröffnung mitgeteilt worden
sei, der Vorwurf der unzulässigen Koppelung von Leistungen noch nicht bestanden. Auch hätten
sie das Sekretariat um Beratung ersucht, was jedoch abgelehnt worden sei. Für sie sei es nicht einleuchtend,
weshalb eine Beratung nach Art. 23 KG nicht hätte offenstehen sollen, zumal es bei den dem Sekretariat
zugesandten Verträgen um die Ausgestaltung der künftigen Vertragsverhältnisse und damit
um künftige Verhaltensweisen gegangen sei. Auch werde bestritten, dass eine Prüfung der Verträge
durch das Sekretariat aufgrund der Komplexität und der Kurzfristigkeit nicht möglich gewesen
wäre. Denn die Verträge seien dem Sekretariat im Juni 2012 angekündigt und am 11. September
2012 eingereicht worden. Schliesslich sei es widersprüchlich, wenn die Prüfung der Verträge
als zu komplex qualifiziert werde, aber gleichzeitig ein offensichtlicher objektiver Sorgfaltsmangel
angenommen werde.
15.1.6 Weiter
bringen die Beschwerdeführerinnen vor, der Verweis auf die Fortführung des Verhaltens nach
den Vorabklärungen bzw. der Untersuchungseröffnung sei für die Begründung der Vorwerfbarkeit
nicht ausreichend. Denn weder die Vorabklärungen noch die Untersuchungseröffnung könnten
mit der Untersagung des betreffenden wirtschaftlichen Verhaltens gleichgesetzt werden. Eine eventualvorsätzliche
Kartellrechtsverletzung falle somit ausser Betracht und Fahrlässigkeit oder ein Organisationsverschulden
werde nicht nachgewiesen. Denn es werde von der Vorinstanz nicht begründet, inwiefern die Beschwerdeführerinnen
eine objektive Sorgfaltspflicht verletzt hätten oder ein Organisationsverschulden vorliege. Aus
dem Bestehen der objektiven Tatbestandsmerkmale eines Wettbewerbsverstosses könne nicht ohne weiteres
auf den subjektiven Tatbestand der Unternehmensmitarbeiter und daraus weiter auf ein Organisationsverschulden
geschlossen werden.
15.1.7 Die
Vorinstanz hielt in ihrer Vernehmlassung unter Verweis auf die Erwägungen in der angefochtenen Verfügung
an der Qualifikation der Verhaltensweisen als zumindest eventualvorsätzlich fest. Zudem seien auch
alle Elemente für einen fahrlässigen Kartellrechtsverstoss aufgezeigt worden. Ausreichend für
das Vorliegen von Verschulden im Sinne von Vorwerfbarkeit sei gemäss der bundesgerichtlichen Rechtsprechung
ein objektiver Sorgfaltsmangel bzw. ein Organisationsverschulden. Sei ein Kartellrechtsverstoss nachgewiesen,
so sei im Regelfall auch ein objektiver Sorgfaltsmangel bzw. ein Organisationsverschulden gegeben. Nur
in seltenen Fällen liege keine Vorwerfbarkeit vor; so möglicherwiese, wenn der durch einen
Mitarbeitenden ohne Organstellung begangene Kartellrechtsverstoss innerhalb des Unternehmens nicht bekannt
gewesen sei und auch mit einer zweckmässigen Ausgestaltung der Organisation nicht habe bekannt werden
können. Vorliegend handle es sich bei der Gestaltung des Geschäftsmodells und der Verträge
um einen Strategieentscheid, der von der Führungsebene getroffen werde. Ein Organisationsverschulden
sei daher in jedem Fall gegeben.
15.1.8 Schliesslich
hält die Vorinstanz betreffend das Vorbringen der Beschwerdeführerinnen, das Sekretariat um
Beratung ersucht zu haben bzw. die überarbeiteten Verträge eingereicht zu haben, fest, dass
während eines kartellrechtlichen Untersuchungsverfahrens kein Raum für eine Beratung nach Art.
23 Abs. 2 KG bestehe. Die Verträge seien nicht für ein Widerspruchsverfahren i.S.v. Art. 49a
Abs. 3 Bst. b KG eingereicht worden und auch nicht vorgängig zum Strategieentscheid für eine
Beratung i.S.v. Art. 23 Abs. 2 KG. Schliesslich wäre eine Beurteilung der Verträge durch
das Sekretariat vor deren Implementierung aufgrund der Komplexität der Materie und der Kurzfristigkeit
ohnehin nicht möglich gewesen.
15.1.9 Sorgfaltspflichtverletzungen
innerhalb eines Unternehmens sind diesem als massgeblichem Kartellrechtssubjekt ohne weiteres objektiv
zuzurechnen, soweit Tochter- und Muttergesellschaft eine wirtschaftliche Einheit im Sinne von Art. 2
Abs. 1bis KG bilden. Davon zu unterscheiden
ist die subjektive Zurechenbarkeit. Für die Beurteilung der subjektiven Zurechenbarkeit und damit
die Vorwerfbarkeit im engeren Sinne ist ein objektiver Sorgfaltsmassstab anzusetzen. So ist das Vorliegen
eines objektiven Sorgfaltsmangels im Sinne eines Organisationsverschuldens auf Seiten des Unternehmens
für die subjektive Zurechenbarkeit prinzipiell ausreichend. Dabei gilt es zu beachten, dass die
Mitglieder der Führungsgremien von Gesellschaften aufgrund von gesellschaftsrechtlichen Vorschriften
im Hinblick auf die gesamte Geschäftstätigkeit des Unternehmens verpflichtet sind, eine sorgfaltsgemässe
Geschäftstätigkeit sicherzustellen, was gesetzeskonformes Verhalten mitumfasst. Im Rahmen des
Kartellrechts ergeben sich die Sorgfaltspflichten primär aus dem Kartellgesetz, an dessen Vorschriften
sich die Unternehmen halten müssen. Der Umstand, dass ein nachweisbares wettbewerbswidriges Verhalten
vorliegt, lässt in aller Regel auch auf eine Verletzung der objektiven Sorgfaltspflicht schliessen,
denn die Unternehmen müssen über die Regeln des Kartellgesetzes, über die dazu ergangene
Praxis und die einschlägigen Bekanntmachungen informiert sein (BGE 143
II 297, Gaba, E. 9.6.2; Urteile
2C_ 985/2015, ADSL II,
E. 8.5.2; 2C.484/2010, Publigroupe, E. 12.2.2 [nicht
publizierte Erwägung in BGE 139 I 72]; B-2977/2007, Publigroupe,
E. 8.2.2; B-581/2012, Nikon, E. 8.2.4; B-7633/2009, ADSL
II, E. 674 ff., 677, 695 f.; Botschaft KG, BBl 1995 I 468, 620).
15.1.10 Soweit
ein Organisationsverschulden im Einzelfall nachgewiesen wird, bedarf es keiner weiteren Abklärungen
von Seiten der Wettbewerbsbehörden oder der Gerichte im Hinblick auf die Verwirklichung des Verschuldens
aufgrund eines sonstigen aktiven oder passiven Verhaltens. Ebenso bedarf es keiner Abklärungen im
Hinblick auf eine vorsätzliche Begehung des wettbewerbswidrigen Verhaltens, soweit die Umstände
einer fahrlässigen Begehung dargelegt sind (Urteil B-7633/2009, ADSL II,
E. 676).
15.1.11 Es
wird vorliegend weder geltend gemacht, noch ist ersichtlich, dass die wettbewerbswidrigen Handlungen
von anderen Personen vorgenommen wurden, als von den Mitarbeitern der HCI, die im Rahmen der geschäftlichen
Tätigkeiten zur Durchführung derartiger Massnahmen berechtigt waren.
15.1.12 Weiter
darf davon ausgegangen werden, dass bei der ehemaligen Galenica-Gruppe Kenntnisse des Kartellgesetzes
vorhanden waren. Die Vorinstanz zeigte korrekt auf, dass die ehemalige Galenica-Gruppe bereits in kartellrechtliche
Verfahren involviert war. Die ehemalige Galenica-Gruppe hätte damit in Bezug auf kartellrechtliche
Problematiken besonders sensibilisiert sein müssen. Die Verantwortlichen kannten zudem unbestrittenermassen
das Urteil des Bundesverwaltungsgericht BVGE 2011/60 und die damit einhergehende Änderung für
die Publikation der Arzneimittelinformationen. Es war für sie auch ohne weiteres erkennbar, dass
es damit auch auf den umliegenden und nachgelagerten Märkten zu Änderungen kommen würde.
15.1.13 Nachdem
die Beschwerdeführerin 2 bei der Offertstellung 2012 selber von einer Marktabdeckung von mehr als
90% ausging und die Vorinstanz mit Verfügung vom 7. Juli 2008 festgestellt hatte, dass Documed auf
den Markt für die Publikation von Fachinformationen gedruckt und online in einem vollständigen
Werk sowie auf dem Markt für die Publikation von Patienteninformationen online in einem vollständigen
Werk eine marktbeherrschende Stellung hatte, hätte der ehemaligen Galenica-Gruppe bewusst sein müssen,
dass sie in den hier massgebenden Märkten möglicherweise als marktbeherrschend eingestuft würde.
15.1.14 Unter
diesen Umständen hätte der ehemaligen Galenica-Gruppe auch bewusst sein müssen, dass Koppelungen
von Leistungen sowie Vertragsklauseln, die Charakteristiken von Alleinbezugsverpflichtungen aufweisen,
kartellrechtlich problematisch sein können. Insgesamt hätte der ehemaligen Galenica-Gruppe
aufgrund der erwähnten Umstände zumindest bewusst sein müssen, dass ihr Verhalten heikel
ist und eine Sanktionierung droht. Gleichwohl hat sie die Verhaltensweisen implementiert, so dass zumindest
ein objektiver Sorgfaltsmangel, d.h. ein Organisationsverschulden vorliegt.
15.1.15 Die
Vorbringen der Beschwerdeführerinnen vermögen an diesem Ergebnis nichts zu ändern. Denn
einerseits hätte für die Verantwortlichen ersichtlich sein sollen, dass sich der vorliegende
Sachverhalt vom Sachverhalt in der Untersuchung Publikation von Arzneimittelinformationen
unterscheidet. So geht es in casu nicht wie damals um die gesetzlich vorgesehene Publikation, sondern
um die Aufnahme der Daten in eine Datenbank eines Datenveredlers, zu welcher die Zulassungsinhaberinnen
nicht durch gesetzliche oder regulatorische Vorgaben verpflichtet sind. Zudem ist es für die Bejahung
eines Organisationsverschuldens bzw. von fahrlässigem Verhalten nicht erforderlich, dass der Vorwurf
der Koppelung von Leistungen bereits bei Untersuchungseröffnung bestand und mitgeteilt wurde. Ebenso
wenig kann auch der Umstand, dass die Beschwerdeführerin 2 das Sekretariat um Beratung ersucht hat,
das Vorliegen von fahrlässigem Handeln umstossen.
15.1.16 Ob
die wettbewerbswidrigen Verhalten von den Verantwortlichen der ehemaligen Galenica-Gruppe gar billigend
in Kauf genommen wurde, kann somit offengelassen werden. In den dem Bundesverwaltungsgericht zur Verfügung
stehenden Unterlagen fehlen ausreichende Belege, welche den Eventualvorsatz genügend dokumentieren
würden. Aus prozessökonomischen Gründen erscheint es weder angezeigt noch erfolgversprechend,
mehrere Jahre später nach solchen Belegen zu forschen. Wie die Beschwerdeführerinnen zu Recht
geltend machen, kann eventualvorsätzliches Handeln zudem nicht alleine aus dem Umstand, dass die
Beschwerdeführerinnen ihr Verhalten auch nach der Eröffnung des Kartellverfahrens fortgeführt
haben, gefolgert werden. Denn die Eröffnung eines Kartellverfahrens kann angesichts der bisherigen
Prüfungs- und Entscheidpraxis der Wettbewerbsbehörden nicht mit einer Untersagung des betreffenden
wirtschaftlichen Verhaltens gleichgesetzt werden (Urteil B-7633/2009, ADSL II,
E. 690).
15.1.17 Zu
Gunsten der ehemaligen Galenica-Gruppe ist daher davon auszugehen, dass kein vorsätzliches, sondern
lediglich ein fahrlässiges Verhalten vorlag (vgl. bereits Urteil B-7633/2009, ADSL
II, E. 690 f.; vgl. auch Tagmann/Zirlick, BSK-KG, Art. 49a N 10
f.).
15.2 Sanktionsbemessung
15.2.1 Allgemeines
15.2.1.1 Sind
die Tatbestandsvoraussetzungen von Art. 49a Abs. 1 KG erfüllt, ist das Unternehmen mit einem Betrag
bis zu 10 Prozent des in den letzten drei Geschäftsjahren in der Schweiz erzielten Umsatzes zu sanktionieren.
Der Betrag bemisst sich dabei nach der Dauer und der Schwere des unzulässigen Verhaltens. Der mutmassliche
Gewinn, den das Unternehmen durch jenes erzielt hat, ist angemessen zu berücksichtigen. Im Rahmen
der konkreten Sanktionsbemessung wird der im Einzelfall auszusprechende Betrag innerhalb des abstrakten
- in Art. 49a Abs. 1 KG festgelegten - Sanktionsrahmens anhand der in Art. 2 ff. der KG-Sanktionsverordnung
vom 12. März 2004 (SVKG, SR 251.5) enthaltenen Kriterien bestimmt (BGE 144 II 194, BMW,
E. 6.2; 143 II 297, Gaba, E. 9.7.1; Urteile 2C_985/2015, ADSL
II, E. 9.1; 2C.484/2010, Publigroupe, E. 12.3.1 [nicht publizierte
Erwägung in BGE 139 I 72]).
15.2.2 Den
Wettbewerbsinstanzen kommt bei der Sanktionsbemessung ein erheblicher Ermessenspielraum in Bezug auf
die konkrete Festlegung der einzelnen Sanktionskomponenten des Basisbetrags, der Dauer sowie der Erhöhungs-
und Milderungsgründe zu (BGE 143 II 297, Gaba, E. 9.7.2;
139 I 72, Publigroupe, E. 7.4.5.4; Urteil B-7633/2009, ADSL
II, E. 709; Borer, a.a.O., Art. 49a Rz. 17; Krauskopf,
DIKE-KG, Art. 49 Abs. 1-2 N 61; Roth/Bovet, CR-Concurrence,
Art. 49a Rz. 17; Weber/Volz, a.a.O., Rz. 3.231). Dieser
Ermessensspielraum wird durch den Verhältnismässigkeitsgrundsatz und den Gleichheitsgrundsatz
eingeschränkt (BGE 143 II 297, Gaba, E. 9.7.2; 139 I
72, Publigroupe, E. 7.4.5.4; Urteil B-7633/2009, ADSL
II, E. 709; Borer, a.a.O., Art. 49a Rz. 15; Krauskopf,
DIKE-KG, Art. 49 Abs. 1-2 N 61; Roth/Bovet,
CR-Concurrence, Art. 49a Rz. 15, 28 ff.; Weber/Volz,
a.a.O., Rz. 3.231). So sieht auch Art. 2 Abs. 2 SVKG ausdrücklich vor, dass bei der Festsetzung
der Sanktion das Prinzip der Verhältnismässigkeit zu berücksichtigen ist.
15.2.3 Basisbetrag
15.2.3.1 Ausgangspunkt
der konkreten Sanktionsberechnung ist der Basisbetrag. Der Basisbetrag beträgt nach Art. 3 SVKG
je nach Art und Schwere des Verstosses bis zu 10% des Umsatzes, den das betreffende Unternehmen in den
letzten drei Geschäftsjahren auf dem relevanten Markt in der Schweiz erzielt hat. Dieser Umsatz
bildet somit die Grund- und Ausgangslage für die Festlegung der Sanktion.
15.2.3.2 Grundlage
für die Feststellung des massgeblichen Umsatzes bildet in der Regel die jeweilige Jahresrechnung
des Unternehmens, aus der die entsprechenden Daten zu entnehmen oder abzuleiten sind (Urteile
2C_985/2015, ADSL II,
E. 9.2.2.1; B-7633/2009, ADSL II,
E. 721).
15.2.3.3 Als
massgeblich für die Ermittlung des Basisbetrags werden die letzten drei Geschäftsjahre statuiert.
Der Zeitraum wurde durch den Gesetzgeber mit drei Geschäftsjahren festgelegt, um zu verhindern,
dass Unternehmen mittels geeigneter Massnahmen kurzfristig den Umsatz verringern, um in den Genuss einer
geringeren Sanktion zu gelangen (Botschaft über die Änderung des Kartellgesetzes vom 7. November
2001 [BBl 2001 2022, 2037]). Die Vorinstanz stellte auf den Umsatz in den Jahren 2013 bis 2015 ab. Dies
ist nicht zu beanstanden und kann somit bestätigt werden.
15.2.3.4
Art. 49a Abs. 1 KG und Art. 3 SVKG sehen keine gesonderte Regelung zur Bestimmung der relevanten
Märkte bei der Bemessung einer Sanktionierung vor. Bei der Bestimmung des relevanten Markts für
die Bemessung einer Sanktionierung eines Marktmissbrauchs sind diejenigen Märkte relevant, auf welche
das marktbeherrschende Unternehmen mit seiner wettbewerbswidrigen Verhaltensweise einwirkt. Grundsätzlich
entspricht der für die Sanktionierung massgebliche relevante Markt dem sachlich und räumlich
relevanten Markt. Für die Sanktionsbemessung kann daher regelmässig auf die Marktabgrenzung
zum sachlich und räumlich relevanten Markt abgestellt werden. Es bedarf für die Sanktionsbemessung
regelmässig keiner erneuten Feststellung des massgeblichen Marktes (Urteile B-631/2011, SIX,
E. 1568 f.; B-7633/2009, ADSL
II, E. 723).
15.2.3.5 Wirkt
das marktbeherrschende Unternehmen mit seiner wettbewerbswidrigen Verhaltensweise im Einzelfall darüber
hinaus auf sonstige Märkte ein, so sind diese ebenfalls in die Sanktionsbemessung mit einzubeziehen
(Urteile B-631/2011, SIX, E. 1570; B-7633/2009,
ADSL II, E. 723).
Massgebend für die Sanktionsbemessung ist daher nicht nur der Markt, auf dem die marktbeherrschende
Stellung des Unternehmens gegeben ist. Der Begriff "relevante Märkte" ist vielmehr auf
eine Erfassung aller derjenigen Märkte ausgerichtet, auf denen sich eine nachteilige Einwirkung
des wettbewerbswidrigen Verhaltens feststellen lässt. Dabei kann es sich sowohl um den Markt, auf
dem das Unternehmen seine marktbeherrschende Stellung innehat, als auch um Sekundärmärkte als
vor- und nachgelagerte Märkte oder Tertiärmärkte handeln, die in das konkrete wirtschaftliche
Verhalten eingebunden sind. Dies gilt insbesondere für diejenigen Missbrauchsformen des Art. 7 KG,
die sich bereits aufgrund ihrer tatbestandlichen Ausgestaltung auf mehrere Märkte erstrecken (Urteil
B-631/2011, SIX, E. 1570 und 1573).
15.2.3.6 Die
Vorinstanz erwog, Documed und e-mediat hätten ihren Umsatz auf dem Markt für veredelte, maschinenlesbare
Daten betreffend Medikamenteninformationen und auf dem Markt für den Zugang zu veredelten, maschinenlesbaren
Medikamenteninformationen erzielt. Entsprechend könne auf die kumulierten Umsätze von Documed
und e-mediat abgestellt werden. Diese entsprächen Fr. [...] im Jahr 2013, Fr. [...]
im Jahr 2014 und Fr. [...] im Jahr 2015. Damit betrage der für die Berechnung des Basisbetrages
massgebliche Umsatz Fr. [...] und die Obergrenze des Basisbetrages belaufe sich auf Fr. [...].
15.2.3.7 Gegen
diese Ermittlung des massgeblichen Umsatzes zur Festlegung des Basisbetrags erheben die Beschwerdeführerinnen
mehrere Einwände. Die Beschwerdeführerinnen sind der Auffassung, es sei für die Berechnung
des Basisbetrages auf die beiden ermittelten relevanten Märkte, den Markt für den Zugang zu
elektronischen Datensätzen betreffend Medikamenteninformationen und den Markt für veredelte
maschinenlesbare Daten betreffend Medikamenteninformationen, abzustellen. So rügen sie, die als
unzulässig qualifizierten Verhaltensweisen der Einschränkung des Absatzes und der Koppelung
von Leistungen würden nur jeweils einen der beiden relevanten Märkte betreffen. Daher könne
für die Berechnung des Umsatzes auf den relevanten Märkten nicht auf den kumulierten Umsatz
von Documed und e-mediat abgestellt werden. Vielmehr habe in einem ersten Schritt eine aufgeschlüsselte
Umsatzberechnung für die beiden relevanten Märkte zu erfolgen und erst in einem zweiten Schritt
könnten die berechneten Umsätze der relevanten Märkte zum Basisbetrag kumuliert werden.
15.2.3.8 Entgegen
den Vorbringen der Beschwerdeführerinnen ist nicht zu beanstanden, wenn trotz zweier betroffener
Märkte eine einheitliche Sanktionsberechnung vorgenommen wird, ohne die Umsätze auf die einzelnen
Märkte aufzuschlüsseln. Denn wie die Vorinstanz zutreffend festhält, ist eine Aufschlüsselung,
wenn überhaupt, dann nur mit erheblichem Mehraufwand möglich - ohne dass sich das Ergebnis
ändert. Das Bundesverwaltungsgericht hat auch bereits im Urteil B-3332/2012 vom 13. November 2015
i.S. BMW bei mehreren betroffenen Märkten eine einheitliche
Sanktionsberechnung vorgenommen, ohne die Umsätze auf die einzelnen Märkte aufzuschlüsseln.
15.2.3.9 Weiter
rügen die Beschwerdeführerinnen, die Berechnung der Vorinstanz sei auch insofern fehlerhaft,
als dass ihr die gesamten Nettoerlöse der Erfolgsrechnungen der Documed und e-mediat aus den Jahren
2013-2015 zugrunde gelegt worden sei. Documed und e-mediat hätten auch Umsätze auf anderen,
nicht relevanten Märkten erzielt, welche in Abzug zu bringen seien. Für die Berechnung des
Basisbetrages sei nur auf die beiden ermittelten relevanten Märkte abzustellen. Die Beschwerdeführerinnen
reichten mit der Beschwerde eine "Übersicht bereinigte Umsatzzahlen" ein und erläuterten
die einzelnen Positionen in ihrer Replik.
15.2.3.10 Die
Vorinstanz bezeichnet die von den Beschwerdeführerinnen eingereichten "bereinigten" Umsatzzahlen
als intransparent, unbelegt und ohne buchhalterische Logik. Die Beschwerdeführerinnen würden
ohne sachliche Begründung unterschiedliche Zahlen als "bereinigte Umsatzzahlen" in den
Raum stellen. Zudem habe sie, die Vorinstanz, berechtigter Weise davon ausgehen können, dass die
gesamten berücksichtigten Umsätze von Documed und e-mediat im Vertrieb der elektronischen Medikamenteninformationen
erzielt worden seien. Denn sowohl G._______ anlässlich des Parteiverhörs als auch die Beschwerdeführerinnen
in ihrer Stellungnahme zum Antrag hätten festgehalten, dass auf den relevanten Märkten bzw.
im Bereich der Medikamenteninformationen jährlich ca. [...] Umsatz erzielt würden.
15.2.3.11 Die
Beschwerdeführerinnen machen, was den sachlich relevanten Markt betreffend die Marktgegenseite der
Zulassungsinhaberinnen (Markt für die Aufnahme und den Erhalt in elektronischen Datensätzen
betreffend Medikamenteninformationen) betrifft, bis auf eine Ausnahme im Beschwerdeverfahren die gleichen
Abzüge geltend wie in ihrer Stellungnahme vom 13. Juli 2016 zum Verfügungsantrag (vgl.
Vorinstanz, act. 1070, Beilage 15). Einzig die Umsätze aus dem D-Modul (Kompendium) machen
sie im Beschwerdeverfahren nicht mehr als Abzug geltend. Was den relevanten Markt betreffend die Marktgegenseite
der Leistungserbringerinnen und -erbringer, etc. (Markt für veredelte, elektronische Datensätze
betreffend Medikamenteninformationen) betrifft machen die Beschwerdeführerinnen im Beschwerdeverfahren
erstmals Abzüge von auf anderen Märkten erzielten Umsätzen geltend.
15.2.3.12 Vorliegend
wurden der Markt für die Aufnahme und den Erhalt in elektronischen Datensätzen betreffend Medikamenteninformationen
sowie der Markt für veredelte, maschinenlesbare Daten betreffend Medikamenteninformationen als relevante
Märkte festgestellt. Für die Ermittlung des Basisbetrags ist somit grundsätzlich vom auf
diesen beiden Märkten erzielten Umsatz auszugehen. Es sind jedoch auch Umsätze von sonstigen
(vor- oder nachgelagerten) Märkten miteinzubeziehen, sofern mit den wettbewerbswidrigen Verhaltensweisen
auch auf diese eingewirkt wurde (s. oben E. 15.2.3.5).
In diesem Sinne ist nachfolgend für die einzelnen strittigen
Umsätze zu prüfen, ob sie bei der Berechnung des Basisbetrages zu berücksichtigen sind.
Dabei handelt es sich zunächst um folgende:
- [...]
- [...]
- [...]
- [...]
- [...]
- [...]
- [...]
- [...]
- [...].
15.2.3.13 Bei
all diesen Umsätzen handelt es sich offensichtlich um Umsätze, die nicht auf dem Markt für
die Aufnahme und den Erhalt in elektronischen Datensätzen betreffend Medikamenteninformationen erzielt
wurden und auch nicht dem Markt für veredelte, elektronische Datensätze betreffend Medikamenteninformationen
zuzuordnen sind. Es ist auch nicht ohne weiteres ersichtlich, inwiefern die Beschwerdeführerinnen
mit den wettbewerbswidrigen Verhaltensweisen unmittelbar auf diese anderen Märkte eingewirkt haben.
Deshalb sind diese erzielten Umsätze von Umsatzzahlen in den Erfolgsrechnungen in Abzug zu bringen.
15.2.3.14 Anders
gestaltet sich die Lage bei den Umsätzen "academy" aus Schulungen. Gemäss Angaben
der Beschwerdeführerinnen besuchten [...] % der Teilnehmenden Schulungen im Zusammenhang mit
einer vertraglichen Bindung, [...] % hätten Pharmavista-Schulungen und [...] % Schulungen
zum Pharmamarkt Schweiz besucht.
15.2.3.15 Zumindest
alle Schulungen, die den Umgang mit den INDEX-Daten beinhalten, können nicht einem anderen Markt
zugeordnet werden. Das Vorbringen der Beschwerdeführerinnen, die Durchführung von Schulungen
habe nichts mit dem Bereitstellen von elektronischen Datensätzen betreffend Medikamenteninformationen
zu tun, überzeugt nicht. Denn gemäss vielen Verträgen von e-mediat mit den Softwarehäusern
waren die Softwarehäuser verpflichtet, Schulungen von e-mediat zum Umgang mit den INDEX-Daten "in
ausreichendem Mass" zu nutzen. Innerhalb von vier Monaten nach Vertragsunterzeichnung war mindestens
ein Kurstag für Programmierer auf eigene Kosten zu absolvieren (vgl. Vorinstanz, act. 1120,
oftmals Ziff. 17 der Verträge). Zudem werden solche Schulungen nur von Softwarehäusern besucht
und nachgefragt, die einen Lizenzvertrag und Zugang zu den INDEX-Produkten haben.
15.2.3.16 Pharmavista
ist ein Online-Informationsangebot für den Schweizer Pharmamarkt und soll einen einfachen Zugriff
auf wissenschaftliche und kommerzielle Daten zu Arzneimitteln, Parapharmazeutika und Kosmetika ermöglichen.
Pharmavista enthält neben den allgemeinen Produktinformationen zu Arzneimitteln, auch die Details
zu Artikeln und Produkten aus den INDEX-Datenbanken. Ergänzend werden Informationen zu aktuellen
Themen aus dem Gesundheitswesen und der medizinisch-therapeutischen Forschung publiziert. Mit Pharmavista
haben Fachpersonen Zugriff auf aktuelle Informationen, wissenschaftliche und kommerzielle Daten zu Arzneimitteln,
Parapharmazeutika und Kosmetika (www.hcisolutions.ch/de/datenbanken-und-software/pharmavista.php [abgerufen
am 07.12.2021]). Damit handelt es sich ebenfalls um ein Produkt, das unter anderem veredelte, maschinenlesbare
Daten betreffend Medikamenteninformationen enthält. Wie bereits oben erwähnt stehen Schulungen
zu einem solchen konkreten, einzelnen Produkt in einem derart engen Zusammenhang zu diesem Produkt, dass
es sich rechtfertigt die Umsätze aus Schulungen ebenfalls zu berücksichtigen.
15.2.3.17 Schulungen
zum Pharmamarkt Schweiz sind dagegen nicht dem Markt für veredelte, elektronische Datensätze
betreffend Medikamenteninformationen zuzuordnen. Entsprechend sind [...] % der aus Schulungen erzielten
Umsätze in Abzug zu bringen.
15.2.3.18 Die
von den Beschwerdeführerinnen angegebenen Prozent-sätze für die Umsätze aus den verschiedenen
Schulungen ergeben im Total nur 80%. Da die Beschwerdeführerinnen damit nicht darlegen, dass die
übrigen 20% der Schulungen nicht im Zusammenhang mit der Aufnahme und dem Erhalt in elektronischen
Datensätzen betreffend Medikamenteninformationen und veredelten, maschinenlesbaren Daten betreffend
Medikamenteninformationen stehen, sind diese Umsätze bei der Sanktionsberechnung zu berücksichtigen.
15.2.3.19 Grundsätzlich
ist bei der Berechnung des Basisbetrages auf die Nettoerlöse abzustellen. Das heisst von den Bruttoumsätzen
sind Erlösminderungen wie Skonti und Rabatte, Mehrwertsteuern und andere Verbrauchssteuern sowie
weitere unmittelbar auf den Umsatz bezogene Steuern abzuziehen (Art. 4 Abs. 1 VKU).
15.2.3.20 Auch
die Vorinstanz stellte bei der Berechnung des Basisbetrages auf die Nettoerlöse ab. In der Vernehmlassung
weist sie allerdings daraufhin, die der Sanktionsberechnung zugrundeliegenden Umsatzzahlen sähen
unter dem Titel "Erlösminderungen" bereits hohe Abzüge vor. Bei einer allfälligen
Zulassung von weiteren Abzügen sei deshalb darauf zu achten, dass nicht die gleiche Position mehrmals
abgezogen werde. Die Beschwerdeführerinnen legen in der Replik aber schlüssig dar, dass durch
die Erlösminderungen und die zu berücksichtigenden Abzüge nicht die gleichen Positionen
mehrmals abgezogen werden. So führen sie aus, bei den geltend gemachten Erlösminderungen handle
es sich um solche nach Art. 4 Abs. 1 VKU (Skonti, Rabatte, Mehrwertsteuern und andere Verbrauchsteuern
sowie weitere unmittelbar auf den Umsatz bezogene Steuern). [...]. Die Darstellung des Bruttoumsatzes
in der Erfolgsrechnung habe rein theoretischen Charakter, konzernintern und gegenüber Investoren
werde ausschliesslich mit der Grösse der Nettoumsätze gearbeitet. Es ist somit auf die Nettoerlöse
abzustellen.
15.2.3.21 Strittig
ist schliesslich die Frage, ob konzerninterne Umsätze bei der Ermittlung des Basisbetrages zu berücksichtigen
sind. Die Beschwerdeführerinnen bringen vor, nach der herrschenden Kartellrechtslehre seien konzerninterne
Umsätze in Anwendung von Art. 5 Abs. 2 VKU bei der Umsatzberechnung nach Art. 49a KG nicht zu beachten.
Die Vorinstanz habe dies in ihren Erwägungen in Rz. 504 sogar selbst erwähnt, jedoch in der
konkreten Sanktionsberechnung dann nicht berücksichtigt. Zudem würde sich der Abzug auch aus
dem Sinn und Zweck von Art. 7 KG ergeben, denn Art. 7 KG verbiete eine Ausbeutung oder Behinderung
anderer Unternehmen, einen konzerninternen Machtmissbrauch gebe es nicht. Sodann dränge sich ein
Abzug der konzerninternen Umsätze auch bei einer wirtschaftlichen Betrachtungsweise auf. Gemäss
Art. 2 Abs. 1bis KG würden sämtliche
Nachfrager oder Anbieter von Gütern und Dienstleistungen im Wirtschaftsprozess unabhängig von
ihrer Rechts- oder Organisationsform als Unternehmen gelten. Mehrere zu einem Konzern gehörende
Rechtsträger werden als ein einziges Unternehmen betrachtet, womit sämtliche Umsätze der
kontrollierten Gesellschaften berücksichtigt werden. Bei einer Betrachtung auf Konzernebene müssten
demnach die konzerninternen Umsätze bei der Berechnung der Sanktion abgezogen werden.
15.2.3.22 Soweit
die Beschwerdeführerinnen geltend machen, die Vorinstanz habe in der Verfügung selbst erwogen,
konzerninterne Umsätze seien nicht zu berücksichtigen, ist festzuhalten, dass die fraglichen
vorinstanzlichen Erwägungen die Festlegung der Maximalsanktion betreffen. Die Maximalsanktion hat
- anders als der Basisbetrag - den Zweck, die wirtschaftliche Tragbarkeit der Sanktion für
das Unternehmen als solches zu garantieren. Da Umsätze innerhalb des Unternehmens die wirtschaftliche
Leistungsfähigkeit desselben nicht verbessern, dürfen sie für die Berechnung der Maximalsanktion
nicht berücksichtigt werden. Entsprechend ist dieses Vorbringen nicht stichhaltig.
15.2.3.23 Wie
bereits erwähnt, sehen Art. 49a Abs. 1 KG und Art. 3 SVKG keine spezifischen Regelungen für
die konkrete Ermittlung des Umsatzes im Einzelfall vor. Literatur und Rechtsprechung nehmen deshalb Bezug
auf die Verordnung über die Kontrolle von Unternehmenszusammenschlüssen. Für Unternehmenszusammenschlüsse
statuieren Art. 4 und 5 VKU Regelungen zur Ermittlung des massgeblichen Umsatzes. Art. 5 Abs. 2
VKU bestimmt, dass Umsätze zwischen gemäss Art. 5 Abs. 1 VKU verbundenen Unternehmen, sogenannte
konzerninterne Umsätze, nicht zu berücksichtigen sind. Das Bundesgericht hat bei der Berechnung
des Umsatzes bislang nur auf Art. 4 VKU verwiesen (BGE 143 II 297, Gaba,
E. 9.7.2; Urteile 2C_985/2015, ADSL II, E. 9.2.2.3; 2C.484/2010,
Publigroupe, E. 12.3.2 [nicht publizierte Erwägung in BGE 139 I
72]). Die Literatur geht davon aus, dass die Bestimmungen der VKU sinngemäss herangezogen werden
können, soweit sie überhaupt passen (Tagmann/Zierlick,
BSK-KG, Art. 49a N 45; Roth/Bovet, CR-Concurrence, Art.
49a N 26).
15.2.3.24
Im Urteil B-7633/2009 vom 14.
September 2015 i.S. ADSL II
erwog das Bundesverwaltungsgericht, bei einer Kosten-Preis-Schere ergebe sich das Schädigungspotential
nicht nur aus der Betrachtung eines einzelnen Marktes, sondern erst das strategische Zusammenwirken von
vertikaler Ausbeutung und horizontaler Behinderung ermögliche die besondere Beeinträchtigungswirkung.
Dabei würden die Umsätze zwischen der Obergesellschaft und dem vertikal integrierten Unternehmen
gerade den Hebel für diese Beschränkung bilden. Bei den berücksichtigten Umsätzen
handle es sich um solche, die in einem unmittelbaren Zusammenhang mit der Wettbewerbsbeeinträchtigung
stünden und nicht um sonstige konzerninterne Umsätze, die keinen Bezug zum Missbrauchsverhalten
aufweisen würden. Es sei deshalb erforderlich und sachgerecht, diese konzerninternen Umsätze
bei der Sanktionsbemessung zu berücksichtigen. Diesem Vorgehen stehe auch nicht entgegen, dass konzerninterne
Transaktionen aufgrund des Konzernprivilegs nicht als wettbewerbswidrig zu qualifizieren seien und Art.
5 Abs. 2 VKU vorsehe, dass konzerninterne Umsätze nicht zu berücksichtigen seien. Denn die
Frage der wettbewerbsrechtlichen Qualifizierung konzerninterner Transaktionen stehe in keinem sachlich
zwingenden Zusammenhang mit der Berücksichtigung von konzerninternen Umsätzen im Rahmen der
Sanktionsbemessung. Nicht nur im Kartellrecht, sondern auch im Strafrecht würden Umsätze und
sonstige wirtschaftliche Aspekte ohne unmittelbaren Bezug zu einem rechtswidrigen Verhalten zur Ermittlung
einer Sanktionierung herangezogen. Eine sinngemässe Heranziehung von Art. 5 Abs. 2 VKU sei schon
deshalb ausgeschlossen, weil die konzerninternen Umsätze bei der Wettbewerbsbeschränkung einer
Kosten-Preis-Schere gerade einen Faktor für die wettbewerbswidrigen Auswirkungen darstellen würden,
während dies bei der Wettbewerbsbeschränkung eines Unternehmenszusammenschlusses nicht der
Fall sei (Urteil B-7633/2009, ADSL II,
E. 724 f.).
15.2.3.25
Das Bundesgericht bestätigte in seinem Urteil
2C_985/2015 vom 9. Dezember 2019 i. S. ADSL II,
dass Art. 5 Abs. 2 VKU nicht auf den konkreten Sachverhalt passe. Zusammenschlussvorhaben seien kartellrechtlich
relevant, wenn sie einen Grenzbetrag erfüllen. Für die Berechnung der Grenzbeträge nach
Art. 9 Abs. 1-3 KG seien nach Art. 3 Abs. 1 Satz 1 VKU die Umsätze der am Zusammenschluss beteiligten
Unternehmen massgebend. Dabei würden Art. 4 ff. VKU die Berechnung regeln. Art. 5 Abs. 2 VKU
schliesse für die Berechnung des Gesamtumsatzes eines beteiligten Unternehmens die Geschäfte
zwischen den am Zusammenschluss beteiligten Unternehmen aus. Der Grund hierfür sei, dass die Umsätze
die wirkliche Stärke des beteiligten Unternehmens im Markt widerspiegeln sollen, denn nur die wirkliche
Stärke der beteiligten Unternehmen bilde den Anlass für die kartellrechtliche Relevanz des
Zusammenschlussvorhabens. Insofern sei Art. 5 Abs. 2 VKU gar nicht Ausfluss des Konzernprivilegs, was
im Übrigen auch Art. 5 Abs. 1 VKU bestätige. Danach umfasse der Umsatz eines beteiligten Unternehmens
neben denjenigen aus eigener Geschäftstätigkeit auch die Umsätze der mit ihm in einer
wirtschaftlichen Einheit bzw. in einem Konzern "verbundenen Unternehmen". Im Urteil 2C_985/2015
gehe es weder um ein Zusammenschlussvorhaben, noch passe die Ausgangslage analog zum dem Urteil zugrundeliegenden
Sachverhalt. Denn die unzulässige Verhaltensweise (Kosten-Preis-Schere) bestehe gerade im Verbund
der beiden Unternehmen. Würde Art. 5 Abs. 2 VKU in einem solchen Fall Anwendung finden, würden
die Beschwerdeführerinnen wegen ihrer Verhaltensweise zudem noch begünstigt, was nicht der
Intention des Gesetzgebers bei Einführung der Sanktionen entsprochen habe (Urteil 2C_985/2015, ADSL
II, E. 9.2.2.4).
15.2.3.26
In casu geht es um Umsätze auf dem Markt für
die Aufnahme und den Erhalt in elektronischen Datensätzen betreffend Medikamenteninformationen,
welche Documed und e-mediat mit den konzerneigenen Zulassungsinhaberinnen erwirtschaftet haben sowie
um Umsätze mit veredelten, maschinenlesbaren Daten betreffend Medikamenteninformationen, die mit
den konzerneigenen Leistungserbringern, Grossisten, etc. erwirtschaftet wurden.
15.2.3.27
Anders als im Urteil B-7633/2009 vom 14. September
2015 i. S. ADSL II
geht es vorliegend nicht um eine Kosten-Preis-Schere, sondern um eine Koppelung von Leistung und eine
Einschränkung des Absatzes. Die vertikal Integration des Vertriebs der Arzneimittel und der
entsprechenden Medikamenteninformationen in der ehemaligen Galenica-Gruppe verhalf vorliegend jedoch
gerade zur marktbeherrschenden Stellung. Die fraglichen Umsätze
stehen in einem unmittelbaren Zusammenhang mit der Wettbewerbsbeeinträchtigung. Es handelt sich
nicht um sonstige konzerninterne Umsätze, die keinen Bezug zum Missbrauchsverhalten aufweisen.
15.2.3.28 Nicht
gefolgt werden kann den Beschwerdeführerinnen auch, soweit sie geltend machen, der Abzug von konzerninternen
Transaktionen ergebe sich auch aus dem Sinn und Zweck von Art. 7 KG. Denn die Frage der wettbewerbsrechtlichen
Qualifizierung konzerninterner Transaktionen steht in keinem sachlich zwingenden Zusammenhang mit der
Berücksichtigung von konzerninternen Umsätzen im Rahmen der Sanktionsbemessung (s. oben E.
15.2.3.24).
15.2.3.29 Soweit
sich gemäss den Beschwerdeführerinnen unter Bezugnahme auf Art. 2 Abs. 1bis
KG ein Abzug der konzerninternen Umsätze auch bei einer wirtschaftlichen Betrachtungsweise aufträgt,
ist festzuhalten, dass eine Betrachtung auf Konzernebene mit Abzug der konzerninternen Transaktionen
bereits bei der Berechnung der Maximalsanktion erfolgt, welche die wirtschaftliche Tragbarkeit der Sanktion
für das Unternehmen garantieren soll.
15.2.3.30 Die
konzerninternen Umsätze sind somit bei der Sanktionsberechnung zu berücksichtigen. Der für
die Berechnung des Basisbetrages massgebliche Umsatz beträgt entsprechend Fr. [...]. Dies ergibt
sich aus den Umsätzen von Documed und e-mediat abzüglich der erwähnten nicht auf den relevanten
Märkten erzielten Umsätze (vgl. Vorinstanz, act. 829 S. 16 und 31, act. 1011 S. 9 f., act.
1038 S. 130 ff. sowie Beilage 15 zur Beschwerde). Die Obergrenze des Basisbetrages beläuft sich
auf Fr. [...].
|
|
Umsatz
(Nettoerlöse)
|
nicht auf relevanten Märkten erzielter Umsatz
|
massgeblicher Umsatz
|
|
2013
|
Fr. [...]
|
Fr. [...]
|
Fr. [...]
|
|
2014
|
Fr. [...]
|
Fr. [...]
|
Fr. [...]
|
|
2015
|
Fr. [...]
|
Fr. [...]
|
Fr. [...]
|
15.2.4 Berücksichtigung
der Art und Schwere des Verstosses
15.2.4.1 Nach
Art. 49a Abs. 1 KG wird der Sanktionsbetrag unter
anderem nach der Schwere des unzulässigen Verhaltens bestimmt. Art.
3 SVKG hält konkretisierend fest, der Basisbetrag werde nach Schwere und Art des Verstosses
gebildet. Unter Schwere ist die objektive, d.h. verschuldensunabhängige Schwere zu verstehen. Massgebend
sind das abstrakte Gefährdungspotential sowie die volkswirtschaftliche Schädlichkeit. Zu berücksichtigen
ist insbesondere der Grad der Beeinträchtigung des Wettbewerbs, die Wirksamkeit des Verstosses sowie
die Anzahl der Beteiligten (BGE 144 II 194, BMW, E. 6.4; Urteil
2C_985/2015, ADSL II, E. 9.2.3.2; Krauskopf,
DIKE-KG, Art. 49a N 41). Mit dem Verweis auf die Art des Verstosses wird der Gegenstand des wettbewerbswidrigen
Verhaltens angesprochen (Urteil B-831/2011, SIX, E. 1592).
15.2.4.2 Die
Erläuterungen zu Art. 3 SVKG gehen in Bst. d davon aus, dass sich bei Missbräuchen von marktbeherrschenden
Unternehmen nach Art. 7 KG der Basisbetrag "regelmässig im oberen Drittel des Rahmens"
bewegen wird (Sekretariat der WEKO, Erläuterungen zur KG-Sanktionsverordnung [SVKG], Art. 3 Bst.
d). Letztlich ist jedoch eine Beurteilung im Einzelfall aufgrund der konkreten Umstände des Einzelfalls
unumgänglich (Urteile B-7633/2009, ADSL II, E. 713; B-2977/2007,
Publigroupe, E. 8.3.4;
Tagmann/Zirlick, BSK-KG, Art. 49a N 54).
15.2.4.3 Die
Vorinstanz legte den Basisbetrag auf 5% fest. Sie erwog, hinter der Verhaltensweise des Unternehmens
sei eine gesamte Strategie gestanden, mit der die Kontrolle über die Gesamtwertschöpfung habe
gesichert werden sollen. Es seien bezüglich die Ausschreibung von AIPS, das Verhältnis zu den
Zulassungsinhaberinnen, als auch bezüglich das Verhältnis zu den Softwarehäusern und Leistungserbringerinnen
und -erbringern Massnahmen ergriffen worden, um die Einkünfte sicherzustellen. Erschwerend hinzukomme,
dass die Verdrängungswirkungen insbesondere in der Zeit, in der sich die Bedingungen änderten
und damit für den Eintritt potentieller Konkurrenten besonders geeignet gewesen wäre, ihre
Wirkungen gezeigt hätten. Zudem habe das Unternehmen trotz Eröffnung der Untersuchung nicht
davor zurückgeschreckt, die Verhaltensweise fortzuführen und weitere Elemente hinzuzufügen.
Weiter seien verschiedene Verhaltensweisen an den Tag gelegt worden, die Teil einer Gesamtstrategie gewesen
seien und sowohl Verdrängungs- als auch Ausbeutungseffekte gezeitigt hätten, was sich ebenfalls
schwerwiegend auswirke. Ferner falle ins Gewicht, dass den Untersuchungsadressatinnen zumindest eventualvorsätzliches
Verhalten vorzuwerfen sei. Schliesslich habe aufgrund der Verhaltensweise kein Konkurrent in den Märkten
wirklich Fuss fassen können und die Zulassungsinhaberinnen seien weiterhin zur Sicherung der Einnahmen
herangezogen worden, ohne dass dies wettbewerbsmässig begründet gewesen wäre. Insgesamt
wiege das Verhalten schwer.
15.2.4.4 Die
Beschwerdeführerinnen bestreiten, dass die Verhaltensweise der HCI Ausdruck einer Gesamtstrategie,
mit der die Kontrolle über die Gesamtwertschöpfungskette hätte gesichert werden sollen,
gewesen sei. Die Verhaltensweise sei das Resultat einer Anpassung an die geänderten Rahmenbedingungen
gewesen, wobei es darum gegangen sei, gegenüber den Kunden im Interesse der Patientensicherheit
nach wie vor den hohen Qualitätsstandard zu gewährleisten.
15.2.4.5 Weiter
rügen die Beschwerdeführerinnen, die Vorinstanz gehe in der Sanktionsbegründung implizit
davon aus, dass den Verhaltensweisen, welche nicht als unzulässig qualifiziert wurden, gleichwohl
ein Unrechtsgehalt beiliege, der bei der Sanktionsbemessung zu berücksichtigen sei. So falle im
Vergleich zu den Ausführungen des Sekretariats im Antrag die Sanktionsbegründung in der Verfügung
beinahe identisch aus. Insbesondere sei es unsachgemäss, zum Ausdruck zu bringen, das Verhalten
von HCI bei der AIPS-Ausschreibung spiele bei der Sanktionsbemessung eine Rolle. Denn die Vorinstanz
habe die Frage, ob der Tatbestand von Art. 7 Abs. 1 i.V.m. Abs. 2 Bst. d KG erfüllt sei, in der
Verfügung explizit offengelassen. Ebenfalls unsachgemäss sei, die Schwere des Verstosses damit
zu begründen, dass die Zulassungsinhaberinnen weiterhin zur Sicherung der Einnahmen herangezogen
worden seien, ohne dass dies wettbewerbsmässig begründet gewesen wäre. Denn die Vorinstanz
habe eine unzulässige Verhaltensweise nach Art. 7 Abs. 1 i.V.m. Abs. 2 Bst. c KG als nicht genügend
erstellt erachtet und diesbezüglich keine Verletzung des Kartellrechts festgestellt. Zudem liege
der Grund weshalb kein Konkurrent auf dem Markt habe Fuss fassen können, nicht im Verhalten der
HCI, sondern in der schlechteren Qualität der Konkurrenzangebote.
15.2.4.6 Weiter
weisen die Beschwerdeführerinnen auch den Vorwurf zurück, HCI habe nach der Untersuchungseröffnung
die Verhaltensweise fortgeführt und weitere Elemente hinzugefügt. HCI habe 2015 anstelle der
kritisierten Klauseln eine neue Formulierung in die Verträge mit den Softwarehäusern aufgenommen.
Ohnehin dürfe die Eröffnung eines Kartellverfahrens nicht mit der Untersagung des betreffend
wirtschaftlichen Verhaltens gleichgesetzt werden. Entsprechend dürfe die Weiterführung einer
Verhaltensweise bei der Art und Schwere des Verstosses nicht negativ ins Gewicht fallen. Dass ein Unternehmen
sein Verhalten nicht ändere, werde überdies bereits bei der Dauer des Verstosses nach Art.
4 SVKG sanktionserhöhend berücksichtigt. Folglich könne dies bei der Art und Schwere des
Verstosses nicht noch einmal berücksichtigt werden. Demgegenüber sei bei der Bemessung des
Basisbetrages aber miteinzubeziehen, dass HCI vor Einführung der Verträge mit dem Sekretariat
das Gespräch gesucht habe, denn diese Besprechung hätte nach Auffassung der Beschwerdeführerinnen
das vorliegende Verfahren verhindern können.
15.2.4.7 Die
Vorinstanz hält zu diesen Einwänden fest, es treffe nicht zu, dass sie bei der Berücksichtigung
von Art und Schwere davon ausgegangen sei, dass auch den nicht bewiesenen Vorwürfen ein Unrechtsgehalt
zukomme. Der Basisbetrag sei in der Verfügung im Vergleich zum Antrag von 10% auf 5% herabgesetzt
worden. Die Beschwerdeführerinnen würden nicht darlegen, weshalb ihr Verstoss als besonders
mild zu bezeichnen wäre. Die sanktionierten Verhaltensweisen seien insbesondere zur Sicherung der
marktbeherrschenden Stellung zum Zeitpunkt der Systemumstellung eingesetzt worden, d.h. zum Zeitpunkt,
in dem mit Markteintritten zu rechnen gewesen wäre.
15.2.4.8 Zum
Vorbringen der Beschwerdeführerinnen betreffend Gesprächsersuchen hält die Vorinstanz
fest, das Sekretariat habe den ersten Termin aufgrund der damaligen Prioritätensetzung nicht wahrnehmen
können. Die Beschwerdeführerinnen hätten aber zu jedem Zeitpunkt des Verfahrens die Möglichkeit
gehabt, sich zu den Vorwürfen zu äussern und ein Gespräch zwischen der Beschwerdeführerin
2 und dem Sekretariat habe noch im Jahr 2012 stattgefunden.
15.2.4.9 Die
ehemalige Galenica-Gruppe hat mittels HCI durch die Bündelung der Aufnahme der Arzneimittelinformationen
in ihre Datenbanken mit der Qualitätssicherung und dem Upload auf AIPS eine Koppelung vorgenommen
(Art. 7 Abs. 1. i.V.m. Abs. 2 Bst. f KG). Zudem hat sie durch die Klauseln A und B in den Verträgen
mit den Softwarehäusern den Absatz der Konkurrenten i.S.v. Art. 7 Abs. 1 i.V.m. Abs. 2 Bst. e KG
einschränkt. Die Verhaltensweisen haben sowohl Verdrängungs- als auch Ausbeutungseffekte gezeitigt.
15.2.4.10 In
den beiden fraglichen Märkten konnte kein Konkurrent wirklich Fuss fassen. Ywesee blieb Nischenanbieterin,
wurde als solche aber nicht komplett vom Markt verdrängt. Oben unter E. 12.5.16
wurde letztlich offengelassen, inwieweit dies tatsächlich auf die geltend gemachten Qualitätsunterschiede
der Konkurrenzangebote und/oder auf die Klauseln A und B in den Verträgen mit den Softwarehäusern
zurückzuführen ist. Die Klauseln A und B waren jedoch offensichtlich geeignet, den Markt für
potentielle Konkurrenzangebote zu verschliessen. Auch die vorgenommenen Koppelungen waren geeignet, potentielle
Wettbewerber zu verdrängen bzw. deren Wettbewerbsstellung zu verschlechtern. Zudem behinderten sie
auch die Zulassungsinhaberinnen, da diese die Qualitätssicherung mit optionalem Upload auf AIPS
bei HCI beziehen mussten, auch wenn sie dies gar nicht wünschten.
15.2.4.11 Zu
Recht erschwerend hat die Vorinstanz den Umstand beurteilt, dass die Verdrängungswirkungen insbesondere
in der Zeit, in der sich die Bedingungen änderten und damit für den Eintritt potentieller Konkurrenten
besonders geeignet gewesen wäre, ihre Wirkungen gezeigt haben.
15.2.4.12 Erfüllt
ein marktbeherrschendes Unternehmen durch sein Verhalten nebeneinander mehrere Tatbestände nach
Art. 7 Abs. 1 i.V.m. Abs. 2 Bst. a-f KG, ist zu prüfen, ob verschiedene Handlungsweisen vorliegen,
die separat zu beurteilen und entsprechend zu sanktionieren sind (Tagmann/Zirlick,
BSK-KG, Art. 49a N 52). Gemäss der neuesten Rechtsprechung des Bundesverwaltungsgerichts ist der
Umstand der Verwirklichung von zwei unterschiedlichen wettbewerbswidrigen Verhaltensweisen allerdings
nicht bei der Schwere des Verstosses und damit nicht beim Basisbetrag zu berücksichtigen, sondern
gemäss Art. 5 Abs. 1 Bst. a SVKG (wenn das Unternehmen "wiederholt gegen das Kartellgesetz
verstossen hat") unter den erschwerenden Umständen (Urteil des BVGer B-8386/2015 vom 24. Juni
2021, Swisscom WAN-Anbindung, E. 10.4.6 m.H.). Dies ist in casu
zu bejahen, da zwei verschiedene Verhaltensweisen vorliegen, die überdies auf zwei unterschiedlich
abgegrenzten Märkten ausgeübt wurden.
15.2.4.13 Im
Übrigen beanstanden die Beschwerdeführerinnen die vorinstanzlichen Erwägungen zu Recht,
soweit die Vorinstanz im Zusammenhang mit der Festlegung der Schwere der Wettbewerbswirkung erwog, hinter
der Verhaltensweise des Unternehmens habe eine Gesamtstrategie gestanden, um die Kontrolle über
die Gesamtwertschöpfung zu sichern. Eine solche Gesamtstrategie konnte HCI nicht in genügender
Weise nachgewiesen werden. Weitere Verhaltensweisen, die zwar untersucht wurden, sich jedoch nicht genügend
erhärten liessen, dürfen bei der Festlegung der Schwere der Wettbewerbsbeschränkung in
keiner Art und Weise Berücksichtigung finden. Hinweise auf das Verhalten bei der Ausschreibung von
AIPS oder auf die Heranziehung der Zulassungsinhaberinnen zur Sicherung von Einnahmen erweisen sich somit
als unsachgemäss.
15.2.4.14 Die
Beschwerdeführerinnen bringen des Weiteren vor, ihre Verhaltensweise sei das Resultat einer Anpassung
an die geänderten Rahmenbedingungen. Sie hätten im Interesse der Patientensicherheit nach wie
vor den hohen Qualitätsstandard gewährleisten wollen. Wie oben dargelegt (vgl. E. 9.2.2.13
und C.a.e),
bestand für die Zulassungsinhaberinnen bis 2011 ein faktischer Zwang die Fach- und Patienteninformationen
ihrer Arzneimittel in der Datenbank von Documed oder ywesee (kostenpflichtig) zu veröffentlichen.
Mit BVGE 2011/60 stellte das Bundesverwaltungsgericht fest, dass Swissmedic nicht befugt sei, die Veröffentlichung
der Arzneimittelinformationen in bestimmten privaten Datensammlungen zu verlangen. Zulässig bzw.
naheliegend sei eine Publikation durch Swissmedic selbst. Daraufhin gab Swissmedic diese jahrelange Praxis,
welche sich als unzulässig herausstellte, auf und entschied, eine eigene elektronische Datenbank
der Arzneimittelinformationen zu betreiben und es wurde das gegenwertig bestehende Arzneimittelinformationssystem
(AIPS) geschaffen. Somit wurde fortan der regulierte Bereich des Betriebes einer Arzneimitteldatenbank
für die Publikation der Arzneimittelinformationen im Sinne einer staatlichen Aufgabe von der Zulassungsbehörde
selbst übernommen. Die Beschwerdeführerinnen waren mit ihren Produkten der INDEX-Datenbanken
und des Compendiums entsprechend nur noch auf dem nachgelagerten Markt der Veredelung der Arzneimittelinformationen
tätig.
15.2.4.15 Das
staatlich vorgesehene System AIPS und der damit zusammenhängende Prozess inkl. Qualitätskontrolle
erwies sich allerdings punktuell als kompliziert. Zudem scheint es teilweise Mängel aufzuweisen
bzw. aufgewiesen zu haben (vgl. E. 13.8.12
f.). Die Beschwerdeführerin 2 hat - auch wenn sie ihre Marktmacht missbraucht hat -
mit ihrer erneuten Qualitätskontrolle Fehler in der Arzneimitteldatenbank ausbessern und mögliche
Medikationsfehler verhindern können. Auf jeden Fall darf ihr die punktuelle Mangelhaftigkeit des
Systems AIPS und des damit zusammenhängenden Prozesses nicht zum Nachteil gereichen. Entsprechend
ist bei der Festlegung des Basisbetrages zu berücksichtigen, dass der Bereich der Medikamenteninformationen
im relevanten Zeitraum einem ganz besonderen Regelungsumfeld unterlag (vgl. ähnlich: Urteile des
BVGer
B-4014/2013 und B-4019/2013 vom 30. Oktober 2019, Vertriebspartner/Auslieferer
von französischsprachigen Büchern, E. 20.3.4.4; Entscheidung der Kommission vom 15.
Oktober 2008 in einem Verfahren nach Artikel 81 EG-Vertrag [COMP/39.188, Abl. 2009 Nr. C 189/12 -
Bananen]). Dieses besondere Regelungsumfeld ist nicht
zuletzt auch auf die jahrelange unzulässige Praxis von Swissmedic zurückzuführen, welche
infolge des Urteils des Bundesverwaltungsgerichts BVGE 2011/60 beendet wurde (vgl. E. 9.2.2.13
und C.a.e).
Schliesslich ist der Vollständigkeit halber zu erwähnen, dass das Argument der Qualitätssicherung
demgegenüber keine Auswirkung auf die Bemessung des Basisbetrages hat (vgl. E. 12.4.37
ff.).
15.2.4.16 Die
Vorinstanz bezog bei der Schwere ferner das zumindest eventualvorsätzliche Handeln der ehemalige
Galenica-Gruppe negativ mit ein. Bei der zu untersuchenden Schwere des Verstosses handelt es sich jedoch
um eine objektive, d.h. verschuldensunabhängige Schwere (Andrea Doss,
Vertikalabreden und deren direkte Sanktionierung nach dem schweizerischen Kartellgesetz, Zürich
2009, Rz. 285; vgl. auch Dähler/Krauskopf/Stebler,
a.a.O., Rz. 8.122). Daher sind Aspekte, welche im Bereich der Verschuldensproblematik anzusiedeln sind,
in diesem Zusammenhang unbeachtlich (s. aber unten E. 15.2.7).
Zudem ist gemäss den Ausführungen in E. 15.1.16
f. ohnehin nur von einem fahrlässigen Verhalten auszugehen.
15.2.4.17 Ebenso
nicht erschwerend zu berücksichtigen ist, dass HCI die Verhaltensweise nach Eröffnung der Untersuchung
weitergeführt hat. Denn die Eröffnung eines Kartellverfahrens ist nicht mit einer Untersagung
des betreffend wirtschaftlichen Verhaltens gleichzusetzen (Urteil
B-7633/2009, ADSL
II, E. 690). Auch weisen die Beschwerdeführerinnen zutreffend daraufhin, dass dieser Aspekt
bereits bei der Dauer des Verstosses nach Art. 4 SVKG sanktionserhöhend berücksichtigt wird.
15.2.4.18 Auf
das Vorbringen, dass HCI vor Einführung der Verträge das Gespräch mit dem Sekretariat
gesucht habe, ist im Rahmen der Prüfung von mildernden Umständen einzugehen (s. unten E. 15.2.7).
15.2.4.19 Insgesamt
hat die Vorinstanz den Basisbetrag in der Verfügung im Vergleich mit dem Antrag mit Sicherheit zu
Recht von 10% auf 5% des massgeblichen Umsatzes gesenkt, auch wenn die Erwägungen selbst nur unwesentlich
angepasst wurden. Die volkswirtschaftliche Beeinträchtigung durch das missbräuchliche Verhalten
der Beschwerdeführerinnen ist als mittelschwer zu beurteilen. Da die Vorinstanz den Umstand der
Verwirklichung von mehreren Tathandlungen bei der Festlegung des Basisbetrages berücksichtigt hat,
dieser nach der neuesten Rechtsprechung aber unter den erschwerenden Umständen zu prüfen ist,
ist der von der Vorinstanz auf 5% des massgeblichen Umsatzes festgesetzte Basisbetrag entsprechend zu
reduzieren. Zusätzlich reduzierend zu berücksichtigen ist, dass der Bereich der Medikamenteninformationen
im relevanten Zeitraum einem besonderen Regelungsumfeld unterlag (vgl. E. 15.2.4.14
f.). Es erscheint deshalb angemessen, den Basisbetrag auf 4% des massgeblichen Umsatzes festzulegen.
Dies entspricht einem Basisbetrag in der Höhe von Fr. [...].
15.2.5 Berücksichtigung
der Dauer des Verstosses
15.2.5.1 Gemäss
Art. 49a Abs. 1 KG bemisst sich die Sanktion auch nach der Dauer des unzulässigen Verhaltens. Art.
4 SVKG konkretisiert diese Erhöhung dahingehend, als dass der Basisbetrag bei einer Dauer zwischen
einem und fünf Jahren um bis zu 50% und bei einer Dauer von mehr als fünf Jahren für jedes
weitere angefangene Jahr um bis zu 10% zu erhöhen ist.
15.2.5.2 Das
Bundesverwaltungsgericht hat im Urteil B-7633/2009 vom 14. September 2015 i.S. ADSL
II unter Berücksichtigung des Verhältnismässigkeitsgrundsatzes darauf abgestellt,
dass bei einem Wettbewerbsverstoss mit Dauercharakter, dem beim Fehlen von besonderen Umständen
von Anfang an im Wesentlichen die gleichen Wirkungen über die jeweilige Zeitdauer zuzusprechen sind,
während der ersten fünf Jahre grundsätzlich eine stufenweise Erhöhung um 0.8333%
je angefangenen Monat, seit dem das wettbewerbswidrige Verhalten durchgeführt wurde, vorzunehmen
ist. Soweit die nachteiligen Einwirkungen im Einzelfall nach Art und Inhalt der Wettbewerbsbeschränkungen
allerdings nicht gleichmässig über die gesamte Zeitdauer, sondern verstärkt während
bestimmter Phasen auftreten, bestünde auch die Möglichkeit zu einer variablen Ansetzung der
Erhöhung (Urteil B-7633/2009, ADSL
II, E. 755; vgl. auch B-831/2011, SIX,
E. 1600). Das Bundesgericht hat diese Erhöhung jüngst als bundesrechtskonform beurteilt (Urteil
2C_985/2015, ADSL II, E. 9.3). Vom
Bundesgericht wurde unter Berücksichtigung eines gewissen zulässigen Schematismus in einem
früheren Entscheid auch die stufenweise Erhöhung um 10% pro angefangenes Jahr für
die Dauer von einem bis fünf Jahren als bundesrechtskonform beurteilt (Urteil 2C.484/2010, Publigroupe,
E. 12.3.4 [nicht publizierte Erwägung in BGE 139 I 72]).
15.2.5.3 Die
Vorinstanz erwog, die Verhaltensweisen und die wettbewerbsschädigenden Effekte hätten mit der
Offertstellung an die Zulassungsinhaberinnen im September 2012 begonnen. Die Benachteiligungseffekte
hätten zwar erst ab dem Jahr 2013 Wirkung gezeigt, da die Verträge erst ab dann offeriert worden
seien. Aber die Märkte für potentielle Konkurrenten seien bereits ab Offertstellung verschlossen
worden. Für potentielle Konkurrenten sei nämlich bereits ab dann offensichtlich geworden, dass
Documed/e-mediat weiterhin über die Möglichkeit der Querfinanzierung verfügen würden.
Es sei von einer Dauerwirkung auszugehen, da das Verhalten während der gesamten Zeit die Zulassungsinhaberinnen
benachteiligt und potentielle Konkurrenten vom Markt ferngehalten habe. Somit sei ein linearer Massstab
anzuwenden, auch wenn die Verdrängungswirkungen besonders bei der Einführung von AIPS erfolgreich
gewesen seien.
15.2.5.4 Weiter
erwog die Vorinstanz, die Verhaltensweisen hätten bis zur Eröffnung der Verfügung (Mitte
Mai 2016) angehalten. Demzufolge sei von einer Dauer von 44 Monaten auszugehen und der Sanktionsbetrag
um 0.8333% je angefangenem Monat, um total 33.333% zu erhöhen.
15.2.5.5 Die
Beschwerdeführerinnen bringen vor, Konkurrenten hätten frühestens ab 1. Januar 2013 in
den Markt eintreten können. Entsprechend liege kein kartellrechtswidriges Verhalten auf die Wettbewerbssituation
im Jahr 2012 vor und die Dauer des Verstosses betrage ab 1. Januar 2013 nur 40 Monate. Da die Vorinstanz
in ihrer Berechnung aber scheinbar bereits mit 40 Monaten gerechnet habe, erscheine die Erhöhung
des Basisbetrages um 33.33% gerechtfertigt.
15.2.5.6 Wie
von der Vorinstanz zutreffend festgestellt, hat die wettbewerbswidrige Verhaltensweise der Koppelung
mit der Offertstellung an die Zulassungsinhaberinnen im September 2012 begonnen und bis zur Eröffnung
der angefochtenen Verfügung im Mai 2016 angehalten. Das entspricht einer Dauer von 44 Monaten. Bei
der effektiven Berechnung der Erhöhung des Basisbetrages ist der Vorinstanz, indem sie irrtümlicherweise
von 40 Monaten ausging, offensichtlich ein Berechnungsfehler unterlaufen. Dieser Berechnungsfehler ist
im Beschwerdeverfahren zu korrigieren. Entsprechend ist der Basisbetrag wegen der Dauer des wettbewerbswidrigen
Verhaltens um 36,652% bzw. um den Betrag von Fr. [...] zu erhöhen. Da die Sanktion im Beschwerdeverfahren
letztlich nicht höher ausfällt als in der angefochtenen Verfügung, liegt damit auch keine
reformatio in peius vor.
15.2.6 Erschwerende
Umstände
15.2.6.1 Gemäss
Art. 5 Abs. 1 SVKG wird der Sanktionsbetrag bei Vorliegen erschwerender Umstände erhöht. Als
erschwerende Umstände nennt Art. 5 Abs. 1 SVKG drei Gründe: (i) das Unternehmen hat wiederholt
gegen das Kartellgesetz verstossen, (ii) das Unternehmen hat mit dem Verstoss einen Gewinn erzielt, der
nach objektiver Ermittlung besonders hoch ausfällt, (iii) das Unternehmen hat die Zusammenarbeit
mit den Behörden verweigert oder versucht, die Untersuchungen sonst wie zu behindern.
15.2.6.2 Die
Aufzählung der erschwerenden Umstände, die zu einer Erhöhung des Sanktionsbetrages führen,
ist gemäss dem Wortlaut von Art. 5 Abs. 1 SVKG ("insbesondere") nicht abschliessend.
15.2.6.3 Vorliegend
ist eine allfällige Erhöhung aufgrund wiederholten Verstosses gegen das Kartellgesetz zu prüfen.
15.2.6.4 Die
Vorinstanz erwog, 2008 sei betreffend Documed eine unzulässige Verhaltensweise i.S.v. Art. 7 Abs.
1 i.V.m. Abs. 2 Bst. b KG rechtskräftig festgestellt worden. Da Documed bereits damals Teil der
Galenica-Gruppe gewesen sei und in der hier fraglichen Untersuchung bis zur Umstrukturierung Untersuchungsadressatin
gewesen sei, verstosse das Unternehmen vorliegend zum zweitem Mal gegen das Kartellgesetz. In beiden
Verfahren seien unzulässige Verhaltensweisen eines marktbeherrschenden Unternehmens i.S.v. Art.
7 KG festgestellt worden. Die Dauer seit dem letzten Verstoss sei kurz. Zum Zeitpunkt der Einführung
des neuen Angebotes ab Januar 2013 inkl. Offertstellung im Herbst 2012 seien weniger als fünf Jahre
seit dem Abschluss des Verfahrens i.S. Publikation von Arzneimittelinformationen
vergangen. Die kurze Dauer seit dem letzten Verstoss sowie die Gleichartigkeit des Verstosses seien erschwerend
zu berücksichtigen, womit eine Erhöhung des Sanktionsbetrages um 20% angemessen sei.
15.2.6.5 Weiter
erwog die Vorinstanz, das Sekretariat habe noch andere Verfahren gegen die Galenica-Gruppe geführt.
Die Vorabklärung i.S. Prewholesale - Lieferstopp durch Alloga
AG habe nicht zu einer Feststellung eines kartellrechtswidrigen Verhalten geführt. Da die
Vorabklärung ohne Folgen eingestellt worden und keine Untersuchung eröffnet worden sei, könne
dies nicht zu einer zusätzlichen Sanktionsschärfung herangezogen werden. In der Untersuchung
i.S. Hors-Liste Medikamente sei betreffend Galexis AG und e-mediat
festgestellt worden, dass diese Gehilfenhandlungen zu Abreden zwischen Pfizer AG, Eli Lilly (Suisse)
SA und Bayer (Schweiz) AG und den selbstdispensierenden Ärztinnen und Ärzte und Apotheken getätigt
habe und dadurch gegen das Kartellgesetz verstossen hätten. Da dieser Fall aufgrund des noch laufenden
Rechtsmittelverfahrens nicht rechtskräftig sei, könne auch daraus nicht auf einen wiederholten
Verstoss im Sinne eines "Rückfalls" geschlossen werden.
15.2.6.6 Die
Beschwerdeführerinnen bringen vor, im Schweizerischen Kartellrecht bestehe keine Praxis zur Frage,
wann ein Widerholungsfall vorliege und in welchem Ausmass eine solcher sanktionserhöhend zu berücksichtigen
sei. Deshalb sei auf die europäische Kartellrechtspraxis abzustellen. Danach gelte als entscheidendes
Kriterium die Gleichartigkeit zwischen der in der Vergangenheit festgestellten Zuwiderhandlung und der
neu zu beurteilenden Verhaltensweise. Vorliegend fehle es an dieser Gleichartigkeit. Zum einen seien
die Marktsituationen nicht vergleichbar. Der sachlich relevante Markt sei nicht gleich definiert worden.
Der Entscheid aus dem Jahr 2008 sei vor dem Systemwechsel 2013 ergangen, als die Zulassungsinhaberinnen
verpflichtet gewesen seien, ihre Arzneimittelinformationen bei Documed (oder ywesee) zu veröffentlichen,
um ihre gesetzliche Publikationspflicht zu erfüllen. In der heutigen Marktsituation erfolge die
Aufnahme in die INDEX-Datenbank auf freiwilliger Basis, die gesetzliche Publikationspflicht sei bereits
mit dem Upload der Medikamenteninformationen auf AIPS erfüllt. Zum anderen seien auch die Verhaltensweisen
nicht gleichartig. 2008 sei eine unzulässige Verhaltensweise nach Art. 7 Abs. 1 i.V.m. Abs. 2 Bst.
b KG, d.h. eine Diskriminierung von Handelspartnern festgestellt worden. Vorliegend gehe es um die unzulässigen
Verhaltensweisen der Einschränkung des Absatzes und der Koppelung.
15.2.6.7 Ferner
rügen die Beschwerdeführerinnen, die Vorinstanz unterstelle den Unternehmen der Galenica-Gruppe
durch die Hinweise auf die eingestellte Vorabklärung i.S. Prewholesale
- Lieferstopp durch Alloga AG und die nicht rechtskräftige
Verfügung i.S. Hors-Liste Medikamente eine Art generelle
Neigung, sich über die Regeln des Kartellgesetzes hinwegzusetzten.
15.2.6.8 Schliesslich
weisen die Beschwerdeführerinnen daraufhin, dass die rechtskräftig festgestellte unzulässige
Verhaltensweise der Documed als "relativ leichte Diskriminierungen von Handelspartnern" mit
geringen Auswirkungen und beschränkter Bedeutung qualifiziert worden sei, was auch die symbolische
Sanktion von Fr. 50'000.- zeige. Deshalb sei - wenn überhaupt - höchstens
eine Erhöhung um 10% vorzunehmen.
15.2.6.9 Die
Vorinstanz hält diesen Vorbringen entgegen, Art. 5 Abs. 1 Bst. a SVKG habe einen anderen Regelungsumfang
als die Bestimmung der EU. Art. 5 Abs. 1 Bst. a SVKG enthalte keine Eingrenzung auf gleichartige oder
ähnliche Verstösse. Das Vorbringen der Beschwerdeführerinnen, aufgrund fehlender Gleichartigkeit
könne keine Erhöhung vorgenommen werden, sei deshalb nicht stichhaltig. Die Gleichartigkeit
sei jedoch bei der Bemessung der Erhöhung von Bedeutung. Bei Verstössen gegen Art. 7 KG
sei von Gleichartigkeit auszugehen, da die unzulässige Verhaltensweise die Behinderung oder die
Ausbeutung durch Missbrauch der marktbeherrschenden Stellung darstelle. Nach dem Wortlaut und Sinn der
Bestimmung sei für die Frage, ob ein wiederholter Verstoss vorliege, die Art und Weise des Verstosses
nicht relevant.
15.2.6.10 Es
ist nachfolgend somit zu prüfen, ob die Vorinstanz das Vorliegen eines "wiederholten Verstosses"
zu Recht bejaht hat und ob die Erhöhung des Basisbetrages um 20% angemessen ist.
15.2.6.11 Nach
Art. 5 Abs. 1 Bst. a SVKG wird der Basisbetrag erhöht, wenn das Unternehmen widerholt gegen das
Kartellgesetz verstossen hat. Im Schweizerischen Kartellrecht gibt es bisher wenig Praxis zu den Fragen,
wann ein Wiederholungsfall in diesem Sinne vorliegt und in welchem Ausmass ein solcher sanktionserhöhend
zu berücksichtigen ist.
15.2.6.12 In
der EU-Bussenleitlinie 2006 (Leitlinien für das Verfahren zur Festsetzung von Geldbussen gemäss
Artikel 23 Absatz 2 Buchstabe a) der Verordnung [EG] Nr. 1/2003 [2006/C 210/02]) wird in Ziffer 28 festgehalten,
der Grundbetrag der Geldbusse könne erhöht werden, wenn die Kommission erschwerende Umstände
feststellt, wie beispielsweise die "Fortsetzung einer Zuwiderhandlung oder erneutes Begehen einer
gleichartigen oder ähnlichen Zuwiderhandlung, nachdem die Kommission oder eine einzelstaatliche
Wettbewerbsbehörde festgestellt hat, dass das Unternehmen gegen Artikel 81 oder Artikel 82 verstoßen
hatte; in diesem Fall wird der Grundbetrag für jeden festgestellten Verstoß um bis zu 100 %
erhöht".
15.2.6.13 Zur
Begründung einer solchen bussgelderschwerenden Widerholungstäterschaft, ist es nach der Praxis
der EU nicht erforderlich, dass die Zuwiderhandlungen im gleichen Marktsektor begangen wurden (Dannecker/Biermann,
in: Immenga/Mestmäcker, Wettbewerbsrecht, Band 1, EU/Teil 2, Kommentar zum Europäischen Kartellrecht,
6. Aufl. 2019, Art. 23 VO 1/2003, Rz. 190; Urteil des EuG vom 6. Mai 2005 T-122/04
Outokumpu und Luvata/Kommission, Slg.
2009 II-01135 Rn. 57). Es kommt vielmehr auf die Art der Zuwiderhandlung und die Identität des Unternehmens
an (Dannecker/Biermann, a.a.O., Rz. 190; Urteil des EuG
vom 13. Juli 2011 T-59/07 Polimeri Europa/Kommission, Slg. 2011
II-04687 Rn. 298 ff.). Die Leitlinien beziehen sich ausdrücklich auf ein erneutes Begehen einer
"gleichartigen oder ähnlichen Zuwiderhandlung". Die erschwerende Wirkung der Widerholungstäterschaft
wird darauf gestützt, dass die bereits zuvor verhängte Sanktion nicht abschreckend genug war
und eine erneute Begehung eine Neigung des betroffenen Unternehmens zur Begehung von Zuwiderhandlungen
gegen das Wettbewerbsrecht ausdrückt (Dannecker/Biermann,
a.a.O., Rz. 190; Urteil des EuG vom 30. September 2003 T-203/01
Michelin/Kommission, Slg. 2003 II-4071 Rz. 293; Urteil des EuG vom 25. Oktober 2005
T-38/02 Groupe Danone/Kommission,
Slg. 2005 II-04407 Rn. 347 ff.; bestätigt durch Urteil des EuGH vom 8. Februar 2007 C-3/06
P Groupe Danone/Kommission, Slg. 2007 I-1331 Rn. 39).
15.2.6.14 Der
EuGH hat aber auch klargestellt, das Verhältnismässigkeitsprinzip gebiete, die zeitliche Dimension
bei der Beurteilung der Neigung des Unternehmens zu Zuwiderhandlungen gegen die Wettbewerbsregeln zu
berücksichtigen. Zur Bemessung des Zeitraums, in dem vorangegangene Zuwiderhandlungen berücksichtigt
werden können, bezeichnet die Rechtsprechung des EuGH eine Zeitspanne von 10 Jahren noch als zu
kurz (Dannecker/Biermann, a.a.O., Rz. 191; Urteil des EuGH
vom 17. Juni 2010 C-413/08 P Lafarge/Kommission, Slg. 2010
I-05361 Rn. 70; Urteil des EuG vom 25. Oktober 2011 T-348/08 Aragonesas
Industrias y Energía/Kommission, Slg. 2011 II-07583
Rn. 68 ff.; Urteil EuGH Groupe Danone/Kommission,
Slg. 2007 I-1331 Rn. 40).
15.2.6.15 Der
Wortlaut von Art. 5 Abs. 1 Bst. a SVKG weicht von jenem der Bestimmung der EU ab. Es kann deshalb zur
Klärung der Frage, wann ein Wiederholungsfall i.S.v. Art. 5 Abs. 1 Bst. a SVKG vorliegt, nicht ohne
Weiteres auf die europäische Kartellrechtspraxis abgestellt werden. Die Leitlinie der EU und die
entsprechende Rechtsprechung können bei der Auslegung von Art. 5 Abs. 1 Bst. a SVKG jedoch zur Hilfe
genommen werden und Anhaltspunkte liefern.
15.2.6.16 Aus
nachfolgenden Gründen ist vorliegend ein Wiederholungsfall zu bejahen. Zum einen kann entgegen dem
Vorbringen der Beschwerdeführerinnen nicht vorausgesetzt werden, dass die Marktsituationen vergleichbar
sein müssen bzw. dass die Verhaltensweisen auf dem gleichen sachlich relevanten Markt begangen wurden.
Eine solche Regelung würde zu kurz greifen und auch in der europäischen Kartellrechtspraxis
wird nicht vorausgesetzt, dass die Zuwiderhandlungen im gleichen Marktsektor begangen wurden.
15.2.6.17 Zum
anderen kann auch nicht vorausgesetzt werden, dass es sich ausschliesslich um gleiche bzw. gleichartige
Zuwiderhandlungen handeln soll. Eine solche Einschränkung schliesst bereits der Wortlaut von Art. 5
Abs. 1 Bst. a SVKG aus. Zudem wiederspräche dies dem Sinn und Zweck, da der Erhöhung aufgrund
eines Wiederholungsfalles insbesondere der Gedanke zugrunde liegt, dass die zuvor verhängte Sanktion
nicht abschreckend genug war um eine Zuwiderhandlung gegen das Wettbewerbsrecht zu verhindern. Schliesslich
reicht auch im europäischen Wettbewerbsrecht nach dem Wortlaut von Ziffer 28 der EU-Bussenleitlinie
2006 eine ähnliche Zuwiderhandlung für die Bejahung einer bussgelderschwerenden Widerholungstäterschaft
aus. Vorliegend wurde 2008 betreffend Documed eine unzulässige Verhaltensweise i.S.v. Art. 7 Abs.
1 i.V.m. Abs. 2 Bst. b KG, mithin eine Diskriminierung von Handelspartnern rechtskräftig festgestellt.
Im vorliegenden Verfahren wurden unzulässige Verhaltensweisen i.S.v. Art. 7 Abs. 1 i.V.m. Abs. 2
Bst. e und f KG, mithin eine Einschränkung des Absatzes und eine Koppelung, festgestellt. Es handelt
sich damit um einen wiederholten Missbrauch der Marktmacht. Darüber hinaus handelt es sich bei der
Diskriminierung von Handelspartnern gleich wie bei der Einschränkung des Absatzes um einen typischen
Behinderungstatbestand (Stäuble/Schraner, DIKE-KG,
Art. 7 N 62). Somit kann eine Ähnlichkeit der Zuwiderhandlungen nicht abgesprochen werden. Es liegt
daher ein Wiederholungsfall vor, der bei der Sanktionsbemessung erschwerend zu berücksichtigen ist.
15.2.6.18 Was
die Vorabklärung i.S. Prewholesale - Lieferstopp Alloga AG
und das Verfahren i.S. Hors-Liste Medikamente betrifft, ist festzuhalten,
dass die Vorinstanz diese in ihren Erwägungen zwar genannt, sie jedoch bei der Sanktionsmessung
richtigerweise in keiner Art und Weise berücksichtigt hat.
15.2.6.19 Die
Erhöhung des Basisbetrages um 20% wegen Vorliegens eines Wiederholungsfalles i.S.v. Art. 5 Abs.1
Bst. a SVKG ist nicht zu beanstanden. Wie erwähnt kommt den Wettbewerbsbehörden bei der Gewichtung
der verschiedenen Kriterien zur Festlegung des Basisbetrags ein erheblicher Ermessensspielraum zu (Urteile
B-831/2011, SIX, E.
1593;
B-3332/2012, BMW,
E.11.2.6; B-463/2010, Gebro,
E.13.3.4; B-7633/2009, ADSL II,
Rz. 744). Die Vorinstanz hat nachvollziehbar aufgezeigt, von welchen Kriterien sie sich bei der
Bemessung der Erhöhung leiten liess. Eine Erhöhung um 20% erscheint auch im Vergleich zu den
Fällen von horizontalen Abreden, bei welchen die WEKO aufgrund wiederholter Verstösse innerhalb
eines Verfahrens einen Zuschlag erhoben hatte, angemessen (Rz. 413 f. der Verfügung der Vorinstanz
vom 18. Oktober 2010 in Sachen Baubeschläge für Fenster und
Fenstertüren [veröffentlicht in: RPW 2010/4 S. 717 ff., 763]; Rz. 978 der Verfügung
der Vorinstanz vom 22. April 2013 in Sachen Wettbewerbsabreden im Strassen-
und Tiefbau im Kanton Zürich [veröffentlicht in: RPW 2013/4 S. 524 ff., 626]; Rz. 1126
ff. der Verfügung der Vorinstanz vom 16. Dezember 2011 in Sachen Wettbewerbsabreden
im Strassen- und Tiefbau im Kanton Aargau [veröffentlicht in: RPW 2012/2 S. 270 ff.,
412]).
15.2.6.20 Die
Verwirklichung von zwei unterschiedlichen wettbewerbswidrigen Verhaltensweisen muss, anders als die Verletzung
zweier Tatbestände durch ein und dieselbe Handlung, zu einer verschärfenden Sanktionierung
führen (Urteil B-8386/2015, Swisscom WAN-Anbindung, E. 10.4.6).
Wie oben in E. 15.2.4.12
erwähnt ist dieser Umstand gemäss der neuesten Rechtsprechung des Bundesverwaltungsgerichts
nicht unter der Schwere des Verstosses und damit beim Basisbetrag zu berücksichtigen, sondern gemäss
Art. 5 Abs. 1 Bst. a SVKG unter den erschwerenden Umständen zu prüfen (Urteil B-8386/2015,
Swisscom WAN-Anbindung, E. 10.4.6 m.H.).
15.2.6.21 Vorliegend
hat die ehemalige Galenica-Gruppe mittels HCI einerseits eine Koppelung vorgenommen (Art. 7 Abs. 1. i.V.m.
Abs. 2 Bst. f KG), namentlich durch die Bündelung der Aufnahme der Arzneimittelinformationen in
ihre Datenbanken mit der Qualitätssicherung und dem Upload auf AIPS. Andererseits hat sie durch
die Klauseln A und B in den Verträgen mit den Softwarehäusern den Absatz der Konkurrenten i.S.v.
Art. 7 Abs. 1 i.V.m. Abs. 2 Bst. e KG einschränkt. Diese beiden Handlungen stehen nicht in
einem unauflösbaren Zusammenhang zueinander. Daher ist von einem Geschehensablauf mit zwei getrennten
Handlungen auszugehen, was als erschwerender Umstand zu berücksichtigen ist. Angemessen erscheint
hierfür eine zusätzliche Erhöhung des Basisbetrages um 12%.
15.2.6.22 Der
unter Berücksichtigung der Art und Schwere sowie der Dauer der Widerhandlung festgestellte Zwischenbetrag
(Fr. [...]) ist somit aufgrund erschwerender Umstände insgesamt um 32%
(Fr.
[...]) zu erhöhen.
15.2.7 Mildernde
Umstände
15.2.7.1 Gemäss
Art. 6 SVKG ist bei Vorliegen von mildernden Umständen eine Verminderung der Sanktion vorzunehmen.
Als mildernder Umstand wird in Art. 6 Abs. 1 SVKG die Einstellung der Wettbewerbsbeschränkung spätestens
vor Eröffnung eines Kartellverwaltungsverfahrens gemäss den Art. 26-30 KG statuiert. Dabei
müssen die eigenen Massnahmen derart sein, dass die wettbewerbswidrigen Handlungen aus eigenem Antrieb
eingestellt werden (Urteil 2C_985/2015, ADSL II, E. 9.4). Für
Preis- und Gebietsabsprachen gemäss Art. 5 Abs. 3 und 4 KG werden mit dem ausschliesslich passiven
Verhalten sowie dem Unterlassen von vereinbarten Vergeltungsmassnahmen zwei weitere Milderungsumstände
aufgeführt (Art. 6 Abs. 1 SVKG). Die Aufzählung ist nicht abschliessender Natur, was sich bereits
aus dem Wortlaut von Art. 6 Abs. 1 Satz 1 SVKG ("insbesondere") ergibt. Daher sind sonstige
mildernde Umstände auch bei der Sanktionierung eines wettbewerbswidrigen Verhaltens gemäss
Art. 7 KG zu berücksichtigen. Im Hinblick auf die entsprechenden Umstände ist zu beachten,
dass es sich hierbei nicht um Aspekte handeln kann, die bereits bei der Festlegung des Basisbetrags zu
berücksichtigen sind (Urteile
B-831/2011,
SIX, E. 1628; B-7633/2009,
ADSL II, E. 778).
15.2.7.2 Die
Vorinstanz kam zum Schluss, dass keine mildernden Umstände vorlägen. Die Verhaltensweisen seien
weder eingestellt worden, noch liege eine überdurchschnittliche Kooperation vor.
15.2.7.3
Demgegenüber stellen sich die Beschwerdeführerinnen auf den Standpunkt, die Kooperation
der HCI sei zwingend mildernd zu berücksichtigen. Sie hätten die Entwürfe der Verträge
mit den Zulassungsinhaberinnen dem Sekretariat von sich aus zugestellt und gegenüber den Wettbewerbsbehörden
stets transparent agiert. HCI habe nach dem Urteil des Bundesverwaltungsgerichts BVGE 2011/60 und der
Einführung von AIPS das Geschäftsmodell komplett überarbeiten müssen. Dabei habe
HCI das Gespräch mit dem Sekretariat gesucht und einen Besprechungstermin verlangt, um die Kartellrechtskonformität
des neuen Modells zu besprechen. Dieser sei jedoch vom Sekretariat abgesagt worden. Zudem hätten
sie mit dem Sekretariat Verhandlungen über den Abschluss einer einvernehmlichen Regelung geführt
und das Sekretariat eingeladen, vor Ort die Tätigkeit der HCI aufzuzeigen. Das Sekretariat habe
dieses Angebot ausgeschlagen und die Verhandlungen überraschend und abrupt abgebrochen. Insgesamt
hätten sie damit ein kooperatives Verhalten an den Tag gelegt, das über ein blosses Ausüben
der Verteidigungsrechte hinausgegangen sei sowie Wille und Bereitschaft für eine einvernehmliche
Lösung gezeigt. Mit dem eingereichten Ausstandsgesuch hätten sie im Übrigen ein verfassungsmässiges
Recht ausgeübt. Die Geltendmachung verfassungsmässiger Rechte dürfe nicht "erschwerend"
eingestuft werden.
15.2.7.4 Weiter
machen die Beschwerdeführerinnen geltend, in den Rahmenbedingungen zum Abschluss einer einvernehmlichen
Regelung sei explizit festgehalten worden, der Wille und die Bereitschaft zum Abschluss einer einvernehmlichen
Regelung werde vom Sekretariat als kooperatives Verhalten gewürdigt und im Rahmen des Antrages als
sanktionsmindernder Umstand berücksichtigt. Sie hätten ernsthaftes Interesse am Abschluss einer
einvernehmlichen Regelung gehabt. Der Abbruch der Verhandlungen durch das Sekretariat habe auf der mit
der Verfügung als unrichtig qualifizierten Prämisse des Sekretariates, dass die von den Zulassungsinhaberinnen
verlangten Gebühren gegen Art. 7 Abs. 2 Bst. c KG verstossen sollen, beruht.
15.2.7.5 Schliesslich
bringen die Beschwerdeführerinnen vor, HCI habe ihr Verhalten während der Untersuchung geändert
und den Gesprächsergebnissen mit dem Sekretariat angepasst. HCI habe beispielsweise die jährliche
Kündbarkeit der Verträge zugunsten der Zulassungsinhaberinnen eingeführt, die mutierten
Einträge von Nichtvertragspartnern in den Datenbanken belassen und in den ab 2015 geltenden Verträgen
mit den Softwarehäusern nicht mehr die beanstandete Klausel verwendet. Die Beschwerdeführerinnen
erachten eine Sanktionsmilderung von insgesamt 40% als geboten.
15.2.7.6
Die Vorinstanz hält hierzu in der Vernehmlassung fest, das Verfahren habe sich zu keinem
Zeitpunkt als besonders transparent dargestellt, vielmehr hätten intransparente Verhältnisse
geherrscht. Das Verfahren sei insbesondere durch das Ausstandsbegehren gegen Mitarbeitende des Sekretariates
und den Sistierungsantrag erschwert worden. Das Bundesverwaltungsgericht habe in der abgewiesenen Beschwerde
gegen die Verfügung des Präsidenten der WEKO betreffend das Ausstandsgesuch, sodann auch festgehalten,
"dass das Ausstandsbegehren offensichtlich unbegründet ist und die Beschwerde angesichts der
klaren Rechtslage zumindest an Trölerei grenzt".
15.2.7.7 Dass
die Parteien dem Sekretariat teilweise unaufgefordert Informationen haben zukommen lassen, stelle keine
über den gewöhnlichen Umfang hinausgehende ausserordentliche gute Kooperation dar. Die Mitteilung
der neuen Verträge hätte der Verteidigung gegen die im Raum stehenden Vorwürfe gedient.
Auch sei nicht schon die Bereitschaft zu Verhandlungen über eine einvernehmliche Regelung sanktionsmildernd
zu berücksichtigen, sondern nur der Abschluss einer einvernehmlichen Regelung. Dies sei auch in
den abgeschlossenen Rahmenbedingungen entsprechend festgehalten worden. Da sich die Vorinstanz und die
Beschwerdeführerinnen verpflichtet hätten, Aussagen und Standpunkte des Sekretariats aus den
Verhandlungen über eine einvernehmliche Regelung nicht als Beweismittel geltend zu machen, nehme
sie keine Stellung zu den Gründen, die zum Abbruch der Verhandlungen geführt hätten.
15.2.7.8 Eine
Sanktionsreduktion infolge des Abschlusses einer einvernehmlichen Regelung bzw. aufgrund des Willens
und der Bereitschaft der Partei zum Abschluss einer einvernehmlichen Regelung ist gesetzlich nicht explizit
vorgesehen. Die Vorinstanz hat den Abschluss einer einvernehmlichen Regelung in den bisherigen Sanktionsverfahren
i.S.v. Art. 49a Abs. 1 KG jedoch als gute Kooperation gewürdigt und mit einer Reduktion der Sanktion
honoriert. Der Reduktionsbetrag betrug zwischen 3 und 25% des Basisbetrags (Beuret,
DIKE-KG, Art. 29 N 44; RPW 2010/4 S. 717 Rz. 427 ff., Baubeschläge
für Fenster und Fenstertüren; Rz. 348 der Verfügung der Vorinstanz vom 10. Mai
2010 in Sachen Komponenten für Heiz- Kühl- und Sanitäranlagen
[veröffentlicht in: RPW 2012/3 S. 615ff, 652]; Rz. 303 ff. der Verfügung der Vorinstanz vom
23. Februar 2015 in Sachen Tunnelreinigung [veröffentlicht
in: RPW 2015/2 S. 193 ff, 240 ff.]; Rz. 313 ff. der Verfügung der Vorinstanz von 10. Dezember 2012
in Sachen Abrede im Speditionsbereich [veröffentlicht in:
RPW 2013/2 S. 142 ff., 202 f.]; Rz. 144 ff. der Verfügung der Vorinstanz vom 6. Juli 2009 in Sachen
Elektroinstallationsbetriebe Bern [veröffentlicht in: RPW
2009/3 S. 196 ff., 217 f.]; Rz. 208 ff. der Verfügung der Vorinstanz vom 29. Juni 2015 in Sachen
Saiteninstrumente [Gitarren und Bässe] und Zubehör [veröffentlicht
in: RPW 2016/3 S. 722 ff., 749]; Rz. 403 ff. der Verfügung der Vorinstanz vom 14. Dezember
2015 in Sachen Flügel und Klaviere [veröffentlicht in:
RPW 2016/3 S. 652 ff., 711]; vgl. auch Merkblatt des Sekretariats der WEKO: Einvernehmliche Regelungen
vom 28. Februar 2018, Rz. 11). Bei der Festlegung der Höhe der Sanktionsreduktion wird insbesondere
der Zeitpunkt des Abschlusses der einvernehmlichen Regelung berücksichtigt. Die Höhe der Reduktion
des Sanktionsbetrages hängt davon ab, wie früh im Verfahren die einvernehmliche Regelung zustande
kommt, ob durch den Abschluss der einvernehmlichen Regelung die Dauer des Verfahrens wesentlich verkürzt
und der Verfahrensaufwand der Wettbewerbsbehörden massgeblich reduziert werden kann (RPW 2014/4
S. 670 ff, 703, Preispolitik und andere Verhaltensweisen der SDA;
Beuret, DIKE-KG, Art. 29 N 44; Merkblatt des Sekretariats
der WEKO: Einvernehmliche Regelungen vom 28. Februar 2018, Rz. 11).
15.2.7.9 Die
Beschwerdeführerin 2 und das Sekretariat haben ab 2014 Gespräche und Verhandlungen über
eine einvernehmliche Regelung geführt. Die Verhandlung über eine einvernehmliche Regelung wurde
am 10. Juli 2015 durch das Sekretariat ohne Erfolg abgebrochen.
15.2.7.10 Am
27. Oktober 2014 wurden die Rahmenbedingungen für Verhandlungen über eine einvernehmliche Regelung
unterschrieben. Gemäss Ziffer 7 der Rahmenbedingungen vereinbarten die Beschwerdeführerin 2
und das Sekretariat, dass "der Wille und die Bereitschaft von HCl Solutions AG, e-mediat AG und
Documed AG zum Abschluss einer einvernehmlichen Regelung [...] vom Sekretariat als kooperatives Verhalten
gewürdigt und im Rahmen des Antrages als sanktionsmindernder Umstand berücksichtigt [werde]".
Weiter wurde vereinbart, dass im Falle eines Scheiterns der Verhandlungen über eine einvernehmliche
Regelung oder bei Nichtgenehmigung der einvernehmlichen Regelung der WEKO die Untersuchung im ordentlichen
Verfahren zu Ende geführt werde und das Sekretariat bei Vorliegen eines Verstosses eine Sanktion
beantrage, "ohne die gescheiterten Verhandlungen über eine einvernehmliche Regelung zu berücksichtigen"
(vgl. Vorinstanz, act. 1003, Ziff. 9).
15.2.7.11 Zwar
könnte bei einer isolierten Betrachtung aus der Formulierung "der Wille und die Bereitschaft
zum Abschluss einer einvernehmlichen Regelung werde als sanktionsmindernder Umstand berücksichtigt"
geschlossen werden, eine Sanktionsminderung sei auch für den Fall des Scheiterns der Verhandlungen
über eine einvernehmliche Regelung vereinbart worden. Einem solchen Schluss widerspricht jedoch
Ziffer 9 der vereinbarten Rahmenbedingung. Und auch vor dem Hintergrund der Praxis der Vorinstanz, wonach
einvernehmliche Regelungen bisher nur bei erfolgreichem Abschluss sanktionsmindernd berücksichtigt
wurden, hält ein solcher Schluss nicht Stand. Hinzukommt, dass Hintergrund der Sanktionsminderung
bei Abschluss einer einvernehmlichen Regelung die (wesentliche) Verkürzung oder Vereinfachung des
Verfahrens ist. Ein solcher verfahrensökonomische Vorteil liegt bei gescheiterten bzw. abgebrochenen
Verhandlungen gerade nicht vor. Die Vorinstanz hat die abgebrochenen Verhandlungen über eine einvernehmliche
Regelung damit unter diesem Titel zu Recht nicht sanktionsmindernd berücksichtigt.
15.2.7.12 Es
bleibt zu prüfen, ob ausserhalb einer einvernehmlichen Regelung eine besonders gute Kooperation
vorliegt, welche sanktionsmildernd zu berücksichtigen ist. Für eine Sanktionsmilderung aufgrund
guter Kooperation muss das Verhalten über das hinausgehen, was üblicherweise zur Ausübung
der Verteidigungsrechte an den Tag gelegt wird (Urteil B-506/2010, Gaba,
E. 14.4.5). Als nicht ausreichend betrachtet wird ein Verhalten, dass bereits nach den gesetzlich vorgesehenen
Mitwirkungspflichten geboten ist (insb. Auskunftspflicht nach Art. 40, vgl. auch Art. 13 Abs. 1 lit.
b und e VwVG; Tagmann/Zirlick, BSK-KG, Art. 49a N 74). Nach
dem Merkblatt des Sekretariats der WEKO vom 28. Februar 2018 betreffend einvernehmliche Regelungen soll
eine besonders gute Kooperation beispielsweise beim freiwilligen Einreichen von Beweismitteln oder bei
Anerkennung des Sachverhalts in Frage kommen. Gemäss Tagmann/Zirlick
kann eine positive, d.h. sanktionsmildernde Zusammenarbeit etwa im Liefern von Hinweisen und in der Erteilung
von Auskünften, nach welchen die Behörden nicht gefragt haben, bestehen (Tagmann/Zirlick,
BSK-KG, Art. 49a N 75).
15.2.7.13 Im
europäischen Wettbewerbsrecht kann gemäss Ziffer 29 4. Spiegelstrich der Leitlinien 2006
eine aktive Zusammenarbeit des Unternehmens mit der Kommission ausserhalb des Anwendungsbereichs der
Kronzeugenregelung und über seine rechtliche Verpflichtung hinaus bussgeldmindernd berücksichtigt
werden. Beispielsweise kann die Lieferung von Beweismaterial, ohne dass die Zuwiderhandlung nicht hätte
festgestellt werden können, bussgeldmindernd berücksichtigt werden. Dabei ist der Wert der
gelieferten Informationen für die Tätigkeit der Kommission beim Umfang der Milderung der Geldbusse
zu berücksichtigen (Dannecker/Biermann, a.a.O., Rz.
213; Entscheidung 2001/135/EG der Kommission vom 5. Juli 2000 betreffend ein Verfahren nach Artikel 81
EG-Vertrag COMP.F.1.36.516 Nathan-Bricolux, Abl. 2001 Nr. L 54/1
Rn. 134; Urteil des EuG vom 29. April 2004 T-236/01
Tokai Carbon/Kommission, Slg. 2004 II-1181 Rn. 435). Eine Milderung kommt dann in Betracht,
wenn die Arbeit der Kommission bei der Ermittlung einer Zuwiderhandlung erleichtert wird, wobei die einfache
Beantwortung eines Auskunftsersuchens, ein blosses Nichtbestreiten der Beschwerdepunkte oder die Abgabe
widersprüchlicher Erklärungen nicht ausreichen, um eine Erleichterung zu begründen (Dannecker/Biermann,
a.a.O., Rz. 213; Urteil des EuGH vom 16. November 2000 C-297/98 P
SCA Holding/Kommission, Slg. 2000
I-10101 Rn. 36; Entscheidung der Kommission
vom 16. Juli 2003 betreffend ein Verfahren nach Artikel 82 EG-Vertrag, COMP/38.233
Wanadoo Interactive, Rn. 412 [abrufbar unter: https://ec.europa.eu/competition/antitrust/cases/dec_docs/38233/38233_88_1.pdf
{abgerufen am 28.08.2020}]; Urteil des EuG vom 8. Juli 2004 T-44/00 Mannesmannröhren-Werke/Kommission,
Slg. 2004 II-2223 Rn. 271; Urteil des EuG vom 8. Juli 2004 T-48/00 Corus/Kommission,
Slg. 2004 II-2325 Rn. 198 f.).
15.2.7.14 Wie
erwähnt kommt den Wettbewerbsbehörden ein erheblicher Ermessensspielraum zu (Urteile
B-831/2011, SIX, E.
1593; B-3332/2012, BMW,
E.11.2.6; B-463/2010, Gebro,
E.13.3.4; B-7633/2009, ADSL II,
E. 744). Vor diesem Hintergrund ist der Schluss der Vorinstanz, es liege keine über
den gewöhnlichen Umfang hinausgehende ausserordentlich gute Kooperation vor, nicht zu beanstanden.
Zwar haben die Beschwerdeführerinnen teilweise von sich aus dem Sekretariat unaufgefordert Informationen
zukommen lassen, zum Beispiel in dem sie die neuen Verträge mit den Zulassungsinhaberinnen einreichten.
Hierbei handelt es sich jedoch nicht um Beweismaterial, ohne das die Zuwiderhandlung nicht hätte
festgestellt werden können. So weist die Vorinstanz zu Recht daraufhin, den Beschwerdeführerinnen
sei klar gewesen, dass das Sekretariat in Kontakt mit anderen Marktakteuren stand und daher ohnehin innert
kurzer Zeit Kenntnis von den neuen Verträgen erhalten würde, was schliesslich auch der Fall
war (vgl. Vorinstanz, act. 62). Auch aus der von den Beschwerdeführerinnen geltend gemachten Beratungsanfrage
lässt sich keine Sanktionsminderung im Sinne einer ausserordentlich guten Kooperation ableiten,
da im Rahmen eines kartellrechtlichen Untersuchungsverfahrens kein Raum für eine Beratung nach Art.
23 Abs. 2 KG besteht.
15.2.7.15 Die
Beschwerdeführerinnen machen schliesslich geltend, ihr Verhalten während der Untersuchung angepasst
zu haben. Gemäss dem einzigen beispielhaft aufgezählten Milderungsgrund in Art. 6 Abs. 1 SVKG
wird die Sanktion gemildert, wenn ein "Unternehmen die Wettbewerbsbeschränkung nach dem ersten
Eingreifen des Sekretariates der Wettbewerbskommission, spätestens aber vor Eröffnung eines
Verfahrens nach den Artikeln 26-30 beendet". Eine solche Konstellation liegt in casu offensichtlich
nicht vor. Eine Sanktionsmilderung rechtfertigt sich zudem auch aus folgenden Gründen nicht: Die
Beschwerdeführerin 2 hat ihr Verhalten während des laufenden Untersuchungsverfahrens nur teilweise
angepasst, insbesondere die vorgeworfene Koppelung wurde bis zum Erlass der Verfügung vom 16. Dezember
2016 durch die Vorinstanz aufrecht erhalten. Aber auch die absatzeinschränkenden Klauseln mit den
Softwarehäusern hat die Beschwerdeführerin 2 im Laufe des Untersuchungsverfahrens nur teilweise
ersetzt. Ab 2015 hat HCI die Klausel B in neuen Verträgen zwar nicht mehr verwendet, den Softwarehäusern
mit bestehendem Vertrag wurde jedoch gemäss den Angaben in der Eingabe der Beschwerdeführerinnen
vom 16. November 2018 erst im April 2017 mitgeteilt, dass sie nicht mehr an die Klausel B gebunden seien.
Zudem fliesst die Anpassung des Verhaltens resp. die Aufgabe der wettbewerbswidrigen Verhaltensweise
bereits im Zusammenhang mit der Berücksichtigung der Dauer des Verstosses in die Sanktionsbemessung
ein. Dadurch ist sie - wenn überhaupt - nur in Ausnahmefällen zusätzlich als
mildernder Umstand zu berücksichtigen, sofern es sich nicht um eine Einstellung der Wettbewerbsbeschränkung
aus eigenem Antrieb vor Eröffnung des Kartellverwaltungsverfahrens handelt.
15.2.7.16 Im
Ergebnis ist nicht zu beanstanden, wenn die Vorinstanz weder aufgrund der (abgebrochenen) Verhandlungen
über eine einvernehmliche Regelung noch aufgrund von sonstigem kooperativen Verhalten, noch aufgrund
einer Anpassung des Verhaltens der Beschwerdeführerinnen das Vorliegen von mildernden Umstände
bejahte. Es liegen keine Sanktionsmildernden Umstände i.S.v. Art. 6 SVKG vor.
15.2.8 Maximalsanktion
15.2.8.1 Gemäss
Art. 49a Abs. 1 KG und Art. 7 SVKG ist die Belastung in jedem Fall auf 10% des in den letzten drei Geschäftsjahren
erzielten Umsatzes des Unternehmens in der Schweiz als Maximalsanktion zu begrenzen.
15.2.8.2 Bei
Konzerngesellschaften sind sämtliche Umsätze der kontrollierten Gesellschaften in die Umsatzberechnung
einzubeziehen (Art. 5 Abs. 1 Bst. a-d VKU). Nicht zu berücksichtigen sind bei der Berechnung
des Gesamtumsatzes konzerninterne Umsätze (Art. 5 Abs. 2 VKU).
15.2.8.3 Die
Vorinstanz stellte auf die Geschäftsjahre 2013-2015 ab und kam zum Schluss, der kumulierte konsolidierte
Konzernumsatz der ehemaligen Galenica-Gruppe betrage Fr. [...] (2013: Fr. [...]; 2014: Fr.
[...]; 2014: Fr. [...]). Die zulässige Maximalsanktion legte die Vorinstanz auf Fr. [...]
fest.
15.2.8.4
Die Festlegung der Maximalsanktion durch die Vorinstanz wird von den Beschwerdeführerinnen
nicht gerügt. Im Übrigen erachtete es das Bundesverwaltungsgericht in seiner bisherigen Rechtsprechung
als zulässig, aus prozessökonomischen Gründen auf eine genaue Bestimmung der Maximalsanktion
zu verzichten, wenn die Sanktion tiefer als die Maximal-sanktion zustehen kommt (Urteil
B-3332/2012, BMW, E.11.2.4).
15.2.8.5 In
casu liegt der Sanktionsbetrag deutlich unterhalb der von der Vorinstanz berechneten Maximalsanktion,
weshalb auf eine genaue Bestimmung der Maximalsanktion durch das Bundesverwaltungsgericht verzichtet
werden kann.
15.2.9 Konkreter
Sanktionsbetrag
Wie die folgende Aufstellung zeigt, ist der Sanktionsbetrag von Fr. 4'546'123.- auf Fr.
3'778'794.- zu korrigieren:
|
Obergrenze Basisbetrag (Art. 3 SVKG)
|
Fr. [...]
|
|
Basisbetrag unter Berücksichtigung der Art und Schwere (Art. 3 SVKG)
|
Fr. [...]
|
|
Zuschlag wegen der Dauer des Verstosses (Art. 4 SVKG)
|
Fr. [...]
|
|
Betrag nach Art. 3 und 4 SVKG
|
Fr. [...]
|
|
Zuschlag wegen erschwerender Umstände (wiederholter Verstoss; Art. 5 SVKG)
|
Fr. [...]
|
|
Total
|
Fr. 3'778'794.-
|
16. Ergebnis
16.1 Die
Beschwerdeführerinnen haben die Aufhebung der Ziffern 1-5 der angefochtenen Verfügung verlangt,
eventualiter das Absehen von einer Sanktion und/oder von Verfahrenskosten bzw. eine Reduktion der Sanktion
und der Verfahrenskosten.
16.2 Der
Vorwurf des durch die angefochtene Verfügung festgestellten wettbewerbswidrigen Verhaltens wird
durch das vorliegende Urteil vollumfänglich bestätigt. Die ehemalige Galenica-Gruppe hat mittels
HCI ihre beherrschende Stellung auf dem Markt für veredelte, maschinenlesbare Daten betreffend Medikamenteninformationen
missbraucht, indem sie absatzeinschränkende Vertragsbestimmungen in den Verträgen mit den Softwarehäusern
verwendete (Art. 7 Abs. 1 i.V.m. Art. 7 Abs. 2 Bst. e KG). Zudem hat die ehemalige Galenica-Gruppe mittels
HCI ihre beherrschende Stellung auf dem Markt für die Aufnahme und den Erhalt in elektronischen
Datensätzen betreffend Medikamenteninformationen missbraucht, indem sie den Zulassungsinhaberinnen
die Aufnahme der Medikamenteninformationen in ihre INDEX-Datenbanken nur gebündelt mit der redaktionellen
und technischen Qualitätskontrolle und dem optionalem (Gratis-)Upload der Arzneimittelinformationen
auf AIPS anbot (Art. 7 Abs. 1 i.V.m. Art. 7 Abs. 2 Bst. f KG).
16.3 Die
selbstständige Feststellung einer marktbeherrschenden Stellung in der angefochtenen Verfügung
ist angesichts der neueren Rechtsprechung unter Berücksichtigung der Feststellungen zum wettbewerbswidrigen
Verhalten gemäss Art. 7 KG im Dispositiv nicht erforderlich. Ziffer 1 des Dispositivs der angefochtenen
Verfügung ist demzufolge aufzuheben. Die Aufhebung erlangt im vorliegenden Verfahren allerdings
keine selbständige inhaltliche Bedeutung.
16.4 Die
angeordneten Massnahmen betreffend die oben erwähnten festgestellten wettbewerbswidrigen Verhaltensweisen
in Ziffer 2 und 3 des Dispositivs der angefochtenen Verfügung sind an sich zu bestätigen. Zufolge
der Umstrukturierungen sind die Massnahmen jedoch nur der Beschwerdeführerin 2 aufzuerlegen.
16.5 Ziffer
5 des angefochtenen Dispositivs, mit welcher die Beweisanträge der Beschwerdeführerinnen abgewiesen
werden, bleibt ebenfalls stehen. Die Vorinstanz hat kein Verfahrensrecht verletzt, indem sie diese Beweisanträge
ablehnte. Im Übrigen lehnt auch das Bundesverwaltungsgericht im Beschwerdeverfahren die beantragten
Parteibefragungen ab, da es den Sachverhalt als genügend geklärt erachtet.
16.6 Die
Vorinstanz hat die Beschwerdeführerinnen zu Recht mit einer Verwaltungssanktion nach Art. 49a KG
belastet. In teilweiser Gutheissung der Beschwerde ist die Sanktion von Fr. 4'546'123.- auf Fr.
3'778'794.- herabzusetzen.
16.7 Das
vorliegende Urteil hat keine Auswirkungen auf die vorgenommene Verlegung der vorinstanzlichen Verfahrenskosten
und die dagegen erhobenen Rügen der Beschwerdeführerinnen erweisen sich nicht als stichhaltig
(s. unten E. 17.1).
Ziffer 6 des Dispositivs der angefochtenen Verfügung bleibt somit bestehen.
16.8 Im
Ergebnis bedeutet dies, dass neben der Anpassung des Dispositivs aus formellen Gründen und der teilweisen
Gutheissung der Beschwerde infolge der Reduktion der Sanktion, die Beschwerde im Übrigen abzuweisen
ist.
17. Kosten
und Entschädigung
17.1 Verfahrenskosten
vor der Vorinstanz
17.1.1 Die
Auferlegung von Kosten im vorinstanzlichen Verfahren richtet sich nach der Verordnung über die Gebühren
zum Kartellgesetz vom 25. Februar 1998 (Gebührenverordnung KG, GebV-KG, SR 251.2). Gebührenpflichtig
ist gemäss Art. 2 Abs. 1 GebV-KG, wer Verwaltungsverfahren verursacht oder Gutachten und sonstige
Dienstleistungen der WEKO oder des Sekretariats veranlasst. Keine Gebührenpflicht besteht gemäss
Art. 3 Abs. 2 GebV-KG für Beteiligte, die eine Vorabklärung oder eine Untersuchung verursacht
haben, sofern sich keine Anhaltspunkte für eine unzulässige Wettbewerbsbeschränkung ergeben
bzw. sich die vorliegenden Anhaltspunkte nicht erhärten und das Verfahren aus diesem Grunde eingestellt
wird. Die Gebühr bemisst sich gemäss Art. 4 GebV-KG nach dem Zeitaufwand. Wurde eine Verfügung
durch mehrere (juristische) Personen gemeinsam veranlasst, haften sie für die Gebühr solidarisch
(Art. 1a GebV-KG i.V.m. Art. 2 Abs. 2 Allgemeine Gebührenverordnung [AllgGebV, SR 172.041.1]).
17.1.2 Die
Vorinstanz auferlegte den Beschwerdeführerinnen eine Gebühr in der Höhe von Fr. [...].
Dabei erwog sie, dass in Anbetracht des vom Antrag des Sekretariates abweichenden Entscheides ein Abzug
in der Höhe eines Drittels der Kosten für diejenigen Tatbestände, welche sich nicht erhärtet
hätten, zu gewähren und zulasten der Staatskasse auszuscheiden sei.
17.1.3 Die
Beschwerdeführerinnen rügen, eine Untersuchung sei nur hinsichtlich der Punkte, die sich erhärten
und zum Erlass einer Verfügung führen, gebührenpflichtig. Vorliegend seien jedoch vier
der insgesamt sechs untersuchten Verhaltensweisen als nicht missbräuchlich qualifiziert worden und
hätten zu keiner Verurteilung geführt, weshalb die Gebührenpflicht bezüglich dieser
Punkte entfalle. Bei den beiden aufrecht erhaltenen Vorwürfen handle es sich nur um "Nebenschauplätze".
Folglich seien den Beschwerdeführerinnen die Kosten des vorinstanzlichen Verfahrens lediglich zu
einem Drittel aufzuerlegen.
17.1.4 Die
Vorinstanz macht hingegen in ihrer Vernehmlassung geltend, mit einer solchen schematischen Reduktion
im Verhältnis der Anzahl ursprünglich untersuchter Vorwürfe zu den erhärteten Vorwürfen
werde dem Umstand nicht Rechnung getragen, dass regelmässig - so auch vorliegend - ein
erheblicher Teil des Aufwands zur Erstellung des Sachverhalts und für das Verständnis des Marktes
anfalle. Dieser Aufwand sei unabhängig von der Anzahl Vorwürfe, die sich erhärten liessen.
Im Übrigen handle es sich um eine unzulässige Wertung zwischen den einzelnen Verhaltensweisen,
soweit die Beschwerdeführerinnen die erhärteten Verhaltensweisen als "Nebenschauplätze"
bezeichnen. Eine solche Wertung sei weder gesetzlich vorgesehen, noch habe sie, die Vorinstanz, eine
solche vorgenommen.
17.1.5 Das
Bundesverwaltungsgericht erwog im Urteil B-506/2010 vom 19. Dezember 2013 i.S. Gaba,
gebührenpflichtig sei nur, wer i.S.v. Art. 2 Abs. 1 GebV-KG eine Untersuchung verursacht habe und
nur hinsichtlich derjenigen Punkte, die sich erhärten liessen und die zum Erlass einer Verfügung
führten (Art. 3 Abs. 2 Bst. c GebV-KG). Der Beschwerdeführerin wurden darauf die Gebühren
nur zu einem Drittel auferlegt, da die angefochtene Verfügung nur hinsichtlich einem der drei Punkte
ergangen ist (Urteil B-506/2010, Gaba, E. 16.1.3).
17.1.6 Aus
dem Urteil B-506/2010 vom 19. Dezember 2013 i.S. Gaba kann jedoch
nicht geschlossen werden, die Gebühren seien in jedem Fall schematisch nach der Anzahl erhärteten
Punkte bzw. nicht erhärteten aufzuerlegen. Zu berücksichtigen bleiben die Umstände im
konkreten Einzelfall.
17.1.7 Eine
exakte Bemessung des Aufwands hinsichtlich jener Punkte, die sich nicht haben erhärten lassen und
bezüglich welcher das Verfahren eingestellt wird, ist in der Praxis regelmässig nicht möglich.
Es kann per se ein erheblicher Anteil des Aufwands auf die Erhebung des Sachverhalts und das Verständnis
des Marktes entfallen, welcher sich nicht einzelnen Vorwürfen zuordnen lässt. Die Vorinstanz
macht zu Recht geltend, dass dies vorliegend der Fall gewesen sei.
17.1.8 Indem
die Vorinstanz den Beschwerdeführerinnen bei dieser Ausgangslage Zweidrittel der Gebühren auferlegte,
verletzte sie weder Bundesrecht, noch hat die Vorinstanz ihr Ermessen überschritten oder missbraucht.
17.2 Kosten
und Entschädigung vor Bundesverwaltungsgericht
17.2.1 Die
Auferlegung der Verfahrenskosten, die sich aus Gerichtsgebühr und Auslagen zusammensetzen, sowie
die Zusprechung einer Parteientschädigung richten sich nach den Bestimmungen des Reglements des
Bundesverwaltungsgerichts vom 21. Februar 2008 über die Kosten und Entschädigungen vor dem
Bundesverwaltungsgericht (VGKE, SR 173.320.2) sowie den allgemeinen Bestimmungen von Art. 63 und
64 VwVG.
17.2.2 Die
Spruchgebühr bemisst sich nach Umfang und Schwierigkeit der Streitsache, Art der Prozessführung
und finanzieller Lage der Parteien (Art. 63 Abs. 4bis
Bst. b VwVG und Art. 2 Abs. 1 VGKE). Art. 4 VGKE sieht bei vermögensrechtlichen Streitigkeiten mit
einem Streitwert von Fr. 1'000'000.- bis Fr. 5'000'000.- eine Gerichtsgebühr zwischen
Fr. 7'000.- und Fr. 40'000.- vor. Wenn besondere Gründe es rechtfertigen, namentlich
mutwillige Prozessführung oder ausserordentlicher Aufwand, kann das Gericht über diesen Höchstbetrag
hinausgehen (Art. 2 Abs. 2 VGKE). Allerdings kann der in Art. 63 Abs. 4bis
VwVG festgesetzte Höchstbetrag von Fr. 50'000.- in keinem Fall überschritten werden
(Kiener/Rütsche/Kuhn, a.a.O., Rz. 1567; Moser/Beusch/Kneubühler,
a.a.O., Rz. 4.22a).
17.2.3 Die
vorliegende Angelegenheit erforderte nach Umfang und Schwere einen grossen Aufwand für ihre sachgerechte
Bearbeitung. Angesichts der angefochtenen Sanktion in der Höhe von Fr. 4'546'123.-, der angefochtenen
Verfahrenskosten in der Höhe von Fr. [...], des Aktenumfangs, des Instruktionsverfahrens sowie
des angefallenen Prüf- und Begründungsaufwands wird die Gerichtsgebühr auf Fr. 40'000.-
festgesetzt.
17.2.4 Gemäss
Art. 63 Abs. 1 VwVG hat das Bundesverwaltungsgericht die Verfahrenskosten entsprechend dem Unterliegerprinzip
der unterliegenden Partei aufzuerlegen. Unterliegt eine Partei nur teilweise, so werden die Verfahrenskosten
ermässigt. In diesem Falle sind die Kosten aufgrund eines allgemeinen prozessualen Grundsatzes im
Verhältnis des Obsiegens und Unterliegens zu verteilen (BGE 132 II 47 E. 3.3; Urteil B-7633/2009,
ADSL II, E. 802).
17.2.5 Die
Beschwerdeführerinnen wurden in der angefochtenen Verfügung zur Zahlung einer Sanktion von
Fr. 4'546'123.- plus Gebühren von Fr. [...] verurteilt. Die Sanktion wurde um Fr. 767'329.-
auf Fr. 3'778'794.- reduziert. Damit haben sie im Umfang von ca. 15% obsiegt. Die Verfahrenskosten
von Fr. 40'000.- sind demnach um den Betrag von Fr. 6'000.- zu reduzieren und auf Fr. 34'000.-
festzulegen. Diese Gebühr wird nach Rechtskraft des Urteils mit dem am 22. Mai 2017 von den Beschwerdeführerinnen
geleisteten Kostenvorschuss von Fr. 40'000.- verrechnet. Den Beschwerdeführerinnen ist der
Differenzbetrag in der Höhe von insgesamt Fr. 6'000.- innert 30 Tagen nach Rechtskraft des
Urteils auf das von ihnen anzugebende Konto zu überweisen.
17.2.6 Gemäss
Art. 64 Abs.1 VwVG ist einer ganz oder teilweise obsiegenden Partei von Amtes wegen oder auf Begehren
hin eine Entschädigung für die ihr erwachsenen notwendigen und verhältnismässig hohen
Kosten zuzusprechen (BVGE 2010/14 E. 8.2.1). Ausgenommen hiervon sind Bundesbehörden, denen gemäss
Art. 7 Abs. 3 VGKE kein Anspruch auf eine Parteientschädigung zusteht.
17.2.7 Die
teilweise obsiegenden Beschwerdeführerinnen haben am 16. November 2018 eine Kostennote eingereicht.
Ausgehend von einem Stundenansatz von Fr. [...] pro Stunde und einem Arbeitsaufwand von [...]
Stunden machen sie für das Verfahren vor dem Bundesverwaltungsgericht Parteikosten in der Höhe
von insgesamt Fr. 60'821.80 geltend. Dieser Betrag beinhaltet ein Anwaltshonorar von Fr. [...] sowie
Auslagen von Fr. [...].
17.2.8 Das
Anwaltshonorar bemisst sich nach dem notwendigen Zeitaufwand des Vertreters oder der Vertreterin (Art.
10 Abs. 1 VGKE). Der Stundenansatz beträgt für Anwälte und Anwältinnen mindestens
Fr. 200.- und höchstens Fr. 400.- (Art. 10 Abs. 2 VGKE). Das Gericht setzt die Parteientschädigung
auf Grund der eingereichten Kostennote oder - mangels Einreichung einer solchen - auf Grund
der Akten fest (Art. 14 Abs. 2 VGKE). Die Parteientschädigung umfasst nur die notwendigen Kosten
(Urteile des BGer 2C_343/2010 und 2C_344/2010 vom 11. April 2011 E. 8.3.4). Obsiegt eine Partei
wie im vorliegenden Fall nur teilweise, ist die Parteientschädigung entsprechend zu kürzen
(Art. 7 Abs. 2 VGKE).
17.2.9 Die
Beschwerdeführerinnen listen den geltend gemachten Arbeitsaufwand von [...] Stunden detailliert
und nachvollziehbar auf. Angesichts des unstrittig hohen Aufwands und der Komplexität der Streitsache
ist dieser Arbeitsaufwand nicht zu beanstanden. Ebenso nicht zu beanstanden sind die geltend gemachten
Auslagen von pauschal 3,5% des Anwaltshonorars. Die ungekürzte Parteientschädigung für
ein vollständiges Obsiegen würde somit Fr. 60'821.80 betragen. Unter Berücksichtigung
des nur teilweisen Obsiegens ist den Beschwerdeführerinnen zulasten der Vorinstanz eine um 17/20
gekürzte Parteientschädigung, d.h. insgesamt ausmachend Fr. 9'123.25 zuzusprechen. Diesen Betrag
hat die Vorinstanz nach Rechtskraft dieses Urteils an eine der Beschwerdeführerinnen zu entrichten
(Art. 64 Abs. 1 und 2 VwVG i.V.m. Art. 14 Abs. 2 VGKE).
Demnach erkennt das Bundesverwaltungsgericht:
1.
Die
Beschwerde gegen die Verfügung der Wettbewerbskommission (WEKO) vom 19. Dezember 2016 wird teilweise
gutgeheissen.
2.
Dispositiv-Ziffer
1 der angefochtenen Verfügung wird aufgehoben.
3.
Die
Dispositiv-Ziffern 2 und 3 werden mit Bezug auf die angeordneten Massnahmen wie folgt neu gefasst:
"HCI Solutions AG wird untersagt, in ihren Verträgen mit den
Softwarehäusern Vertragsklauseln zu verwenden und durchzusetzen, die eine Alleinbezugspflicht der
Softwarehäuser für zusätzliche Partner und Produkt-Stamm-Daten bei HCI Solutions AG oder
eine Untersagung der anderweitigen Verwendung der Strukturen der auf der Datenbank der HCI Solutions
AG beruhenden Software für die Softwarehäuser vorsehen.
HCI Solutions AG wird verpflichtet, den Zulassungsinhaberinnen die Dienstleistung
der Aufnahme der Medikamenteninformationen in die Indices und andere Dienstleistungen entbündelt
anzubieten. HCI Solutions AG wird verpflichtet, die redaktionelle und technische Qualitätskontrolle
der Arzneimittelinformationen sowie den Upload der Arzneimittelinformationen auf AIPS zu kostenbasierten
Preisen anzubieten."
4.
Dispositiv-Ziffer
4 der angefochtenen Verfügung wird mit Bezug auf die den Beschwerdeführerinnen auferlegte Sanktion
wie folgt neu gefasst:
"Vifor Pharma AG und HCI Solutions AG werden in Anwendung von Art.
49a Abs. 1 i.V.m. Art. 7 KG wegen unzulässiger Verhaltensweise mit einem Betrag von Fr. 3'778'794.-
belastet. Der Betrag von insgesamt Fr. 3'778'794.- wird den Adressaten der Verfügung unter
solidarischer Haftung auferlegt."
5.
Im
Übrigen wird die Beschwerde abgewiesen.
6.
Von
den Kosten des vorliegenden Verfahrens wird den Beschwerdeführerinnen zu gleichen Teilen und unter
solidarischer Haftung ein Betrag in der Höhe von Fr. 34'000.- auferlegt, welcher nach Rechtskraft
dieses Urteils dem geleisteten Kostenvorschuss in der Höhe von insgesamt Fr. 40'000.- entnommen
wird. Den Beschwerdeführerinnen wird der Differenzbetrag in der Höhe von Fr. 6'000.-
nach Rechtskraft des Urteils überwiesen.
7.
Die
Vorinstanz hat den Beschwerdeführerinnen nach Eintritt der Rechtskraft dieses Urteils eine reduzierte
Parteientschädigung von Fr. 9'123.25 zu bezahlen.
8.
Dieses
Urteil geht an die Beschwerdeführerinnen, die Vorinstanz und das Eidgenössische Departement
für Wirtschaft, Bildung und Forschung.
Für die Rechtsmittelbelehrung
wird auf die nächste Seite verwiesen.
|
Die vorsitzende Richterin:
|
Die Gerichtsschreiberin:
|
|
|
|
|
Vera Marantelli
|
Corine Knupp
|